
(12��)��29�ÊW�\(y��n)��(hu��)���ƻ����⚤�����Ǹߏ�(qi��ng)�ȵ��X�V�Ͻ�ij�n����(d��ng)С�M����(du��)�X�V�Ͻ��M(j��n)���о����y(c��)�������V���|(zh��)����?j��n)?sh��)�����������}�ᡢ�������c��Һ�O(sh��)Ӌ(j��)�����N��ͬ�Č�(sh��)�(y��n)������
����һ���X�V�Ͻ� �y(c��)�����ɚ��w���w�e
�y(c��)�����ɚ��w���w�e
���������X�V�Ͻ� �y(c��)�����ɚ��w���w�e
�y(c��)�����ɚ��w���w�e
���������X�V�Ͻ� ��Һ
��Һ �Q���Ɵ��a(ch��n)����|(zh��)����
�Q���Ɵ��a(ch��n)����|(zh��)����
��1����������һ�аl(f��)������(y��ng)���x�ӷ���ʽ ��
��2����(sh��)�(y��n)С�M����(j��)�������O(sh��)Ӌ(j��)�˃ɂ�(g��)��(sh��)�(y��n)�b�ã�����Ȧ(�D�е��F���_(t��i)��ʡ��)��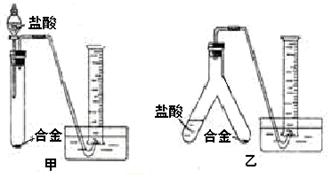
���J(r��n)���x�� ���x�����)�b���M(j��n)�Ќ�(sh��)�(y��n)���������`���С��
��3���÷������M(j��n)�Ќ�(sh��)�(y��n)�r(sh��)�����˷Q���Ɵ��a(ch��n)���|(zh��)���⣬߀��Q������ ��
��4����չ�о��������X�V�Ͻ������}������Һ�м����^��NaOH��Һ�r(sh��)�����ɳ������|(zh��)���c����NaOH��Һ�w�e���P(gu��n)ϵ���Ô�(sh��)�S�P(gu��n)ϵ��ʾ��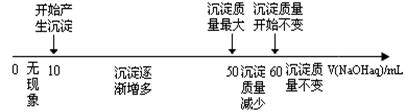
Ո(q��ng)���Д࣬����(j��)�ψD��(sh��)�S��Ĕ�(sh��)��(j��)�ܷ�����Ͻ����V���|(zh��)����?j��n)?sh��)? (�x��ܡ����ܡ�)
���Т٢ڃ��}�xһ�}����
������������Ͻ����V���|(zh��)����?j��n)?sh��)��Ո(q��ng)�f������ ��
����������Ͻ����V���|(zh��)����?j��n)?sh��)���t�V���|(zh��)����?j��n)?sh��)�� ������һλС��(sh��)����
��1��2Al+2OH-+2H2O=2AlO2-+3H2�� (3��)����2����(2��)
��3���Ͻ��Ʒ���|(zh��)��(2��) ��4����(2��) 30.8��(3��).
����ԇ�}��������1������һ�аl(f��)������(y��ng)���x�ӷ���ʽ��2Al+2OH-+2H2O=2AlO2-+3H2������2���ڶ���(g��)�b��ʹ�õăx���٣�������©�⣬�����������_ʼ�r(sh��)�Ͻ����Y�ܵ�һ��(g��)֧�ܣ��}�����Y����һ��(g��)֧���У��ڶ���δ���|�r(sh��)�����ܷ���(y��ng)�a(ch��n)�����w����(d��ng)��Y�ܹ܃Aб�r(sh��)����������|������(y��ng)�a(ch��n)����⣬�����������ݷe�^�����c�՚��M(j��n)�г�ֵ���s���أ����ʹ�Q���Ě��w���w�e���ӽ��挍(sh��)ֵ���`���^С�������b���M(j��n)�Ќ�(sh��)�(y��n)���������`���С����3���÷������M(j��n)�Ќ�(sh��)�(y��n)�r(sh��)��ԭ���w���V�X���ڽ�(j��ng)�^�}���ܽ�r(sh��)����Һ�к����Ȼ��V���Ȼ��X���}�ᣬ�������м����^����NaOH��Һ�r(sh��)����K�õ�����Mg(OH)2�����������^�V��ϴ�졢�Ɵ��������s���õ�����MgO,�������ԓ���������˷Q���Ɵ��a(ch��n)���|(zh��)���⣬߀��Q�������V�X�Ͻ��Ʒ���|(zh��)������4��Mg2+��Al3+�γɳ���һ������NaOH���w�e��40ml;�ܽ�Al(OH)3����NaOH���w�e��10ml,�t����Al3+����NaOH�w�e��30ml, ����Mg2+����NaOH�w�e��10ml,��������ͬ���w�e��(n��i)����NaOH�����|(zh��)������ȣ�����n(Al):n(Mg)=2:1������Mg���|(zh��)����?j��n)?sh��)��[24�£�24+2��27��]��100%=30.8��.
���c(di��n)�������X�V�Ͻ��Ʒ���|(zh��)����?j��n)?sh��)�Ĝy(c��)�������ı��^���x�ӷ���ʽ�ĕ�����������Ӌ(j��)���֪�R(sh��)��


 ��У�n��ϵ�д�
��У�n��ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�F��һ�N���͵��^�ɽ��٣��F���F�Ļ����������a(ch��n)���������ЏV���đ�(y��ng)�á��������Ӌ(j��)�㣺
��1����11.802 g䓘ӷ�ĩ��ֻ���F��̼���ڸߜ������������ļ����г�ַ���(y��ng)����s��õ�16.240 g���������F��
��䓘��к��F________g��
�����ɵ�CO2�ژ�(bi��o)��(zh��n)��r���w�e��________mL��
��2����10 mL�Ȼ��F��Һ�����}��0.001 mol���м���16.8 g 5%�ğ��A��Һ������������ַ���(y��ng)���^�V��ϴ���������ϴ��Һ�c�VҺ�ϲ���ϡ���250mL��ȡ25mLϡ�Һ����0.100 mol/L�}��ζ����K�c(di��n)�r(sh��)�����}����w�e15.50mL��Ӌ(j��)��ԭ��Һ��Fe3+�����|(zh��)������ȡ�
��3���F�P����Ҫ�ɷ�(sh��)���u�������F[���W(xu��)ʽFeO(OH)]����һ�K���P�FƬ����700mL pH��0��ϡ�����г�ַ���(y��ng)���ռ�����(bi��o)��(zh��n)��r��NO���w3.584 L����Kʣ��2.020g�F����
�ٷ���(y��ng)����Һ�����|(zh��)�ijɷ��c���|(zh��)������
��ԭ���P�FƬ���F�P���|(zh��)����?j��n)?sh��)��
��4����FeSO4��NaOH�Ƃ�Fe(OH)2�r(sh��)��������(hu��)�γ�һ�N�ҾGɫ�����g���X��ʾ������(j��ng)������X�к������N��x���c�ɷN�(y��ng)�x�ӣ�ꎡ��(y��ng)�x�ӵĿ��|(zh��)��֮�Ȟ�11:12����֪�ɷN�(y��ng)�x�Ӟ�Fe2+�cFe3+�����|(zh��)����֮�Ȟ�2:1��Ո(q��ng)ͨ�^Ӌ(j��)��_��X�Ļ��W(xu��)ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ������}
�ú���A12O3��SiO2������FeO��xFe2O3���X���Ƃ�A12(SO4)3��18H2O����ˇ�������£�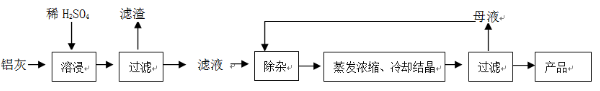
��һ���l���£�MnO4- ���cMn2+����(y��ng)����MnO2��
��֪�� ���ɚ������������pH
| | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| �_ʼ����r(sh��) | 3.4 | 6.3 | 2.7 |
| ��ȫ����r(sh��) | 5.2 | 9.7 | 3.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�Ӌ(j��)���}
��F��Ʒ��(j��ng)���M(j��n)�п��{(l��n)̎���������F��Ʒ�ı�������һ�����ܵ�Fe3O4��ij�W(xu��)��(x��)С�M�����о����{(l��n)�FƬ���քe�M(j��n)��������(sh��)�(y��n)������
�ٰ�һ�������{(l��n)�FƬ�ӹ��ɾ����ĩ��
��ȡm gԓ��ĩ������28.00 mL 1 mol��L���}���У�ǡ����ȫ����(y��ng)�����ɘ�(bi��o)��(zh��n)��r�µĚ��w134.4 mL������Һ�е���KSCN��Һ���o���@�F(xi��n)��
����ȡ���ݲ�ͬ�|(zh��)���ķ�ĩ���ּӼӵ���ͬ�w�e(V)�����|(zh��)������Ⱦ���l0.00 mol��L������������Һ�У���ַ���(y��ng)���wȫ���ܽ⣬���P(gu��n)�Č�(sh��)�(y��n)��(sh��)��(j��)���±���ʾ(���O(sh��)NO�������Ψһ߀ԭ�a(ch��n)��)��
| ��(sh��)�(y��n)��̖(h��o) | �� | �� | �� |
| �����ĩ�|(zh��)��/g | 13.68 | 27.36 | 34.20 |
| ���ɚ��w���w�e����(bi��o)��(zh��n)��r��/L | 2.912 | 5.824 | 6.720 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���(sh��)�(y��n)�}
��9�֣��oˮAlCl3��һ�N��Ҫ���ЙC(j��)�ϳɴ�����ԓ���|(zh��)��183��r(sh��)���A��������՚⼴�a(ch��n)���������F��ij�ЌW(xu��)���W(xu��)�dȤС�M�M�����ЌW(xu��)��Ҋ�x���O(sh��)Ӌ(j��)��(sh��)�(y��n)�Ƃ�oˮAlCl3����(sh��)�(y��n)�b�����D��ʾ��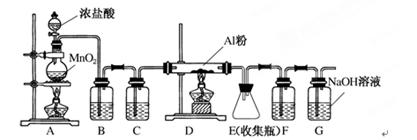
Ո(q��ng)�ش����І��}��
��1���Ƃ䌍(sh��)�(y��n)�_ʼ�r(sh��)���șz���b�õĚ����ԣ������IJ���������________��
a������MnO2��ĩ b���c(di��n)ȼA�оƾ��� c��������}�� d���c(di��n)ȼD̎�ƾ���
��2������A�b���аl(f��)������(y��ng)���x�ӷ���ʽ___________________________________��
��3���b��B�е�ԇ����__________��ԓ�b�ô��ڰ�ȫ�[����Ո(q��ng)ָ�� ��
��4����ͬ�W(xu��)�J(r��n)��F��G������һ�N�x��������Ҽ���һ�NˎƷ�����_(d��)����ͬЧ�����@�NˎƷ������____��
��5��E�еõ�������ɫ��ĩ�����_ܛľ��������@�^�쵽�F��ƿ���а��F���ɣ��û��W(xu��)����ʽ��ʾ��ԭ��____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���(sh��)�(y��n)�}
��16�֣��~�c�����ᷴ��(y��ng)����(sh��)�(y��n)�b����D��ʾ��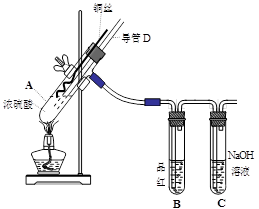
��1�� �b��A�аl(f��)������(y��ng)�Ļ��W(xu��)����ʽ�飺 ������(y��ng)�^����ԇ��B�еĬF(xi��n)���� ��ԇ��C�������� ��
��2�� ��(d��o)��D���¶�(̓����)��(y��ng)λ�� ��Һ���ϡ�Һ���£�����(d��o)��D�������У��ٌ�(sh��)�(y��n)�Y(ji��)�����ų��b���е�SO2���� ��
��(sh��)�(y��n)�аl(f��)�F(xi��n)ԇ�܃�(n��i)���ˮa(ch��n)����ɫ���w�⣬���~�z����߀�к�ɫ���w�����ɣ����п��ܺ���CuO��Cu2O��CuS��Cu2S����̽���ijɷ֣��M(j��n)�������µČ�(sh��)�(y��n)��
����Y�Ͽ�֪��Cu2O + 2HCl =CuCl2+ Cu + H2O�� 2Cu2O + O2�џ� 4CuO��2CuS+3O2�џ�2CuO+2SO2��Cu2S+2O2�џ�2CuO+SO2��CuS�� Cu2S��ϡHCl������(y��ng)��
|
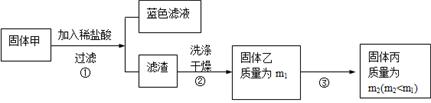 ��3�� ���w���ڿ՚����џ��r(sh��)��ʹ�õČ�(sh��)�(y��n)�x�����˲����������_�ܡ��ƾ����⣬߀����У� ��
��3�� ���w���ڿ՚����џ��r(sh��)��ʹ�õČ�(sh��)�(y��n)�x�����˲����������_�ܡ��ƾ����⣬߀����У� ���鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���(sh��)�(y��n)�}
��14�֣�FeSO4��7H2O�V�������t(y��)ˎ���I(y��)�I(l��ng)��������FeSO4��7H2O�Č�(sh��)�(y��n)���Ƃ����̈D������(j��)�}�����������գ�
(1)�Fм�cϡ���ᷴ��(y��ng)ǰ����(y��ng)��10% Na2CO3��Һ���ݎ�犣�����Ŀ����_____�����ݺ���____����������������x��ϴ���Fм��
(2)����a��_______________��
(3)���õ��ľG�\���w��������ˮϴ�죬��Ŀ���ǣ��ٳ�ȥ���w���渽����������s�|(zh��)��
��____________________��
(4) FeSO4��7H2O��ijЩ�a(b��)Ѫ?ji��ng)�����Ҫ�ɷ֣��?sh��)�(y��n)��Ҫ�y(c��)��ij�a(b��)Ѫ?ji��ng)����FԪ�صĺ�����
I������һ������KMn04��Һ�M(j��n)������߀ԭ�ζ���������100mL 1.00 �� 10 - 2 mol��L-1��KMnO4��Һ�r(sh��)�����õăx������ƽ��ˎ�ס���������������߀��___________����x�����Q�����������^���У������f�����_����____________������̖(h��o)��ĸ����
| A��KMnO4����ˮ���şᣬ����ֱ��������ƿ���ܽ� |
| B������ƿϴ�������T��ֱ�����ڌ�(sh��)�(y��n) |
| C�����ݺ�u��Һ����ڿ̶Ⱦ����ټ�ˮ����Һ������c(di��n)�c�̶Ⱦ���ƽ |
| D��������ݕr(sh��)��ˮ���^�̶Ⱦ����ع���� |

�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���(sh��)�(y��n)�}
�G�\��FeSO4?7H2O�����ί�ȱ�F��ؚѪ����Чˎ��ij�W(xu��)У�Ļ��W(xu��)�dȤС�M��ͬ�W(xu��)��(du��)�G�\�M(j��n)�������µ�̽����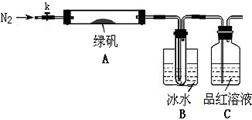
FeSO4?7H2O���Ƃ�
ԓ���W(xu��)�dȤС�M��ͬ�W(xu��)�ڌ�(sh��)�(y��n)��ͨ�^����(sh��)�(y��n)�ɏU�Fм�������������~�������F���s�|(zh��)���Ƃ�FeSO4��7H2O���w��
�ٌ�5%Na2CO3��Һ���뵽ʢ��һ�����U�Fм�ğ����У��ӟᔵ(sh��)��犣��ÃA������ȥ
Na2CO3��Һ��Ȼ�U�Fм��ˮϴ��2��3�顣
����ϴ���^�ďU�Fм�м����^����ϡ���ᣬ���Ɯض���50��80��֮�g���Fм�ıM��
�۳ß��^�V�����VҺ�D(zhu��n)�뵽���]�����У��o�á���s�Y(ji��)����
�ܴ��Y(ji��)���ꮅ�V�����w����������ˮϴ��2��3�Σ����ÞV�������w���ɣ�
���Ƶõ�FeSO4��7H2O���w����һ��(g��)С�V��ƿ�У����]���档
Ո(q��ng)�ش����І��}��
��1����(sh��)�(y��n)���E�ٵ�Ŀ��������������������������������
��2����(sh��)�(y��n)���E�����@����������������������������������������
��3������ϴ���ȥ���w���渽����������s�|(zh��)����(sh��)�(y��n)���E������������ˮϴ�쾧�w��ԭ������������������������������������������ ��
������̽���G�\��FeSO4��7H2O����ֽ�Įa(ch��n)��
��֪SO3�����c(di��n)��16.8��C�����c(di��n)��44.8��C��ԓС�M�O(sh��)Ӌ(j��)���D��ʾ�Č�(sh��)�(y��n)�b�ã��D�мӟᡢ�A�փx���Ⱦ�ʡ�ԣ���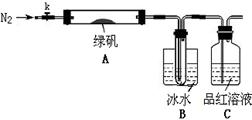
����(sh��)�(y��n)�^�̡�
�كx���B�Ӻz���b��A�cB�����ԣ�
��ȡһ�����G�\���w����A�У�ͨ��N2���(q��)�M�b�Ã�(n��i)�Ŀ՚⣬�P(gu��n)�]k���þƾ����ӟ�Ӳ�|(zh��)�����ܣ�
���^�쵽A �й��w��u׃�t��ɫ��B��ԇ���ռ����oɫҺ�w��C����Һ��ɫ��
�ܴ�A�з���(y��ng)��ȫ����s���Ҝغ�ȡ��������(y��ng)����w��ԇ���У����������ܽ⣬ȡ���������KSCN��Һ����Һ׃�tɫ��
����B�b�õ�ԇ���е����BaCl2��Һ����Һ׃���ᡣ
(4����(sh��)�(y��n)�Y(ji��)������
�Y(ji��)Փ1��B���ռ�����Һ�w�� ��
�Y(ji��)Փ2��C����Һ��ɫ������֪�a(ch��n)������ ��
�Y(ji��)Փ3���C�Ϸ���������(sh��)�(y��n)�ۺܿ͢���֪���w�a(ch��n)��һ����Fe2O3��
����(sh��)�(y��n)��˼��
��5��Ո(q��ng)ָ��ԓС�M�O(sh��)Ӌ(j��)�Č�(sh��)�(y��n)�b�õ����@���㣺 ��
��6���ֽ��Ĺ��w�п��ܺ�������FeO��ȡ������(sh��)�(y��n)�����}���ܽ�����Һ���S��ԇ���У��x��һ�Nԇ���b�e��ԓԇ������m���� ��
a����ˮ��KSCN��Һ b������KMnO4��Һ c��H2O2 d��NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���(sh��)�(y��n)�}
�F(xi��n)Ҫ�y(c��)��ij�Ȼ����F���Ȼ��F��������FԪ�ص��|(zh��)����?j��n)?sh��),�����²��E�M(j��n)�Ќ�(sh��)�(y��n):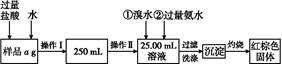
��.Ո(q��ng)����(j��)��������,�ش������}:
��1�����������õ��IJ����x������������������,߀���������������������������x�����Q����
��2��Ո(q��ng)����������ˮ�l(f��)�����x�ӷ���(y��ng)����ʽ: ����
��3����������ӟ�,��s���Ҝ�,����ƽ�Q�����|(zh��)����b1 g,�ٴμӟᲢ��s���ҜطQ�����|(zh��)����b2 g,��b1-b2="0.3" g,�t����߀��(y��ng)�M(j��n)�еIJ������� ��
�����l(f��)���|(zh��)����W1 g,���l(f��)���c�ӟ����w���|(zh��)����W2 g,�t��Ʒ���FԪ�ص��|(zh��)����?j��n)?sh��)������������������
��.��ͬ�W(xu��)���,߀���Բ������·�����y(c��)��: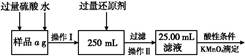
��1���ܽ��Ʒ����������,���������}��,��ʲô? ����
��2���x���߀ԭ���Ƿ������F������������ǡ���,ԭ����:�� ����
��3�����ζ��õ�c mol/L KMnO4��Һb mL,�t��Ʒ���FԪ�ص��|(zh��)����?j��n)?sh��)������������
�鿴�𰸺ͽ���>>
��(gu��)�H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com