
【化學—選修3:物質結構和性質】(15分)
元素周期表是研究元素原子結構及性質的重要工具。現有X、Y和Z三種元素,其原子序數依次減小。X元素原子的4p軌道上有3個未成對電子,Y元素原子的最外層2p軌道上有2個未成對電子,X跟Y可形成化合物X2Y3。Z元素既可以形成正一價離子也可形成負一價離子。請回答下列問題:
(1)Y元素原子的價層電子的軌道表示式為______________,該元素的名稱是_____;
(2)在X與Z形成的化合物XZ3中,X的雜化類型是 ,該化合物的空間構型為_____________;短周期元素形成的化合物中與XZ3互為等電子體的是 ;
(3)請寫出X的兩種含氧酸的化學式 、 ,其中酸性較強的是 。
(4)Q與Z同主族。Q單質的晶胞如下圖所示,若設該晶胞的密度為ag/cm3,阿伏加德羅常數為NA,Q原子的摩爾質量為M,則表示Q原子半徑的計算式為 。
(15分)
(1)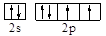 或
或 (2分) 氧。(1分)
(2分) 氧。(1分)
(2)sp3(2分),三角錐形。(1分)NH3、PH3(2分,每個1分)
(3)H3AsO3、H3AsO4。(共2分,各1分)H3AsO4(1分)
(4) 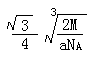 (4分,只要有這個式子即給4分,有無單位或對錯均不考慮。)
(4分,只要有這個式子即給4分,有無單位或對錯均不考慮。)
解析試題分析:X元素原子的4p軌道上有3個未成對電子,所以X是第四周期第五主族元素As元素;Y元素原子的最外層2p軌道上有2個未成對電子,則2p上的電子可能是2個也可能是4個,所以Y元素可能是C或O;X跟Y可形成化合物X2Y3,說明Y的化合價為-2價,所以Y是O元素;Z元素既可以形成正一價離子也可形成負一價離子,則Z是H元素。
(1)Y元素原子最外層6個電子,所以價電子的軌道表示式為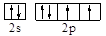 ;該元素是O;
;該元素是O;
(2)在X與Z形成的化合物XZ3中,即AsH3,As的價層電子對數=3+1/2(5-3)=4,所以As是sp3雜化;空間構型為三角錐型;短周期元素形成的化合物中與XZ3互為等電子體的是同主族元素的氫化物NH3、PH3;
(3)As的兩種含氧酸的化學式為H3AsO3、H3AsO4。根據酸性強弱的判斷依據,同種元素的化合價越高,其含氧酸的酸性越強,所以H3AsO4的酸性強;
(4)由圖可知,該晶胞中Q原子的個數是8×1/8+1=2,設晶胞的棱長為xcm,原子半徑為rcm,則4r=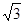 x,根據已知得a=2M/NAx3,可計算出x,所以r=
x,根據已知得a=2M/NAx3,可計算出x,所以r=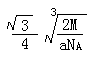
考點:考查元素推斷,物質結構與性質,晶胞計算


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:填空題
(10分)下圖是元素周期表短周期中11種元素的化臺價與原子序數的關系示意圖,請回答下列問題(用具體的元素符號作答):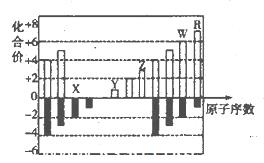
(1)元素x、Y、z、W、R五種元素中屬于金屬元素的是___________;Z的簡單離子的結構示意圖是___________。
(2)由此圖可以判斷,11種元素中處于同主族的共有____________組。
(3)X、Y.Z三種元素的原子半徑大小順序為___________;它們的離子的半徑大小順序為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2009年《自然》雜志報道了我國科學家通過測量SiO2中26Al和10Be兩種元素的比例確定“北京人”年齡的研究結果,這種測量方法叫“鋁鈹測年法”。 請完成下列填空:
(1)10Be和9Be 。(填序號)
a.具有相同的化學性質 b.Be 元素的近似相對原子質量是9.5
c.具有相同的中子數 d.通過化學變化可以實現10Be和9Be間的相互轉化
(2)研究表明26Al可以衰變為26Mg,可以比較這兩種元素金屬性強弱的方法是 。(填序號)
a.比較這兩種元素的單質的硬度和熔點
b.將空氣中放置已久的這兩種元素的單質分別和熱水作用
c.將打磨過的鎂帶和鋁片分別和熱水作用,并滴入酚酞溶液
d.在氯化鋁和氯化鎂的溶液中分別滴加過量的氫氧化鈉溶液
(3)目前還有一種測量方法叫“鉀氬測年法”。寫出和Ar核外電子排布相同的陰離子的半徑由大到小的順序 (用化學符號表示);其中一種離子與鉀相鄰元素的離子所形成的化合物可用做干操劑,此化合物的電子式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(15分)A、B、C、D、E為原子序數依次增大的元素,其中只有E不屬于短周期,相關信息如下表:
| 元素 | A | B | C | D | E |
| 相關 信息 | 最高正價與最低負價代數和為2 | 與元素C可形成離子個數比為2:1和1:1的化合物 | 單質質軟,通常保存在煤油中 | D元素可形成兩種氧化物,其中一種是形成酸雨的主要成分 | 其單質是用途最廣泛的金屬,人體缺少該元素易患貧血癥 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)現有A、B、C、D、E、F、G、H八種短周期主族元素,原子序數依次增大。已知A與E、D與G分別同主族;E、F、G、H同周期;A分別與C、D可形成含有10個電子的共價化合物M、N;B的最外層電子數是其電子層數的2倍;D是地殼中含量最多的元素;F位于B的前一主族。請回答下列問題:
(1)元素B在周期表中的位置 ,M的空間構型是 。
(2)A、D、E三種元素組成一種常見化合物,W與該化合物的陰離子具有相同的原子種類和數目且不帶電,W的電子式為 ,工業上利用某一個反應可同時生產該化合物和H的單質,寫出該反應的化學方程式 。
(3)E、F元素的最高價氧化物對應的水化物之間反應的離子方程式 。
(4)M、N均能結合H+,其中結合H+能力較強的是 (填化學式),用離子方程式證明 。
(5)E分別與D、G形成摩爾質量相等的化合物X、Y,其中Y的水溶液顯堿性的原因是 (用離子方程式表示)。常溫下7.8 g X與水反應放出Q kJ熱量(Q>0),寫出該反應的熱化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(12分) 類推法是科學學習的重要方法之一
⑴下列類推結論正確的是
| | 類比對象 | 結論 |
| A | Cl2+H2O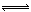 HCl+HClO HCl+HClO | I2+H2O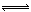 HI+HIO HI+HIO |
| B | C+2CuO ="==" 2Cu+CO2↑(條件:加熱) | C+SiO2 ="==" Si+ CO2↑(條件:加熱) |
| C | Na2O+H2O ="=" 2NaOH | CuO+H2O ="=" Cu(OH)2 |
| D | Ca(ClO)2+CO2+H2O="=" CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O="=" CaSO3↓+2HClO |
| 元素 | 8O | 16S | 34Se | 52Te |
| 單質熔點(℃) | -218.4 | 113 | | 450 |
| 單質沸點(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合價 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半徑 | 逐漸增大 | |||
| 單質與H2反應情況 | 點燃時易化合 | 加熱化合 | 加熱難化合 | 不能直接化合 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(10分)Q、W、X、Y、Z是原子序數依次增大的短周期元素,X、Y是金屬元素,Q、W、Z是非金屬元素。五種元素核電荷數之和為55,對應原子最外層電子數之和為21。W、Z最外層電子數相同,但Z的核電荷數是W的2倍。
(1)Q在周期表中位于第 周期 族。
(2)X、Y各自的最高價氧化物對應的水化物可以發生反應生成鹽和水,請寫出該反應的離子方程式: 。
(3)X單質能在W單質中燃燒可生成化合物R,R的電子式 ___,該物質所含有的化學鍵的類型為 。
(4)Z的氫化物與W的氫化物發生反應生成Z單質和水,寫出其化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(24分)下表是元素周期表的一部分,針對表中①~⑩種元素,填寫下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | | | | ① | ② | ③ | ④ | |
| 3 | ⑤ | ⑥ | ⑦ | | | | ⑧ | |
| 4 | ⑨ | ⑩ | | | | | | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E五種短周期元素,已知:
①原子半徑遞增順序為:A、D、C、B、E
②短周期(除稀有氣體元素外)所有元素中A的原子半徑與E的原子半徑之比為最小
③B、C、D三種元素電子層相同,三者原子序數之和為21,且D原子次外層電子數為最外層電子數的,
請回答下列問題:
(1)寫出E單質在D單質中燃燒產物的電子式: 。(2)C2A4·H2O與NH3·H2O相似,水溶液也呈弱堿性,用電離方程式表示其水溶液呈弱堿性的原因: 。(3)B、D、E三種元素可組成常見化合物X,A、B、D、E可組成常見化合物Y,X、Y均是生活中常見的化學試劑,它們在一定條件下可互相轉化。當a mol Y轉化成amol X時:(溶液中進行)
①若加入a mol純凈物Z就可實現轉化,則加入Z為 (填一種Z物質化學式)。②若加入0.5a mol純凈物Z就可實現轉化,則加入Z為 (填一種Z物質化學式)。(4)C2A4可用作高能燃料電池的燃料,生成物之一為C的單質,惰性材料作電極,KOH作電解質溶液構成原電池,寫出負極的電極反應: ;用該電池電解過量CuSO4溶液,共收集到3.36 L(標準狀況)的氣體,電池消耗6.4 g C2A4,則該燃料的利用率為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com