
I “套管實驗”是將一支較小的玻璃儀器裝入另外一個玻璃儀器中,經組裝來完成原來需要更多儀器進行的實驗。因其具有許多優點,被廣泛應用于化學實驗中,如圖實驗為“套管實驗”,小試管內塞有沾有無水硫酸銅粉末的棉花球。請觀察實驗裝置,分析實驗原理,回答下列問題: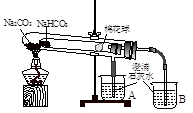
(1)該實驗的目的是_____________________
(2)實驗開始前微熱試管,說明裝置不漏氣的現象是
(3)一段時間后結束實驗,待裝置冷卻,取出小試管中固體溶于水,然后滴加1mol/L鹽酸,產生CO2的量與鹽酸的量的關系如圖所示。其中合理的是________________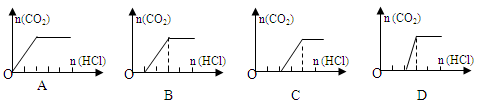
II燃料電池是一種連續的將燃料和氧化劑的化學能直接轉化為電能的化學電池。氫氣、烴、肼、甲醇等液體或氣體,均可以作燃料電池的燃料。請回答下列問題:
(1)以甲烷和氧氣為原料,氫氧化鈉溶液為電解質溶液構成電池。寫出其正極反應式
(2)以上述電池為電源,石墨為電極電解1L0. 1mol/L的氯化鉀溶液。回答下列問題:
寫出電解總反應的離子方程式 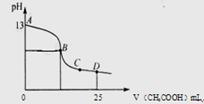
(3)室溫時,電解一段時間后,取25mL上述電解后溶液,滴加0.2mol/L醋酸,加入醋酸的體積與溶液的pH的關系如圖所示(不考慮能量損失和氣體溶于水,溶液體積變化忽略不計)
①計算消耗標準狀況下甲烷 mL
②若圖中的B點pH=7,則酸堿恰好完全反應的點在 區間(填“AB”、“BC”或“CD”)
③AB區間溶液中各離子濃度大小關系中可能正確的是
A. c(K+)>c(OH-)>c (CH3COO-) >c(H+)
B. c(K+)>c(CH3COO-)>c(OH-) >c(H+)
C. c(K+)>c(CH3COO-)=c(OH-) >c(H+)
(I)(1)探究(或證明)碳酸氫鈉不穩定,受熱易分成解產生CO2和H2O,而碳酸鈉穩定。
(2)A、B導管末端均有氣泡產生,冷卻后均有液柱回流(3)B、C
(II)(1)O2+2H2O+4e-=4OH— (2)2Cl—+2H2O 2OH—+H2↑+Cl2↑
2OH—+H2↑+Cl2↑
(3) ①280 ②A B ③A B C
解析試題分析:(I)(1)兩個試管內分別裝有Na2CO3、NaHCO3,給它們加熱,病用澄清的石灰水來檢驗CO2的產生。就是來探究二者的熱穩定性的相對大小。(2)實驗開始前微熱試管,說明裝置不漏氣的現象是A、B導管末端均有氣泡產生,冷卻后均形成穩定的水柱。(3)NaHCO3不穩定,受熱分解2NaHCO3 Na2CO3+2H2O+CO2↑。向固體中加入HCl時首先發生反應:Na2CO3+HCl=NaCl+NaHCO3;無氣體產生,當該反應完全后,再發生反應 NaHCO3+HCl=NaCl+H2O+ CO2↑。放出氣體。因此,若NaHCO3完全分解,則兩步消耗的HCl的物質的量相等,體積也相等。若它部分分解,則發生第一步消耗的HCl就比第二步少些。B為部分分解的圖像;C為完全分解的圖像。選項為BC。(II)(1)以甲烷和氧氣為原料,氫氧化鈉溶液為電解質溶液構成電池。其正極反應式為O2+2H2O+4e-=4OH—。(2)電解KCl溶液,陽離子放電能力H+>K+,所以H+在陰極放電產生氫氣,陰離子放電能力Cl->OH-。所以H+在陰極放電產生氯氣。總反應的離子方程式2Cl—+2H2O
Na2CO3+2H2O+CO2↑。向固體中加入HCl時首先發生反應:Na2CO3+HCl=NaCl+NaHCO3;無氣體產生,當該反應完全后,再發生反應 NaHCO3+HCl=NaCl+H2O+ CO2↑。放出氣體。因此,若NaHCO3完全分解,則兩步消耗的HCl的物質的量相等,體積也相等。若它部分分解,則發生第一步消耗的HCl就比第二步少些。B為部分分解的圖像;C為完全分解的圖像。選項為BC。(II)(1)以甲烷和氧氣為原料,氫氧化鈉溶液為電解質溶液構成電池。其正極反應式為O2+2H2O+4e-=4OH—。(2)電解KCl溶液,陽離子放電能力H+>K+,所以H+在陰極放電產生氫氣,陰離子放電能力Cl->OH-。所以H+在陰極放電產生氯氣。總反應的離子方程式2Cl—+2H2O  2OH—+H2↑+Cl2↑。(3)①開始時pH="13," c(OH-)="0.1mol/L," v(OH-)=1L,所以n(OH-)=0.1mol.根據方程式可知轉移電子0.1mol.則消耗CH4的物質的量為0.1mol÷8=0.0125mol,所以V(CH4)="0.0125mol×" 22.4 L/mol=0.28L=280ml.②酸堿恰好完全反應得到CH3COOK是強堿弱酸鹽,水解顯堿性,所以若圖中的B點pH=7,則酸堿恰好完全反應的點在AB間。③AB區間溶液可能是酸堿完全反應得到CH3COOK,也可能是KOH過量時的KOH與CH3COOK的混合溶液。若KOH過量,且KOH>CH3COOK,則離子濃度大小關系為c(K+)>c(OH-)>c (CH3COO-) >c(H+)A正確。若KOH<CH3COOK,存在關系:c(K+)>c(CH3COO-)>c(OH-) >c(H+);若恰好反應,由于CH3COO—水解消耗,促進了水的電離,最終使溶液中的離子c(OH-)>c(H+)。存在關系:c(K+)>c(CH3COO-)>c(OH-) >c(H+)。B正確。若產生的CH3COOK與剩余的KOH物質的量相等,則c(K+)>c(CH3COO-)=c(OH-) >c(H+)。C正確。因此選項為ABC。
2OH—+H2↑+Cl2↑。(3)①開始時pH="13," c(OH-)="0.1mol/L," v(OH-)=1L,所以n(OH-)=0.1mol.根據方程式可知轉移電子0.1mol.則消耗CH4的物質的量為0.1mol÷8=0.0125mol,所以V(CH4)="0.0125mol×" 22.4 L/mol=0.28L=280ml.②酸堿恰好完全反應得到CH3COOK是強堿弱酸鹽,水解顯堿性,所以若圖中的B點pH=7,則酸堿恰好完全反應的點在AB間。③AB區間溶液可能是酸堿完全反應得到CH3COOK,也可能是KOH過量時的KOH與CH3COOK的混合溶液。若KOH過量,且KOH>CH3COOK,則離子濃度大小關系為c(K+)>c(OH-)>c (CH3COO-) >c(H+)A正確。若KOH<CH3COOK,存在關系:c(K+)>c(CH3COO-)>c(OH-) >c(H+);若恰好反應,由于CH3COO—水解消耗,促進了水的電離,最終使溶液中的離子c(OH-)>c(H+)。存在關系:c(K+)>c(CH3COO-)>c(OH-) >c(H+)。B正確。若產生的CH3COOK與剩余的KOH物質的量相等,則c(K+)>c(CH3COO-)=c(OH-) >c(H+)。C正確。因此選項為ABC。
考點:考查Na2CO3、NaHCO3的熱穩定性及它們與酸反應的情況;電解原理、溶液中離子濃度的比較。


 天天向上課時同步訓練系列答案
天天向上課時同步訓練系列答案 陽光課堂同步練習系列答案
陽光課堂同步練習系列答案科目:高中化學 來源: 題型:填空題
氯化亞銅(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,熔點422
℃,沸點1366 ℃,在空氣中迅速被氧化成綠色,常用作有機合成工業中的催化劑。以粗鹽水(含Ca2+、Mg2+、SO42—等雜質)、Cu、稀硫酸、SO2等為原料合成CuCl的工藝流程如下: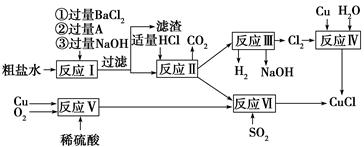
(1)A的化學式為________。
(2)寫出反應Ⅴ的化學方程式______________________________________
(3)寫出反應Ⅵ的離子方程式______________________________________
(4)本工藝中可以循環利用的物質是(用化學式表示)___________________________
(5)反應Ⅵ后,過濾得到CuCl沉淀,用無水乙醇洗滌沉淀,在真空干燥機內于70 ℃ 燥2小時,冷卻,密封包裝即得產品。于70 ℃真空干燥的目的是_________________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
日常生活中使用的鋁合金中的鋁來自于電解氧化鋁。工業上電解氧化鋁要求其純度不得低于98.2%,而天然鋁土礦的氧化鋁含量為50%~70%,雜質主要為SiO2、Fe2O3、CaO、MgO、Na2O等。工業生產鋁錠的工藝流程示意圖如下: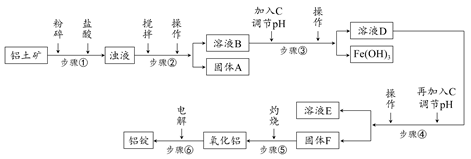
一些氫氧化物沉淀的pH如下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 |
| 開始沉淀pH(離子初始濃度0.01 mol/L) | 4 | 2.3 | 10.4 |
| 完全沉淀pH(離子濃度<10-5 mol/L) | 5.2 | 4.1 | 12.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
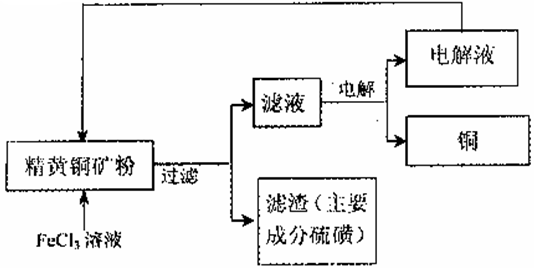
工業上以黃銅礦(主要成分CuFeS2)為原料制備金屬銅,有如下兩種工藝。
I.火法熔煉工藝:將處理過的黃銅礦加人石英,再通人空氣進行焙燒,即可制得粗銅。
(1)焙燒的總反應式可表示為:2CuFeS2 + 2SiO2+5O2=2Cu+2FeSi03+4SO2該反應的氧化劑是_____。
(2)下列處理SO2的方法,不合理的是_____
| A.高空排放 |
| B.用純堿溶液吸收制備亞硫酸鈉 |
| C.用氨水吸收后,再經氧化制備硫酸銨 |
| D.用BaCl2溶液吸收制備BaSO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
以硫鐵礦燒渣(含有氧化鐵和少量硫化亞鐵、二氧化硅等)為原料制備聚鐵{可表示為Fe2(OH)n(SO4)3-n/2,和綠礬(FeSO4.7H2O)具有成本低、反應快、產品質量高等優點。制備流程如下圖: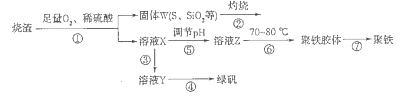
(1)流程圖中溶液X為Fe(SO4)3,溶液,據此寫出操作①中屬于氧化還原反應的離子方程式:____________。
(2)操作②的處理存在弊端,該弊端是_____________。若固體W與KOH溶液昆合加熱,其中一個反應的化學方程式為3S+6KOH 2K2S+K2SO3+3H2O,該反應的氧化劑與還原劑質量之比為___________。
2K2S+K2SO3+3H2O,該反應的氧化劑與還原劑質量之比為___________。
(3)操作③需要加入的物質(試劑)是_________,目的是___________________________。
(4)操作⑤是使溶液pH___________(填“增大”或“減小”)。
(5)操作⑥控制溫度為70 -80℃的目的是_________________________________________ 。
(6)雙氧水在酸性環境(硫酸)中是一種強氧化劑,可以將硫酸亞鐵氧化成三價鐵,制得Fe2(OH)n(SO4)3-n/2,反應的化學方程式為__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某學校化學興趣小組為探索金屬回收物的綜合利用,專門設計實驗用含有鋁、鐵、銅的合金制取純凈的氯化鋁溶液、綠礬晶體(FeSO4·7H2O)和膽礬晶體(CuSO4·5H2O),其實驗方案如下: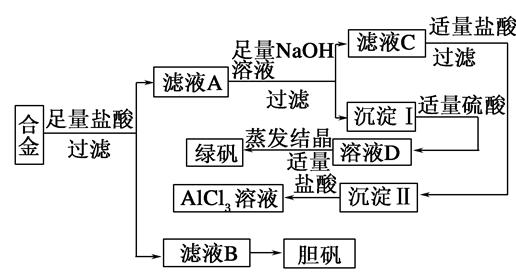
請回答下列問題:
(1)過濾用的玻璃儀器有________。
(2)小組成員經過檢測,發現制得的綠礬不純,試分析原因:________________________,要想由沉淀I最終制得純度較高的綠礬,應如何改進:______________________。
(3)小組成員從資料中獲知H2O2是一種綠色氧化劑,在濾渣B中加入稀硫酸和H2O2可以使B溶解,則該反應的化學方程式為______________________。
(4)有同學提出可將方案中最初溶解合金的鹽酸改用燒堿,重新設計方案,也能最終制得三種物質,你認為后者方案相對于前者方案________(填“更合理” 或“不合理”),理由是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
檸檬酸亞鐵(FeC6H6O7)是一種易吸收的高效鐵制劑,可由綠礬(FeSO4·7H2O)通過下列反應制備:
FeSO4+Na2CO3=FeCO3+Na2SO4
FeCO3+C6H8O7=FeC6H6O7+CO2+H2O
下表列出了相關金屬離子生成氫氧化物沉淀的pH(開始沉淀的pH按金屬離子濃度為1.0 mol·L-1計算)。
| 金屬離子 | 開始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氯化鐵是常見的水處理劑,無水FeCl3易升華。工業上制備無水FeCl3的一種工藝如圖所示:
(1)加入吸收塔的吸收劑X應是 (填字母編號)。
a.NaOH溶液 b.飽和食鹽水 c.FeCl2溶液 d.淀粉KI溶液
(2)取0.5 mL飽和FeCl3溶液滴入50 mL沸水中,得紅褐色氫氧化鐵膠體,則發生反應的離子方程式為 。
(3)實驗室中從FeCl3溶液制得FeCl3·6H2O晶體的過程中,需先加入 且保持過量,然后進行的操作依次為 、冷卻結晶、過濾。
(4)將H2S氣體通入FeCl3溶液中會出現渾濁,則其反應的離子方程式為 。
(5)鐵鉻氧化還原液流電池是一種低成本的儲能電池,電池結構如圖所示(電極材料為石墨),工作原理為:Fe3++Cr2+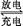 Fe2++Cr3+
Fe2++Cr3+
則電池放電時,Cl-將移向 極(填“正”或“負”);充電時,陰極的電極反應式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某廠的酸性工業廢水中含有一定量的Na+、Al3+、 Fe3+、Cu2+、Cl-。該廠利用如圖所示的工藝流程圖,利用常見的氣體氧化物、酸、堿和工業生產中的廢鐵屑,從廢水中生產出了氯化鐵、氧化鋁、NaCl晶體和金屬銅,產生了很好的社會經濟效益。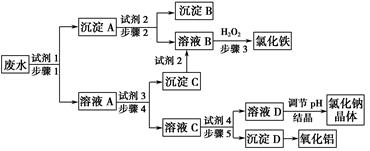
請填寫下列空白:
(1)圖中試劑1是________,試劑2是________。
(2)步驟1和步驟2所用到的玻璃儀器是________。
(3)步驟1反應的離子方程式為_______________________________________。
(4)步驟3反應的離子方程式為_______________________________________。
(5)從節約藥品和環保方面考慮,步驟5所發生反應的離子方程式應為__________________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com