
���F���(K2FeO4)���к�(qi��ng)�������ԣ������a(ch��n)���������ЏV����(y��ng)�á�
��1��K2FeO4��������Чˮ̎�턩����ɷN���÷քe�ǣߣߣߣߣߡ�
[��֪��FeO42����3e����4H2O Fe(OH)3��5OH��]
Fe(OH)3��5OH��]
��2���Ƃ�K2FeO4���Բ��Ý�ʽ���������������D��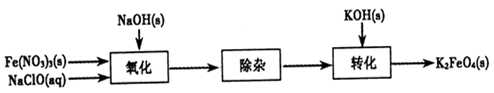
���������������x�ӷ���ʽ��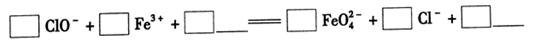
�ڳ��s����Ŀ���dz�ȥNa��FeO4��Һ�е��s�|(zh��)����ȥ���s�|(zh��)��Ҫ�Уߣߣߣߣ�(�����W(xu��)ʽ)��
���D(zhu��n)�����������ij�ض����M(j��n)�У��tԓ�ض����ܽ�ȣ�Na��FeO4�ߣߣߣߣ�K2FeO4 (�����������������)��
��3�������ģ�M���I(y��)늽ⷨ��ȡK2FeO4���b�����҈D��
�ٴ��b�����Դ��ؓ(f��)�O�ǣߣߣߣ�(�a����b��)��
��ꖘO��늘O����(y��ng)ʽ��ߣߣߣߣߣߡ�
��4����֪K2FeO4ϡ��Һ�д�������ƽ�⣺4FeO42����10H2O 4Fe(OH)3��8OH����3O2�����y��K2FeO4��Һ����c�ضȺ�pH���P(gu��n)ϵ�քe���D��ʾ��
4Fe(OH)3��8OH����3O2�����y��K2FeO4��Һ����c�ضȺ�pH���P(gu��n)ϵ�քe���D��ʾ��
���ɈDI�ɵó��ĽY(ji��)Փ��ԓ����(y��ng)�ġ��ȣߣߣ�0(�����������������)��
�ڈD����pH���ߣߣ�pH3(�����������������)��
��1������������ ��2����ClO2����2Fe3����10OH����2FeO42����3Cl����5H2O
��NaNO3��NaCl �ۣ� ��3����a ��Fe��6e����8OH����FeO42����4H2O
��4���٣� �ڣ�
����ԇ�}��������1����֪FeO42����3e����4H2O Fe(OH)3��5OH�����@�f��K2FeO4���Џ�(qi��ng)�����ԣ��ܚ����������������ɵ��F�x��ˮ�����ɚ������F�z�w���������ԣ�߀��ˮ�������á�
Fe(OH)3��5OH�����@�f��K2FeO4���Џ�(qi��ng)�����ԣ��ܚ����������������ɵ��F�x��ˮ�����ɚ������F�z�w���������ԣ�߀��ˮ�������á�
��2���ٸ���(j��)����ʽ��֪������(y��ng)����Ԫ�صĻ��σr��+1�r���͵���1�r���õ�2����ӡ��F�Ļ��σr��+3�r���ߵ�+6�r���õ�2����ӣ���˸���(j��)��ӵ�ʧ�غ��֪���������c߀ԭ�������|(zh��)����֮����3:2��������Һ�@�A�ԣ����Ը���(j��)ԭ���غ��֪������(y��ng)��߀��ˮ���ɣ��tԓ����(y��ng)���x�ӷ���ʽ��3ClO2����2Fe3����10OH����2FeO42����3Cl����5H2O��
�ڸ���(j��)ԭ���غ��֪������(y��ng)��߀�������c���Ȼ��c���ɣ����Գ��s��Ŀ���dz�ȥNaNO3��NaCl��
�۸���(j��)ԓ�ض��¸��F���c���D(zhu��n)������F��⛣����Ը���(j��)������������y�ķ����D(zhu��n)����֪�����F���c���ܽ�ȴ��ڸ��F��⛵��ܽ�ȡ�
��3����늽ⷨ��ȡK2FeO4���t����(y��ng)���F��(y��ng)ԓ��ʧȥ��ӣ������F��ꖘO�����b���Դ�����O��a�Ǵ��ڵ�ؓ(f��)�O��
���F��ꖘOʧȥ6����ӣ����ꖘO늘O����(y��ng)ʽ��Fe��6e����8OH����FeO42����4H2O��
��4�����ɈDI��֪���ض�T1�����_(d��)��ƽ���B(t��i)���@�f���ض�T1��ߡ����ضȸ�K2FeO4��Һ���ԽС���@�f�����ߜض�ƽ����������(y��ng)�����Ƅӣ����������(y��ng)�����ᷴ��(y��ng)����ԓ����(y��ng)�ġ��ȣ�0��
��pHԽС����Һ������Խ��(qi��ng)���t��Һ��OH��ԽС��������ƽ����������(y��ng)�����Ƅӡ����Ը���(j��)�D2��֪pH���rK2FeO4��Һ�����С�����pH��С��pH3��
���c�������̼���}�����á�����߀ԭ����(y��ng)����ʽ��ƽ���ܽ�ƽ�⡢늽�ԭ���đ�(y��ng)���Լ����l����ƽ���B(t��i)��Ӱ푵�


 �����Ļ��옷�����h������ϵ�д�
�����Ļ��옷�����h������ϵ�д� ��(y��u)�����옷����ÿһ��ȫ�º������I(y��)��ϵ�д�
��(y��u)�����옷����ÿһ��ȫ�º������I(y��)��ϵ�д� ��ٽ���ِ�½������������ϵ�д�
��ٽ���ِ�½������������ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
��Ҫ����ա�
(1)��S2����Fe2����Fe3����Mg2����S��I����H���У�ֻ�������Ե��� ��ֻ��߀ԭ�Ե��� ����������������߀ԭ�Ե��� ��
(2)ijͬ�W(xu��)���������������W(xu��)����ʽ(δ��ƽ)
��NO��HNO3�D��N2O3��H2O
��NH3��NO�D��HNO2��H2O
��N2O4��H2O�D��HNO3��HNO2
�������J(r��n)��һ�������܌��F(xi��n)���� ��
(3)������������߀ԭ����(y��ng)�У��������(qi��ng)�����|(zh��)�� ��
��2FeCl3��2KI=2FeCl2��2KCl��I(xi��n)2
��2FeCl2��Cl2=2FeCl3
��2KMnO4��16HCl(��)=2KCl��2MnCl2��5Cl2����8H2O
�����|(zh��)��Cl���cI�����棬��������I����Cl�����������������|(zh��)�⣬߀��(y��ng)����������(y��ng)�е� ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
���|(zh��)��ˮ��Һ���в�ͬ���О顣��Ҫ��ش����І��}��
��1��Na2SO3��Һ�@�A�ԣ���ԭ����______________________________(���x�ӷ���ʽ��ʾ)��ԓ��Һ�и��x�ӝ���ɴ�С������______________________��
��2���Ҝ�����10mL��ˮ��Һ�м�ˮϡጺ��������������__________(�̖����ͬ)���pС����___________����׃����____________��
a����Һ���x�ӝ�� b����ˮ����x�̶�
c��ˮ���x�ӷe����(sh��) d��c(H+)/ c(NH3��H2O)
��3���������c��NaClO2����һ�N��(qi��ng)������Ư�ׄ����V�����ڼ�����ӡȾ��ʳƷ���I(y��)��NaClO2׃�|(zh��)�ɷֽ��NaClO3��NaCl��ȡ���|(zh��)����׃�|(zh��)��δ׃�|(zh��)��NaClO2ԇ�Ӿ������Һ���քe�c����FeSO4��Һ����(y��ng)�r������Fe2+�����|(zh��)���� �����ͬ������ͬ��������ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
���F���(K2FeO4)��һ�N���͡���Ч����ܾGɫˮ̎�턩����Cl2��O2��ClO2��KMnO4�����Ը���(qi��ng)���o������Ⱦ�����I(y��)�������Ƶø��F���c��Ȼ���ڵ͜��£�����F���c��Һ�м���KOH��ͣ�ʹ���F���������
(1)�ɷ��Ƃ���F��⛵���Ҫ����(y��ng)�飺2FeSO4�� 6Na2O2=2Na2FeO4�� 2Na2O �� 2Na2SO4�� O2��
��ԓ����(y��ng)�е���������________��߀ԭ����________��ÿ����1 mol Na2FeO4�D(zhu��n)��________mol��ӡ�
�ں�Ҫ�f��K2FeO4����ˮ̎�턩�r���������__________________________________
(2)���Ƃ���F���(K2FeO4)�ķ���(y��ng)�wϵ�������N���ӣ�Fe(OH)3��ClO����OH����FeO42����Cl����H2O��
�ٌ�������ƽ���Ƹ��F��⛷���(y��ng)���x�ӷ���ʽ��____________________________
________________________________________________________________________��
��ÿ����1 mol FeO42���D(zhu��n)��________mol��ӣ�������(y��ng)�^�����D(zhu��n)����0.3 mol��ӣ��t߀ԭ�a(ch��n)������|(zh��)������________mol��
�۵͜��£��ڸ��F���c��Һ�м���KOH��Ϳ��������F���(K2FeO4)���f��ʲô���}_______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
��.ij���AС�M�O(sh��)Ӌ���a(ch��n)�������c��NaClO2������Ҫ������D��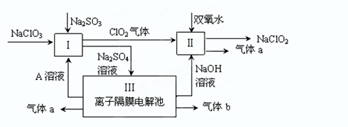
��֪NaClO2��һ�N��(qi��ng)������Ư�ׄ����V�����ڼ�����ӡȾ���I(y��)�����ډA�ԭh(hu��n)���з�(w��n)�����ڡ�
��1���p��ˮ�����ʽ�� ���b�â��аl(f��)������(y��ng)��߀ԭ������������������W(xu��)ʽ����
��2��A�Ļ��W(xu��)ʽ������ �����b�â�늽����A���������O�^(q��)�a(ch��n)�������b�â������ɚ��wa�� 11.2 L(��(bi��o)��(zh��n)��r)���t��Փ��ͨ�^늽�ص������������ ����֪�����ڳ���(sh��)F="9.65��l" 04C�� mol-1)��
��3���b�â��з���(y��ng)���x�ӷ���ʽ������������ ������ ��
��ij���BС�M�y�������a�Ͻ��Ʒ�ļ��ȣ��H�������\���~���M�ɾ�������Ʒ���������}��: Sn+ 2HCl=SnCl2+H2�����^�V��ϴ�졣���VҺ��ϴ��Һ�ϲ��ټ��^����FeCl3��Һ��������һ����ȵ�K2Cr2O7������Һ�ζ����ɵ�Fe2+���˕r߀ԭ�a(ch��n)���Cr3+���F(xi��n)���a�Ͻ�ԇ��1.23g����(j��ng)��������(y��ng)����������ȥ0.200mol/L��K2Cr2O7��������Һ15.00mL��
��4�� ��ʽӋ���Ʒ���a���|(zh��)����?j��n)?sh��)��
��5����������Ʒģ�M���I(y��)��늽⾫���a����D��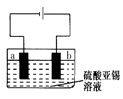
b�O�l(f��)��늘O����(y��ng)ʽ ����(d��ng)?sh��)õ?1.90g���a�r��늽��|(zh��)��Һ�|(zh��)���p�p0.54g���t�a�Ͻ��|(zh��)���p��_______ g���Y(ji��)������һλС��(sh��)����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
����������i��������ˮ���I(y��)��ˮ̎���I(l��ng)������M�������L�^�졣����ҿ��ö������i����Ҫԭ���Ƃ���i��⛡��䲿���������£�
(1)�ڢٲ��в����F�������ô�����ԭ����(�û��W(xu��)����ʽ��ʾ)________________________________________��
(2)KOH��KClO3��MnO2���۷���(y��ng)����ī�GɫK2MnO4�Ļ��W(xu��)����ʽ��________________________________________��
(3)�ڢܲ�ͨ��CO2����ʹMnO42���l(f��)������(y��ng)������MnO4����MnO2���tK2MnO4��ȫ����(y��ng)�r���D(zhu��n)����KMnO4�İٷ��ʼs��________(���_��0.1%)��
(4)�ڢݲ��ß��^�V��Ŀ����______________________________________��
(5)�ڢ��ӟ��s��Һ���м�(x��)С���w�����r��ֹͣ�ӟᣬ��s�Y(ji��)����________��ϴ�졢��������^���У��ضȲ����^�ߣ����____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�о�̼���仯����ľC�����Ì����M(j��n)��̼����Ę�(g��u)��������Ҫ�����x��Ո�\�����P(gu��n)֪�R�о�̼���仯��������|(zh��)��
��1����������҇�����{��̼���о�ȡ���ش��M(j��n)չ����늻����ϳɵ�̼�{���г����д���̼�{���w�����s�|(zh��)�����@�N̼�{���w�����������⻯���ἃ���䷴��(y��ng)�Ļ��W(xu��)����ʽ�飺______C��________K2Cr2O7��________����________CO2����________K2SO4��________Cr2��SO4��3��________H2O��
����ɲ���ƽ�������W(xu��)����ʽ��
�����������W(xu��)����ʽ�Ϙ�(bi��o)��ԓ����(y��ng)����D(zhu��n)�Ƶķ����c��(sh��)Ŀ��
��2���ߜؕr����CO߀ԭMgSO4���Ƃ��MgO��
��750��r���y�Ú��w�к������|(zh��)����SO2��SO3���˕r����(y��ng)�Ļ��W(xu��)����ʽ��_________________________________________________________��
����MgO���Ƴɡ��V���������}��ȼ��늳أ����b��ʾ��D��D��a����ʾ��ԓ늳ط���(y��ng)���x�ӷ���ʽ��________________________________________��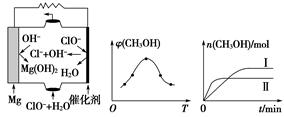
��a���������� ����b��������������c��
��3��������̼�ϳɼ״���̼�p�ŵ��·���CO2�D(zhu��n)����״��ğữ�W(xu��)����ʽ��CO2��g����3H2��g��  CH3OH��g����H2O��g������H��
CH3OH��g����H2O��g������H��
��ԓ����(y��ng)��ƽ�ⳣ��(sh��)���_(d��)ʽ��K��________��
��ȡ��ݵ��w�eCO2��H2�Ļ�Ϛ��w�����|(zh��)����֮�Ⱦ���1��3�����քe����ضȲ�ͬ���ݷe��ͬ�ĺ������]�����У��l(f��)����������(y��ng)������(y��ng)��ͬ�r�g�y�ü״����w�e��?j��n)?sh��)�գ�CH3OH���c����(y��ng)�ض�T���P(gu��n)ϵ������D��b����ʾ���t����CO2�D(zhu��n)����״�����(y��ng)�Ħ�H________�������������������0��
���ڃɷN��ͬ�l���°l(f��)������(y��ng)���y��CH3OH�����|(zh��)�����S�r�g׃����D��c����ʾ��������?q��)��?y��ng)��ƽ�ⳣ��(sh��)��С�P(gu��n)ϵ��K��________K�����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
����̼ѭ�h(hu��n)����������ĸ߶���ҕ������ν��ʹ����CO2�ĺ�������Ч���_�l(f��)����CO2��������ȫ������ձ���ҕ�����ԡ���̼��(j��ng)��(j��)�����ɞ�ƌW(xu��)���о�����Ҫ�n�}��
��1����늻����ϳɵă���{��̼�ܳ����д�����̼�{���w�����s�|(zh��)�����@�N�w�����������������ἃ��Ո���ԓ����(y��ng)�Ļ��W(xu��)����ʽ��(����ƽ���ϵ��(sh��)���ڙM����)
__ C+ __ KMnO4+ ___ H2SO4��___CO2��+ ___MnSO4 + ___K2SO4+ ___H2O
��(d��ng)����(y��ng)����2��408��1024����Ӱl(f��)���D(zhu��n)�ƕr��߀ԭ�����|(zh��)����
��2������ͬ����CO��g����H2O��g���քeͨ�뵽�w�e��2 L�ĺ������]�����У��M(j��n)�з���(y��ng)CO��g����H2O��g��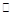 CO2��g����H2��g�����õ����ɽM��(sh��)��(j��)��
CO2��g����H2��g�����õ����ɽM��(sh��)��(j��)��
| ���M | �ضȡ� | ��ʼ��/mol | ƽ����/mol | �_(d��)��ƽ������r�g/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | x | 2��0 | 1��6 | 2��4 | 6 |
| 2 | 900 | 2��0 | 1��0 | 0��4 | 1��6 | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
���F���(K2FeO4)��һ�N��������������������һ�w�����Ͷ��ˮ̎�턩�������a(ch��n)��ˇ�������£�
Ոͬ�����І��}��
(l)������KOH��Һ��ͨ������Cl2�l(f��)������(y��ng)���x�ӷ���ʽ_______ ��
��2������ҺI�м���KOH���w��Ŀ����______���̖����
| A������һ������(y��ng)�ṩ�A�Եĭh(hu��n)�� |
| B��ʹKClO3�D(zhu��n)����KClO |
| C���c��ҺI���^����Cl2�^�m(x��)����(y��ng)�����ɸ����KClO |
| D��KOH���w�ܽ�r���ų��^��ğ�������������߷���(y��ng)���� |

�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com