
合成氨工業對國民經濟和社會發展具有重要的意義。其原理為: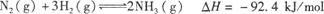 ,據此回答以下問題:
,據此回答以下問題:
(1)①該反應的化學平衡常數表達式為K= 。
②根據溫度對化學平衡的影響規律可知,對于該反應,溫度越高,其平衡常數的值越 。
(2)某溫度下,若把10 mol N2與30 mol H2置于體積為10 L的密閉容器內,反應達到平衡狀態時,測得混合氣體中氨的體積分數為20%,則該溫度下反應的K= (可用分數表示)。
能說明該反應達到化學平衡狀態的是 (填字母)。
a.容器內的密度保持不變 b.容器內壓強保持不變
c.v正(N2)=2v逆(NH3) d.混合氣體中c(NH3)不變
(3)對于合成氨反應而言,下列有關圖像一定正確的是(選填序號) 。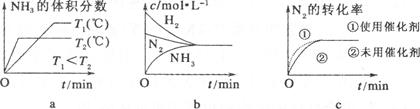
(4)相同溫度下,有恒容密閉容器A和恒壓密閉容器B,兩容器中均充入1 mol N2和3 mol H2,此時兩容器的體積相等。在一定條件下反應達到平衡狀態,A中NH3的體積分數為a,放出熱量Q1kJ;B中NH3的體積分數為b,放出熱量Q2kJ。則:a b(填“>”、“<”或“=”,下同),Q1 Q2,Q1 92.4。
(1)①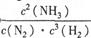 (2分) ②小(1分)
(2分) ②小(1分)
(2)1/12 (2分) bd (2分) (3)ac (2分) (4)< (2分) < (2分) <(2分)
解析試題分析:(1)①K為生成物濃度冪之積與反應物濃度冪之積的比,則K=c2(NH3)/c(N2)c3(H2)②該反應為熱反應,升高溫度,平衡逆向移動,則平衡常數K減小,溫度越高,K越小。
N2(g)+3H2(g)?2NH3(g)
開始 1 3 0
轉化 x 3x 2x
平衡1-x 3-3x 2x
平衡混合氣體中氨的體積分數為20%,2x/(1?x+3?3x+2x)×100%="20%" 解得x=1/3,平衡常數K=1/12; 由平衡的特征“等”、“定”可判定平衡,則a.容器的體積、氣體的質量始終不變,則容器內的密度保持不變,不能判斷平衡,故a錯誤;b.該反應為反應前后體積不等的反應,則容器內壓強保持不變,達到平衡,故b正確;c.υ正(N2)=2υ逆(NH3),正逆反應速率不等,反應沒有達到平衡,故c錯誤; d.混合氣體中 c(NH3)不變,為平衡的特征,達到平衡,故d正確;(3)a.先出現拐點的先達到平衡,則T2大,溫度高,平衡逆向移動,與圖象一致,故a正確;b.平衡時濃度不一定相等,平衡濃度取決起始濃度和轉化率,圖象表示錯誤,故b錯誤;c.使用催化劑加快反應速率,對平衡無影響,平衡時物質的濃度不變,與圖象一致,故c正確;(4)恒容密閉容器A,反應達到平衡狀態,A中NH3的體積分數為a,放出熱量Q1kJ,而恒壓密閉容器B,均充入1mol N2和3molH2,反應發生后總物質的量減少,由pV=nRT可知,相對于A來說,相當于B加壓,則平衡正向移動,氨氣的體積分數變大,所以a<b,B中放出的熱量對,則Q1<Q2,熱化學方程式中反應熱為完全反應放出的熱量,而A中不能完全轉化,放出的熱量少,則Q1<92.4。
考點:化學平衡的計算;化學平衡常數的含義;化學反應速率的影響因素;化學平衡狀態的判斷;體積百分含量隨溫度、壓強變化曲線;轉化率隨溫度、壓強的變化曲線。


科目:高中化學 來源: 題型:填空題
高爐煉鐵過程中發生的主要反應為1/3Fe2O3(s) + CO(g) 2/3Fe(s) + CO2(g)
2/3Fe(s) + CO2(g)
已知該反應在不同溫度下的平衡常數如下:
請回答下列問題:
(1)該反應的平衡常數表達式K=_____________,△H________0(填“>”、“<”或“=”);
(2)在一個容積為10L的密閉容器中,1000℃時加入Fe、Fe2O3、CO、CO2各1.0 mol,反應經過l0 min達到平衡。求該時間范圍內反應的平均反應速率υ(CO2)=" _________" 、CO的平衡轉化率= _____________:
(3)欲提高(2)中CO的平衡轉化率,可采取的措施是_____________。
| A.減少Fe的量 |
| B.增加Fe203的量 |
| C.移出部分CO2 |
| D.提高反應溫度 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某些金屬及金屬氧化物對H2O2的分解反應具有催化作用,請回答下列問題: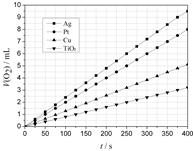
(1)已知:2H2O2(aq) =" 2" H2O (l) + O2(g) 的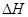 < 0, 則該反應的逆反應能否自發進行? (填“能”或“不能”),判斷依據是 。
< 0, 則該反應的逆反應能否自發進行? (填“能”或“不能”),判斷依據是 。
(2)某同學選用Ag、Pt、Cu、TiO2作為催化劑,在25℃ 時,保持其它實驗條件相同,測得生成的O2體積(V)。V與分解時間(t)的關系如圖所示(O2的體積已折算成標準狀況),則:在不同催化劑存在下,H2O2分解反應的活化能大小順序是 Ea( ) > Ea( ) > Ea( ) > Ea( ) (括號內填寫催化劑的化學式)金屬Pt 催化下,H2O2分解的反應速率v(O2) = mol·s-1
(3)為研究溫度對H2O2分解速率的影響(不加催化劑),可將一定濃度和體積的H2O2置于密閉容器中,在某溫度下,經過一定的時間t,測定生成O2的體積V。然后保持其它初始條件不變,改變溫度T,重復上述實驗。獲得V(O2) ~ T關系曲線。下列趨勢圖最可能符合實測V(O2) ~ T關系曲線的是 ,原因是 。
| A. | B. | C. | D. (4)以Pt為電極電解H2O2也可產生氧氣,寫出H2O2水溶液電解過程中的電極反應式(已知:H2O2的氧化性及還原性均比H2O強):陰極;陽極 。 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
碘及其化合物在人類活動中占有重要地位。
(1)加碘食鹽中含有碘酸鉀(KIO3),工業上以電解法制備碘酸鉀,電解設備如圖所示。先將一定量的碘溶于過量氫氧化鉀溶液,發生反應: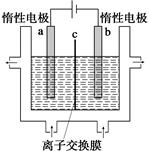
3I2+6KOH=5KI+KIO3+3H2O,再將該溶液加入 (陰極、陽極)區,另將氫氧化鉀溶液加入另外一個區。使用 (陰、陽)離子交換膜,在陽極發生的電極反應式: 。
(2)碘化氫不穩定,分解反應的熱化學方程式是2HI(g)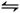 I2(g)+H2(g) ΔH="+9.48" kJ·mol-1已知ΔS>0
I2(g)+H2(g) ΔH="+9.48" kJ·mol-1已知ΔS>0
①該反應屬于( )
A.任何溫度均自發 B.任何溫度均不自發 C.高溫自發 D.低溫自發
②一定條件下,反應在一個帶有活塞的密閉容器中達到平衡,下列說法中不正確的是( )
A.恒溫,縮小體積,平衡常數不變
B.恒溫,縮小體積,平衡不移動,顏色加深
C.恒容,升溫,正向反應速率和逆向反應速率均增大
D.恒容,在容器中若投入2mol HI,達到平衡時吸收9.48 kJ 的熱量
③一定溫度下,平衡常數K=1/4,在2L的容器中,加入4molHI發生反應達到平衡,HI的轉化率 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在某密閉容器內有正反應為放熱的可逆反應,其中A、B為氣體,C為固體,若反應開始經 s后達平衡。如圖:
s后達平衡。如圖:
(1)該反應的化學方程式為_________________________
(2)反應物的轉化率______________________
(3)要使反應物的轉化率增加可能的原因是____________
A.增大了B或C的濃度 B.使用了催化劑
C.縮小體積,使體系壓強增大 D.升高了反應溫度
(4)該反應達到平衡后,向該容器中再充入0.5mol的He。若恒溫恒壓,,這時反應速率 _________(填“加快”、“減慢”或“不變”),平衡_____________ (填“向正方向移動”、“向逆方向移動”、“不移動”);若恒溫恒容時,這時反應速率_______(填“加快”、“減慢”或“不變”),反應物的轉化率___________(填“加快”、“減慢”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
反應m A+n B p C在某溫度下達到平衡
p C在某溫度下達到平衡
①若A、B、C都是氣體,減壓后正反應速率小于逆反應速率,則m、n、p的關系是 。②若C為氣體,且m + n = p,在加壓時化學平衡發生移動,則平衡必定向______方向移動。
③如果在體系中增加或減少B的量,平衡均不發生移動,則B肯定不能為______態。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一容積為2 L的密閉容器中,加入0.2 mol的N2和0.6 mol的H2,在一定條件下發生反應:N2(g)+3H2(g)  2NH3(g) ΔH<0 。反應中NH3的物質的量濃度的變化情況如下圖所示,請回答下列問題:
2NH3(g) ΔH<0 。反應中NH3的物質的量濃度的變化情況如下圖所示,請回答下列問題:
(1)根據上圖,計算從反應開始到平衡時,氫氣的平均反應速率v(H2)為______________。
(2)該反應達到平衡時N2的轉化率_________________。
(3)反應達到平衡后,第5分鐘末,保持其它條件不變,若改變反應溫度,則NH3的物質的量濃度不可能為____________。(填序號)
a.0.20 mol·L-1 b.0.12 mol·L-1 c.0.10 mol·L-1 d.0.08 mol·L-1
(4)請寫出該反應的平衡常數表達式_________,若該反應在298K、398K時的化學平衡常數分別為K1、K2,則K1 K2(填“>”、“="”" 或 “<” )。
(5)在第5分鐘末將容器的體積縮小一半后,若在第8分鐘末達到新的平衡(此時NH3的濃度約為0.25 mol·L-1),請在上圖中畫出第5分鐘末到此平衡時NH3濃度的變化曲線。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一固定容積為2L的密閉容器內加入0.2 mol的N2和0.6 mol的H2,在一定條件下發生如下反應:N2(g)+3H2(g) 2NH3(g)+Q(Q>0),
2NH3(g)+Q(Q>0),
(1)該反應所用的催化劑是 (填寫名稱)
該反應450℃的平衡常數 500℃時的平衡常數(填“>”、“<”或“=”)。
(2)下列描述中能說明上述反應已達平衡的是
| A.3V正(H2)=2V逆(NH3) | B.容器中氣體的平均分子量不隨時間而變化 |
| C.容器中氣體的密度不隨時間而變化 | D.容器中氣體的分子總數不隨時間而變化 |
| | A | B | C | D |
| 研究目的 | 壓強對反應的影響(P1>P2) | 溫度對反應的影響 | 平衡體系增加N2對反應的影響 | 催化劑對反應的影響 |
| 圖示 |  |  |  |  |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)將一定量純凈的氨基甲酸銨置于密閉真空容器中(假設容器體積不變,固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡:
H2NCOONH4(s) 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
實驗測得不同溫度下的平衡數據列于下表:
| 溫度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡氣體總濃度(×10—3 mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com