
�⼰�仯����������(d��ng)��ռ����Ҫ��λ��
(1)�ӵ�ʳ�}�к��е����(KIO3)�����I(y��)����늽ⷨ�Ƃ����⛣�늽��O(sh��)����D��ʾ���Ȍ�һ�����ĵ������^(gu��)�����������Һ���l(f��)������(y��ng)��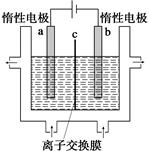
3I2��6KOH=5KI��KIO3��3H2O���ٌ�ԓ��Һ���� (ꎘO���(y��ng)�O)�^(q��)���팢���������Һ��������һ��(g��)�^(q��)��ʹ�� (ꎡ��(y��ng))�x�ӽ��QĤ�����(y��ng)�O�l(f��)����늘O����(y��ng)ʽ�� ��
(2)�⻯�䲻��(w��n)�����ֽⷴ��(y��ng)�ğữ�W(xu��)����ʽ��2HI(g)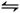 I2(g)+H2(g) ��H="+9.48" kJ��mol��1��֪��S��0
I2(g)+H2(g) ��H="+9.48" kJ��mol��1��֪��S��0
��ԓ����(y��ng)����( )
A���κΜضȾ��l(f��) B���κΜضȾ����l(f��) C���ߜ��l(f��) D���͜��l(f��)
��һ���l���£�����(y��ng)��һ��(g��)���л��������]�������_(d��)��ƽ�⣬�����f(shu��)���в����_����( )
A����أ��sС�w�e��ƽ�ⳣ��(sh��)��׃
B����أ��sС�w�e��ƽ�ⲻ�Ƅ�(d��ng)���ɫ����
C�����ݣ����أ�����(y��ng)���ʺ�����(y��ng)���ʾ�����
D�����ݣ�����������Ͷ��2mol HI���_(d��)��ƽ��r(sh��)����9.48 kJ �ğ���
��һ���ض��£�ƽ�ⳣ��(sh��)K=1/4����2L�������У�����4molHI�l(f��)������(y��ng)�_(d��)��ƽ�⣬HI���D(zhu��n)���� ��
��1���(y��ng)�O � I-+6OH-��6e-=IO3-+3H2O ��2����C��D ��0.5
����ԇ�}��������1�����}��֪늽ⷨ�Ƃ����⛵�ԭ�����KOH���ڵėl��늽�KI��KIO3�Ļ��Һ������(y��ng)�Č�(sh��)�|(zh��)�ǵ��x�Ӱl(f��)��ʧ��ӵ���������(y��ng)����K���ɵ�����x�ӣ��Y(ji��)��늽�ԭ��늽�ص��(y��ng)�O�l(f��)��ʧ��ӵ���������(y��ng)������KI��KIO3�Ļ��Һ��(y��ng)�����c�Դ���O���B���(y��ng)�O�^(q��)�����b���е�a�O�^(q��)������(j��)늘O����ʽ����ԭ�tԭ���غ��늺��غ㣬늘O����(y��ng)ʽ�飺I-+6OH-��6e-=IO3-+3H2O��ԓ�O�^(q��)����(y��ng)����OH������(y��ng)�м���ꎘO�^(q��)��KOH��Һ�a(b��)�䣬�x�ӽ��QĤ��(y��ng)���S��x��ͨ�^(gu��)������x�ӽ��QĤ��
��2����ԓ����(y��ng)��H��0����S��0������(j��)����(y��ng)������Г�(j��)��֪�ߜؕr(sh��)��H��T��S<0�����l(f��)�M(j��n)�У��xC.
��A��ƽ�ⳣ��(sh��)��Ӱ����؞�ضȣ����_��B��ԓ����(y��ng)��߅���w���|(zh��)ϵ��(sh��)��ȣ���أ��sС�w�e��ƽ�ⲻ�Ƅ�(d��ng)���������|(zh��)�ĝ�������ɫ������_��C�����ط���(y��ng)���ʼӿ죬���_��D�����淴��(y��ng)�����c(di��n)�Dz����M(j��n)�е��ף�Ͷ��2mol HI���_(d��)��ƽ��r(sh��)���յğ���С��9.48 kJ���e(cu��)�`��
�� �O(sh��)�D(zhu��n)���ĵ⻯���x���������η��ó������|(zh��)��ƽ���ȣ�����ƽ�ⳣ��(sh��)���_(d��)ʽ����⻯���ƽ���ȣ������D(zhu��n)����Ӌ(j��)�㹫ʽӋ(j��)��ɵá�
���c(di��n)������늽�ԭ�������淴��(y��ng)�����c(di��n)�����l����(du��)����ƽ���Ӱ푼�ƽ��Ӌ(j��)��


 ��У�n��ϵ�д�
��У�n��ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
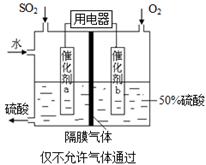
���ô���������(y��ng)��SO2�D(zhu��n)����SO3�ǹ��I(y��)�����a(ch��n)������P(gu��n)�I���E��
��֪��SO2��g���� O2��g��
O2��g�� SO3��g�� ��H����98 kJ��mol��1��
SO3��g�� ��H����98 kJ��mol��1��
��1��ij�ض���ԓ����(y��ng)��ƽ�ⳣ��(sh��)K��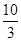 �����ڴ˜ض��£���100 L�ĺ������]�����У�����3.0 mol SO2(g)��16.0 mol O2(g)��3.0 mol SO3(g)���t����(y��ng)�_ʼ�r(sh��)v������ v���棩�����������������������
�����ڴ˜ض��£���100 L�ĺ������]�����У�����3.0 mol SO2(g)��16.0 mol O2(g)��3.0 mol SO3(g)���t����(y��ng)�_ʼ�r(sh��)v������ v���棩�����������������������
��2��һ���ض��£���һ���������w�e��2 L�����]�����г���2.0 mol SO2��1.0 molO2���_(d��)��ƽ����w�e׃?y��u)?.6 L���tSO2��ƽ���D(zhu��n)���ʞ� ��
��3���ڣ�2���еķ���(y��ng)�_(d��)��ƽ���׃���Зl������ʹSO2(g)ƽ���ȱ�ԭ��(l��i)�pС���� ������ĸ����
| A�����֜ضȺ������w�e��׃������1.0 mol O2 |
| B�����֜ضȺ�������(n��i)����(qi��ng)��׃������1.0 mol SO3 |
| C�����͜ض� |
| D���Ƅ�(d��ng)�������s���w |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
KI��Һ�����ԗl�������c���ⷴ��(y��ng)���F(xi��n)������(sh��)�(y��n)ӛ䛣�
| ��(sh��)�(y��n)��̖(h��o) | �� | �� | �� | �� | �� |
| �ضȣ��棩 | 30 | 40 | 50 | 60 | 70 |
| �@ɫ�r(sh��)�g��s�� | 160 | 80 | 40 | 20 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
���������a(ch��n)���ʡ����ᡢ���A�ȵ���Ҫԭ�ϡ�
��1����(sh��)�(y��n)��ģ�M�ϳɰ����ں�غ������]�����а��ռס��ҡ������N��ʽ�քeͶ�ϣ���λ��mol /L����ƽ��r(sh��)�y(c��)�ü�������H2���D(zhu��n)���ʞ�20%��
| | N2 | H2 | NH3 |
| �� | 1 | 3 | 0 |
| �� | 0.5 | 1.5 | 1 |
| �� | 0 | 0 | 4 |
 CO(NH2)2 (l) + H2O (l)��ԓ����(y��ng)��ƽ�ⳣ��(sh��)�͜ض��P(gu��n)ϵ���£�
CO(NH2)2 (l) + H2O (l)��ԓ����(y��ng)��ƽ�ⳣ��(sh��)�͜ض��P(gu��n)ϵ���£�| T / �� | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
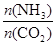 ��x���D�ǰ�̼�ȣ�x���cCO2ƽ���D(zhu��n)���ʣ��������P(gu��n)ϵ�����S��x����������ԭ���� ��
��x���D�ǰ�̼�ȣ�x���cCO2ƽ���D(zhu��n)���ʣ��������P(gu��n)ϵ�����S��x����������ԭ���� ��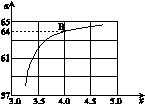
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
����(y��ng)aA��g��+bB��g�� cC��g������H��0���ڵ��ݗl�����M(j��n)�С���׃��������(y��ng)�l�����ڢ��A���wϵ�и����|(zh��)����S�r(sh��)�g׃�����������D��ʾ��
cC��g������H��0���ڵ��ݗl�����M(j��n)�С���׃��������(y��ng)�l�����ڢ��A���wϵ�и����|(zh��)����S�r(sh��)�g׃�����������D��ʾ�� 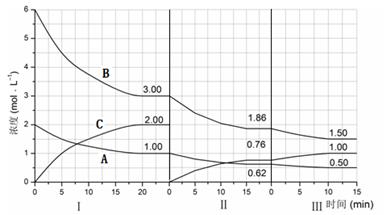
�ش���(w��n)�}��
��1������(y��ng)�Ļ��W(xu��)����ʽ�У�a��b��c�� ��
��2��B��ƽ���D(zhu��n)���ʦ�����B����������B����������B���������� ����ֵ�� ��
��3���ɵ�һ��ƽ��ڶ���ƽ�⣬ƽ���Ƅ�(d��ng)�ķ����� ����ȡ�Ĵ�ʩ�� ��
��4�����^�ڢ��A�η���(y��ng)�ضȣ�T2���͵ڢ��A�η���(y��ng)�ضȣ�T3���ĸߵͣ�T2 T3 ���<������>��=�������Д�������� ��
��5���_(d��)��������ƽ����������w�e�U(ku��)��һ�����ٶ�10min���_(d��)���µ�ƽ�⣬Ո(q��ng)?ji��n)��D����������ʾ��IV�A���wϵ��B���|(zh��)�ĝ���S�r(sh��)�g׃����څ��(sh��)��ע��ֻ횮���B�ĝ���S�r(sh��)�g׃����������
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
��һ���l���£����淴��(y��ng)A2(g)+B2(g)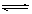 2C(g)��һ��(g��)���]�������_(d��)��ƽ��r(sh��),�y(c��)��c(A2)=0��5mol��L-1��c(B2)=0��1mol��L-1��c(C)=1��6mol��L-1����
2C(g)��һ��(g��)���]�������_(d��)��ƽ��r(sh��),�y(c��)��c(A2)=0��5mol��L-1��c(B2)=0��1mol��L-1��c(C)=1��6mol��L-1���� ��
�� ��C����ʼ��ȷքe��a mol��L-1��b mol��L-1��g mol��L-1Ո(q��ng)�_����
��C����ʼ��ȷքe��a mol��L-1��b mol��L-1��g mol��L-1Ո(q��ng)�_����
(l)a��g��(y��ng)�M����P(gu��n)ϵʽ��_____________��
(2)������(y��ng)��������(y��ng)�����_ʼ�M(j��n)�У���(d��ng)g=_________,a�����ֵ��__________��
(3)������(y��ng)���淴��(y��ng)�����_ʼ�M(j��n)�У���(d��ng)b=_________��a����Сֵ��_________��
(4)b��ȡֵ������___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
�ϳɰ����I(y��)��(du��)��(gu��)��(j��ng)��(j��)�����(hu��)�l(f��)չ������Ҫ�����x����ԭ��飺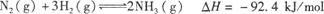 ����(j��)�˻ش�����(w��n)�}��
����(j��)�˻ش�����(w��n)�}��
��1����ԓ����(y��ng)�Ļ��W(xu��)ƽ�ⳣ��(sh��)���_(d��)ʽ��K= ��
�ڸ���(j��)�ضȌ�(du��)���W(xu��)ƽ���Ӱ�Ҏ(gu��)�ɿ�֪����(du��)��ԓ����(y��ng)���ض�Խ�ߣ���ƽ�ⳣ��(sh��)��ֵԽ ��
��2��ij�ض��£�����10 mol N2�c30 mol H2�����w�e��10 L�����]������(n��i)������(y��ng)�_(d��)��ƽ���B(t��i)�r(sh��)���y(c��)�û�Ϛ��w�а����w�e��?j��n)?sh��)��20�����tԓ�ض��·���(y��ng)��K= (���÷�?j��n)?sh��)��ʾ)��
���f(shu��)��ԓ����(y��ng)�_(d��)�����W(xu��)ƽ���B(t��i)���� (����ĸ)��
a��������(n��i)���ܶȱ��ֲ�׃ b��������(n��i)����(qi��ng)���ֲ�׃
c��v��(N2)=2v��(NH3) d����Ϛ��w��c(NH3)��׃
��3����(du��)�ںϳɰ�����(y��ng)���ԣ��������P(gu��n)�D��һ�����_����(�x����̖(h��o)) ��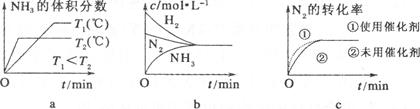
��4����ͬ�ض��£��к������]����A�ͺ㉺���]����B���������о�����1 mol N2��3 mol H2���˕r(sh��)���������w�e��ȡ���һ���l���·���(y��ng)�_(d��)��ƽ���B(t��i)��A��NH3���w�e��?j��n)?sh��)��a���ų�����Q1kJ��B��NH3���w�e��?j��n)?sh��)��b���ų�����Q2kJ���t��a b(���������������=������ͬ)��Q1 Q2��Q1 92��4��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
(14��)ij���W(xu��)����(y��ng)2A(g) B(g)+D(g)���ķN��ͬ�l�����M(j��n)�У�B��D��ʼ��Ȟ��㣬����(y��ng)��A�ĝ��(mol/L)�S����(y��ng)�r(sh��)�g(min)��׃����r������(j��)������(sh��)��(j��)�����������գ�
B(g)+D(g)���ķN��ͬ�l�����M(j��n)�У�B��D��ʼ��Ȟ��㣬����(y��ng)��A�ĝ��(mol/L)�S����(y��ng)�r(sh��)�g(min)��׃����r������(j��)������(sh��)��(j��)�����������գ�
| ��(sh��)�(y��n) ��̖(h��o) | �ض�/�� | �r(sh��)�g/min | ||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| 1 | 800�� | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800�� | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800�� | c 3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820�� | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
(14��)���I(y��)���������Ҫ����(y��ng)��4NH3(g)+5O2(g)  4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
(1)�����4molNH3��5molO2���������У��_(d��)��ƽ��r(sh��)���ų�����0.8akJ���t����(y��ng)�r(sh��)�D(zhu��n)�Ƶ���Ӕ�(sh��)��
mol
(2)�������l����׃�������P(gu��n)ϵ�D���e(cu��)�`���� ���x����̖(h��o)��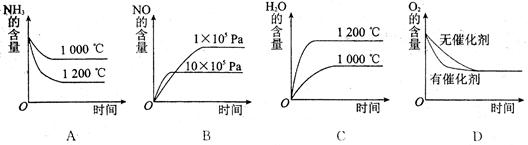
(3)t��r(sh��)�����ݷe�̶������]�����аl(f��)����������(y��ng)��������(n��i)�����|(zh��)�ĝ�����±�
| ���(mol/L) �r(sh��)�g(min) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| �� ʼ | 4.0 | 5.5 | 0 | 0 |
| ��2min | 3.2 | x | 0.8 | 1.2 |
| ��4min | 2.0 | 3.0 | 2.0 | 3.0 |
| ��6min | 2.0 | 3.0 | 2.0 | 3.0 |
�鿴�𰸺ͽ���>>
��(gu��)�H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com