
氮可以形成多種化合物,如NH3、N2H4、HCN、NH4NO3等。
(1)已知:N2(g)+2H2(g)=N2H4(l) △H=" +" 50.6kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H="-571.6" kJ·mol-1
則①N2H4(l)+O2(g)=N2(g)+2H2O(l) △H= kJ·mol-1
②N2(g)+2H2(g)=N2H4(l) 不能自發進行的原因是 。
③用次氯酸鈉氧化氨,可以得到N2H4的稀溶液,該反應的化學方程式是 。
(2)采礦廢液中的CN-可用H2O2處理。已知:H2SO4=H++ HSO4- HSO4-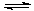 H++ SO42-
H++ SO42-
用鉑電極電解硫酸氫鉀溶液,在陽極上生成S2O82-,S2O82-水解可以得到H2O2。寫出陽極上的電極反應式 。
(3)氧化鎂處理含NH4+的廢水會發生如下反應:
MgO+H2O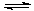 Mg(OH)2 Mg(OH)2+2NH4+
Mg(OH)2 Mg(OH)2+2NH4+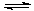 Mg2+ +2NH3·H2O。
Mg2+ +2NH3·H2O。
①溫度對氮處理率的影響如圖所示。在25℃前,升高溫度氮去除率增大的原因是 。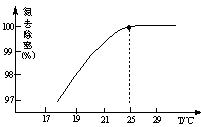
②剩余的氧化鎂,不會對廢水形成二次污染,理由是 。
(4)滴定法測廢水中的氨氮含量(氨氮以游離氨或銨鹽形式存在于水中)步驟如下:①取10 mL廢水水樣于蒸餾燒瓶中,再加蒸餾水至總體積為175 mL②先將水樣調至中性,再加入氧化鎂使水樣呈微堿性,加熱③用25 mL硼酸吸收蒸餾出的氨[2NH3+4H3BO3=(NH4)2B4O7+5H2O]④將吸收液移至錐形瓶中,加入2滴指示劑,用c mol·L-1的硫酸滴定至終點[(NH4)2B4O7+H2SO4+5H2O=(NH4)2SO4+4H3BO3],記錄消耗的體積V mL。則水樣中氮的含量是 mg·L-1(用含c、V的表達式表示)。
(1)①-622.2 ②△H>0 △S<0 ③NaClO+2NH3=N2H4+NaCl+H2O
(2)2HSO4--2e-= S2O82-+2H+
(3)①升高溫度NH3的溶解度降低,有利于NH3的逸出
②氧化鎂難溶于水中,以沉淀的形式排出,因此不會形成二次污染
(4)2800cV
解析試題分析: (1)①根據蓋斯定律求?H。
②根據題目所給熱化學方程式,可知△H>0,由氣體生成液體可知△S<0。
③NaClO被還原為NaCl,根據元素守恒可推出還生成H2O,進而寫出化學方程式。
(2)生成S2O82-,可推出HSO4?失電子,根據化合價的變化配平,寫出電極方程式。
(3)①氣體的溶解度隨溫度的升高而減小。
②溶解到廢液中才會造成污染,MgO難溶。
(4)根據題目所給信息和元素守恒可知:氮元素與硫酸的對應關系為2N~H2SO4,由H2SO4的體積和濃度可算出氮的含量為:0.001VCmol×2×14000mg/mol÷0.01L=2800VCmg/L。
考點:反應熱、電化學、化學計算


科目:高中化學 來源: 題型:填空題
蓋斯定律在生產和科學研究中有很重要的意義。有些反應的反應熱雖然無法直接測得,但可通過間接的方法測定。現根據下列3個熱化學反應方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=―24.8kJ?mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=―47.2kJ?mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ?mol-1
寫出CO氣體還原FeO固體得到Fe固體和CO2氣體的熱化學反應方程式:__________________________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)已知:2NO2(g) N2O4(g);△H<0。在恒溫恒容條件下,將一定量NO2和N2O4的混合氣體通入容積為2L的密閉容器中,反應過程中各物質的物質的量濃度c隨時間t的變化關系如下圖所示。
N2O4(g);△H<0。在恒溫恒容條件下,將一定量NO2和N2O4的混合氣體通入容積為2L的密閉容器中,反應過程中各物質的物質的量濃度c隨時間t的變化關系如下圖所示。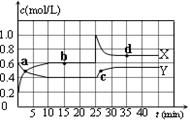
①a、b、c、d四個點中,表示化學反應處于平衡狀態的點是 。
②前10 min內用NO2表示的化學反應速率v(NO2)= mol·L-1·min-1。反應在第一個平衡點的平衡常數K(1)= (可用分數表示)。反應在第二個平衡點的平衡常數K(2)與第一個平衡點的平衡常數K(1)的關系:K(2) K(1)(填“>”、“=”或“<”)。
③請在右圖坐標中畫出1 mol N2O4通入2L的密閉容器中反應發生過程中的能量變化示意圖,并在虛線上分別標出反應物和生成物的化學式。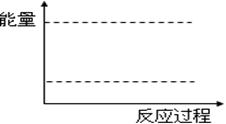
(2)右圖中a、b、c、d分別代表氧族元素(ⅥA族):Te(碲)、Se(硒)、S、O氫化物的反應熱的數據示意圖。試回答下列問題: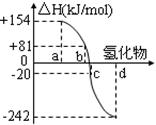
①請你歸納:非金屬元素氫化物的穩定性與形成氫化物的反應熱△H的關系 。
②寫出硒化氫發生分解反應的熱化學反應方程式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
SO2和NOx在化學工業上有重要用途,也是大氣污染的主要來源,開發和利用并重,預防和治理并舉是當前工業上和環境保護領域研究的主要課題之一。
(1)在接觸法制硫酸的過程中,發生2SO2(g)+O2(g)  2SO3(g) △H<0反應,某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖所示,根據圖示回答下列問題:
2SO3(g) △H<0反應,某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖所示,根據圖示回答下列問題:
①平衡狀態由A到B時,平衡常數K(A) K(B)(填“>”、“<”或“=”);
②將2.0molSO2和1.0molO2置于10L的密閉容器中,若40s后反應達到平衡,此時體系總壓強為0.10MPa,這一段時間內SO2的平均反應速率為 。
該反應的平衡常數為 。
(2)用CH4催化還原NOx可消除氮的氧化物的污染,例如:
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=—574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=—1160kJ·mol—1
取標準狀況下4.48LCH4并使之完全反應:
①若將NO2還原至N2,整個過程中轉移電子的物質的量為 ;
②若還原NO2和NO的混合物,放出的總熱量Q的取值范圍是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知反應:3I-(aq)+S2O82-(aq)  I3-(aq)+2SO42-(aq)+Q
I3-(aq)+2SO42-(aq)+Q
(1)寫出反應的平衡常數表達式:K= 。
(2)如圖表示反應過程中有關物質的能量,則反應過程中的Q 0(填>、<、=);(I)、(II)兩曲線中,使用催化劑的是 曲線。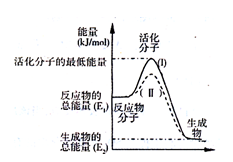
(3)反應的速率可以用I3-與加入的淀粉溶液反應顯藍色的時間t來度量,t越小,反應速率越大。下表是在20℃進行實驗時所記錄的數據
| 實驗編號 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-)/mol·L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
研究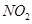 、
、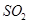 、CO等大氣污染氣體的測量及處理具有重要意義。
、CO等大氣污染氣體的測量及處理具有重要意義。
(1) 可使
可使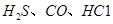 等氧化,常用于定量測定CO的含量。已知:
等氧化,常用于定量測定CO的含量。已知: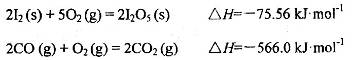
寫出CO(g)與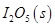 反應生成
反應生成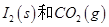 的熱化學方程式:________________。
的熱化學方程式:________________。
(2)CO可制做燃料電池,以KOH溶液作電解質,向兩極分別充入CO和空氣,工作過程中,K+移向_______極(填“正”或“負”),正極反應方程式為:___________________。
(3)新型氨法煙氣脫硫技術的化學原理是采用氨水吸收煙氣中的SO2,再用一定量的磷
酸與上述吸收產物反應。該技術的優點除了能回收利用SO2外,還能得到一種復合肥料。
①該復合肥料可能的化學式為___________(寫出一種即可)。
②若氨水與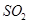 恰好完全反應生成正鹽,則此時溶液呈________性(填“酸”或“堿”)。
恰好完全反應生成正鹽,則此時溶液呈________性(填“酸”或“堿”)。
常溫下弱電解質的電離平衡常數如下:氨水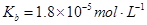

③向②中溶液中通入________氣體可使溶液呈中性。(填“SO2”或NH3”)
此時溶液中 ________2(填“>”“<”或“=”)
________2(填“>”“<”或“=”)
(4)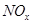 可用強堿溶液吸產生硝酸鹽。在酸性條件下,FeSO4溶液能將
可用強堿溶液吸產生硝酸鹽。在酸性條件下,FeSO4溶液能將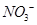 還原為NO,寫出該過程中產生NO反應的離子方程式___________________________________。
還原為NO,寫出該過程中產生NO反應的離子方程式___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
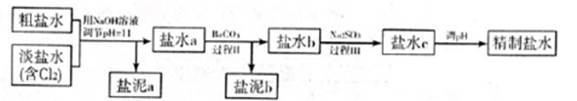
利用海水資源進行化工生產的部分工藝流程如圖: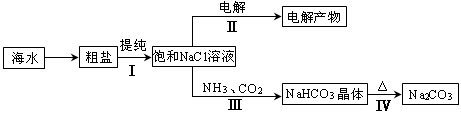
(1)流程I中,欲除去粗鹽中含有的Ca2+、Mg2+、SO42-等離子,需將粗鹽溶解后,按序加入藥品進行沉淀、過濾等。加入藥品和操作的順序可以是 。
a.Na2CO3、NaOH、BaCl2、過濾、鹽酸 b.NaOH、BaCl2、Na2CO3、過濾、鹽酸
c.NaOH、Na2CO3、BaCl2、過濾、鹽酸 d.BaCl2、Na2CO3、NaOH、過濾、鹽酸
(2)流程II中,電解飽和NaCl溶液的離子方程式為 。通電開始后,陽極區產生的氣體是 ,陰極附近溶液pH會 (填“增大”、“減小”或“不變”)。
(3)流程III中,通過反應得到NaHCO3晶體。下圖為NaCl、NH4Cl、NaHCO3、NH4HCO3的溶解度曲線,其中能表示NaHCO3溶解度曲線的是 ,化學反應方程式是 。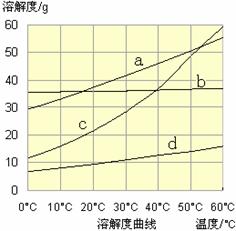
(4)流程IV中,所得純堿常含有少量可溶性雜質,提純它的過程如下:將碳酸鈉樣品加適量水溶解、 、 、過濾、洗滌2-3次,得到純凈Na2CO3?10H2O,Na2CO3?10H2O脫水得到無水碳酸鈉,已知:
Na2CO3·H2O(s)==Na2CO3(s)+H2O(g) ΔH1=+58.73kJ·mol-1
Na2CO3·10H2O(s)==Na2CO3·H2O(s)+9H2O(g) ΔH2=" +473.63" kJ·mol-1
把該過程產生的氣態水完全液化釋放的熱能全部用于生產Na2CO3所需的能耗(不考慮能量損失),若生產1molNa2CO3需要耗能92.36kJ,由此得出:H2O(g)==H2O(l) △H = 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氫氣的制取與儲存是氫能源利用領域的研究熱點。
(1)已知: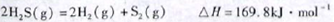
下列有關該反應的敘述正確的是
| A.正反應活化能小于169.8kJ·mol-1 |
| B.逆反應活化能一定小于169.8kJ·mol-1 |
| C.正反應活化能不小于169.8kJ·mol-1 |
| D.正反應活化能比逆反應活化能小169.8kJ·mol-1 |
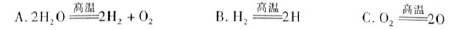
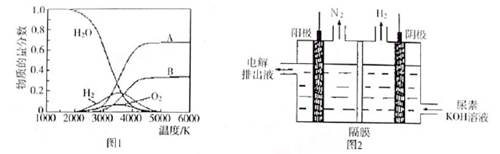
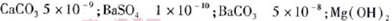
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
多晶硅是太陽能光伏產業的重要原料。
(1)由石英砂可制取粗硅,其相關反應的熱化學方程式如下: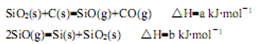
①反應SiO2(s)+2C(s)=Si(s)+2CO(g)的△H= kJ·mol-1(用含a、b的代數式表示)。
②SiO是反應過程中的中間產物。隔絕空氣時,SiO與NaOH溶液反應(產物之一是硅酸鈉)的化學方程式是 。
(2)粗硅提純常見方法之一是先將粗硅與HCl制得SiHCl3,經提純后再用H2還原:SiHCl3(g)+H2(g) Si(s)+3HCl(g)不同溫度及不同n(H2)/n(SiHCl3)時,反應物X的平衡轉化率關系如圖;
Si(s)+3HCl(g)不同溫度及不同n(H2)/n(SiHCl3)時,反應物X的平衡轉化率關系如圖;
①X是 (填“H2”、“SiHCl3”)。
②上述反應的平衡常數K(1150℃) K(950℃)(選填“>”、“<”、“=”)
(3)SiH4(硅烷)法生產高純多晶硅是非常優異的方法。
①用粗硅作原料,熔鹽電解法制取硅烷原理如圖10,電解時陽極的電極反應式為 。
②硅基太陽電池需用N、Si兩種元素組成的化合物Y作鈍化材料,它可由SiH4與NH3混合氣體進行氣相沉積得到,已知Y中Si的質量分數為60%,Y的化學式為 。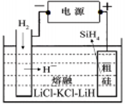
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com