
已知:Cu(OH)2是二元弱堿;亞磷酸(H3PO3)是二元弱酸,與NaOH溶液反應,生成Na2HPO3。
(1)在銅鹽溶液中Cu2+發生水解反應的離子方程式為____,該反應的平衡常數為____;(已知:25℃時,Ksp[Cu(OH)2]=2.0×10-20mol3/L3)
(2)根據H3PO3的性質可推測Na2HPO3稀溶液的pH______7(填“>”“<”或“=”)。常溫下,向10mL0.01mol/L H3PO3溶液中滴加10ml0.02mol/LNaOH溶液后,溶液中各種離子濃度由大到小的順序是_________;
(3)電解Na2HPO3溶液可得到亞磷酸,裝置如圖(說明:陽膜只允許陽離子通過,陰膜只允許陰離子通過)
①陽極的電極反應式為____________________。
②產品室中反應的離子方程式為____________。
(13分)(1)Cu2++2H2O Cu(OH)2+2H+(2分);5×10-9(2分)
Cu(OH)2+2H+(2分);5×10-9(2分)
(2)>(2分);c(Na+)>c(HPO32-)>c(OH-)>c(H2PO3-)>c(H+)(2分)
(3)①4OH――4e-=2H2O+O2↑(2分)
②HPO32-+2H+=H3PO3(2分)或HPO32-+H+=H2PO3-、H2PO3-+H+=H3PO3(各1分)
解析試題分析:(1)氫氧化銅是弱堿,所以銅離子可以水解,溶液顯酸性,其水解反應的離子方程式為Cu2++2H2O Cu(OH)2+2H+。化學平衡常數是在一定條件下,當可逆反應達到平衡狀態時,生成物濃度的冪之積和反應物濃度的冪之積的比值,所以該反應的平衡常數K=
Cu(OH)2+2H+。化學平衡常數是在一定條件下,當可逆反應達到平衡狀態時,生成物濃度的冪之積和反應物濃度的冪之積的比值,所以該反應的平衡常數K= =
=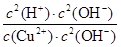 =
=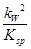 =
=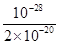 =5×10-9。
=5×10-9。
(2)H3PO3是弱酸,Na2HPO3是強堿弱酸鹽,所以HPO32-水解,其水溶液呈堿性,即pH>7;向10mL0.01mol/LH3PO3溶液中滴加10ml 0.02mol/LNaOH溶液后,二者恰好反應生成Na2HPO3,溶液水解顯堿性,所以溶液中離子濃度大小為c(Na+)>c(HPO32-)>c(OH-)>c(H2PO3-)>c(H+)。
(3)①電解池陽極失去電子,發生氧化反應,陰極得到電子發生還原反應。所以根據裝置圖可知,陽極上氫氧根離子失電子發生氧化反應,電極反應式為4OH――4e-=2H2O+O2↑。
②由于陽膜只允許陽離子通過,陰膜只允許陰離子通過,所以產品室中HPO32-和氫離子結合生成亞磷酸,反應離子方程式為HPO32-+2H+=H3PO3,或HPO32-+H+=H2PO3-、H2PO3-+H+=H3PO3。
考點:考查水解方程式、平衡常數計算;酸堿中和溶液中離子濃度大小比較;電解原理的應用以及電極反應式的書寫等


 同步練習強化拓展系列答案
同步練習強化拓展系列答案科目:高中化學 來源: 題型:填空題
(1)水的電離平衡曲線如圖所示,若A點表示25℃時水的電離達平衡時的離子濃度,B點表示100℃時水的電離達平衡時的離子濃度。則100℃時1 mol·L-1的NaOH溶液中,由水電離出的c(H+)=___________mol·L-1。25 ℃時,向水的電離平衡體系中加入少量NH4Cl固體,對水的電離平衡的影響是________(填“促進”、“抑制”或“不影響”)。
(2)電離平衡常數是衡量弱電解質電離程度強弱的量。已知如表數據。
| 化學式 | 電離平衡常數(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫酸是強酸,中學階段將硫酸在水溶液中看作完全電離。但事實是,硫酸在水中的第一步電離是完全的,第二步電離并不完全,其電離情況為:H2SO4=H++HSO4-,HSO4- H+ + S042-。
H+ + S042-。
請回答下列有關問題:
(1)Na2SO4溶液呈_(填“弱酸性”、“中性”或“弱堿性”),其理由是_
(用離子方程式表示)。
(2)H2SO4溶液與BaC12溶液反應的離子方程式為_ 。
(3)在0.l0mol·L-1的Na2SO4溶液中,下列離子濃度關系正確的是_ (填寫編號)。
| A.c(Na+)=c(SO42-)+c(HSO4一)+c(H2SO4) |
| B.c(OH-)="c(" HSO4-)+c(H+) |
| C.c( Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-) |
| D.c( Na+)=2c(SO42-)+2c(HSO4-) |
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
[14分]已知:I2+2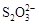

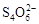 +2I―。相關物質的溶度積常數見下表:
+2I―。相關物質的溶度積常數見下表:
| 物質 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
運用化學反應原理研究碳、氮、硫、氯等單質及其化合物的反應,對生產、生活、環境保護等領域有著重要的意義。
(1)下列措施中,不利于環境保護的有 (填編號)。
a.大量開采使用化石燃料
b.使用無氟冰箱、空調
c.多步行多乘公交車,少用專車和私家車
d.將工業“廢氣”、“廢液”、“廢渣”直接排放
(2)工業上的“脫碳”指的是從“脫硝”、“脫硫”后的煙氣用堿液吸收并得到濃縮的二氧化碳。利用二氧化碳合成甲醇是碳減排的新方向。
①寫出吸收二氧化碳的離子方程式 。
②常溫下,0.1mol/LNaHCO3溶液的pH>8,則溶液中c(H2CO3) _______c(CO32-) (填“>”、“<”或“=”)。
③合成的甲醇可以做為新型燃料電池的原料,若電解液是堿性的,則其負極的電極反應式為 。
(3)二氧化氯(ClO2),為一種黃綠色氣體,是公認的高效、廣譜安全的殺菌消毒劑。工業上制備ClO2的反應原理為:4HC1(濃)+2NaClO3=2ClO2↑+Cl2↑+2H2O+2NaCl。上述反應中,產生1 mol ClO2,則被氧化的HC1為 。
(4)SO2溶于水可以得到二元弱酸H2SO3(亞硫酸)。
①25℃時,將NaOH深液與亞硫酸混合至恰好中和,則混合液中各種離子濃度的大小關系為 。
②25℃時,當NaOH溶液與H2SO3等物質的量混合時,發現混合液pH<7,請你簡要解釋其原因 。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
列式并計算下列各小題:
(1)某溫度時,測得0.01 mol/L的NaOH溶液pH為11,求該溫度下水的離子積常數Kw
(2)在此溫度下,將pH=a的NaOH溶液Va L與pH=b的硫酸Vb L混合。
①若所得混合溶液為中性,且a=12,b=2,求Va∶Vb。
②若所得混合溶液的pH=10,且a=12,b=2,求Va∶Vb。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
化學能與電能之間的相互轉化與人的生活實際密切相關,在生產、生活中有重要的應用,同時也是學生形成化學學科素養的重要組成部分。
(1)熔融狀態下,鈉的單質和氯化亞鐵能組成可充電電池(如圖1),反應原理為:2Na+FeCl2 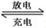 Fe+2NaCl,該電池放電時,正極反應式為 ________________ _____:
Fe+2NaCl,該電池放電時,正極反應式為 ________________ _____:
充電時,__________(寫物質名稱)電極接電源的負極;
該電池的電解質為________ _。
(2)某同學用銅片、石墨作電極電解一定濃度的硫酸銅溶液(如圖2),一段時間停止通電取出電極。若在電解后的溶液中加入0.98g氫氧化銅粉末恰好完全溶解,經測定所得溶液與電解前完全相同。請回答下列問題:
①Y電極材料是 ,發生 (填“氧化或還原”)反應。
②電解過程中X電極上發生的電極反方應式是:
③如在電解后的溶液中加入足量的小蘇打,充分反應后產生氣體在標準狀況下所占的體積是
(3)常溫時,BaSO4的Ksp=1.08×10-10,現將等體積的BaCl2溶液與2.0×10-3mol/l的Na2SO4
溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小濃度為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(12分)某學生用0.1000mol·L-1標準NaOH溶液滴定未知濃度的鹽酸,其操作可分解為以下幾步:
A移取25.00mL待測鹽酸溶液注入潔凈的錐形瓶中,并加入2~3滴酚酞溶液
B用標準NaOH溶液潤洗滴定管2~3次
C把盛有標準NaOH溶液的堿式滴定管固定好,擠壓玻璃珠,使滴定管尖嘴充滿溶液
D取標準NaOH溶液注入堿式滴定管到“0”刻度以上2~3cm
E.調節液面至“0”或“0”刻度以下,記下讀數
F.把錐形瓶放在滴定管的下面,用標準NaOH溶液滴定到終點,并記下滴定管液面的讀數
(1)下圖中屬于堿式滴定管的 (選填:“甲”、“乙”)。
(2)正確的操作順序是 (填字母序號)。
(3)上述B步操作的目的是 。
(4)判斷到達滴定終點的實驗現象是 。
(5)上述A步操作之前,若先用待測溶液潤洗錐形瓶,則對滴定結果的影響是 (填“偏大”或“偏小”或“無影響”)。
(6)若平行實驗三次,記錄的數據如下表
| 滴定次數 | 待測溶液的體積(/mL) | 標準NaOH溶液的體積 | |
| 滴定前讀數(/mL) | 滴定后讀數(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
粗CuO是將工業廢銅、廢銅合金等高溫焙燒而成的,雜質主要是鐵的氧化物及泥沙。以粗CuO為原料制備膽礬的主要流程如下:
已知Fe3+、Fe2+ 、Cu2+轉化為相應氫氧化物時,開始沉淀和沉淀完全時的pH如下表:
| | Fe3+ | Fe2+ | Cu2+ |
| 開始沉淀時的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀時的pH | 3.7 | 9.6 | 6.4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com