
【題目】空氣污染問題日益引起全民關注。
(1)PM2.5是指大氣中直徑小于或等于2.5μm(1μm =103 nm)的顆粒物。下列說法不正確的是______(填字母序號)。
a.PM2.5主要來源于火力發電、工業生產、汽車尾氣排放等過程
b.PM2.5顆粒小,所以對人體無害
c.直徑介于1 ~2.5μm的顆粒物分散到空氣中可形成膠體
d.推廣使用電動汽車,可以減少PM2.5的污染
(2)北京科研工作者用五年時間研究出利用石灰乳除工業燃煤尾氣中的硫(SO2、SO3)和氮(NO、NO2)的新工藝,既能凈化尾氣,又能獲得應用廣泛的CaSO4和Ca(NO2)2。

①硫酸型酸雨的形成過程是大氣中的SO2溶于雨水生成某種弱酸,在空氣中經催化氧化生成硫酸,該過程中反應的化學方程式依次為__________________、_________________。
②CaSO4可以調節水泥的硬化時間。尾氣中SO2與石灰乳反應生成CaSO4的化學方程式為_________。
③Ca(NO2)2可制成混凝土防凍劑、鋼筋阻銹劑等。尾氣中NO、NO2與石灰乳反應生成Ca(NO2)2的化學方程式_______________。
(3)工業上利用NO電解制備NH4NO3,其工作原理如下圖所示,陽極的電極反應為________________,陰極的電極反應為__________________________,為使電解產物全部轉化為NH4NO3,需補充物質A,A可以是______。

【答案】bcSO2+H2O![]() H2SO32H2SO3 +O2 =2H2SO42SO2 +O2 +2Ca(OH)2 =2CaSO4+2H2ONO+NO2+Ca(OH)2 =Ca(NO2)2 +H2ONO-3e-+2H2O=NO3-+4H+NO+5e-+6H+=NH4++H2ONH3·H2O
H2SO32H2SO3 +O2 =2H2SO42SO2 +O2 +2Ca(OH)2 =2CaSO4+2H2ONO+NO2+Ca(OH)2 =Ca(NO2)2 +H2ONO-3e-+2H2O=NO3-+4H+NO+5e-+6H+=NH4++H2ONH3·H2O
【解析】
(1)a.PM2.5是指大氣中直徑小于或等于2.5μm的顆粒物。它的主要來源是日常發電、工業生產、汽車尾氣排放等過程中經過燃燒而排放的殘留物; b.PM2.5表面積大,具有吸附性,能吸附大量有毒物質; c.膠體微粒直徑在10-7m~10-9m之間,PM2.5粒子的大小不符合; d.減少機動車尾氣排放,減少了煙塵,能降低空氣中PM2.5;(2)①硫酸型酸雨形成過程是SO2溶于水生成亞硫酸,再被空氣中的氧氣氧化成硫酸;②尾氣中SO2與氧氣和石灰乳反應生成CaSO4和水;③尾氣中NO、NO2與石灰乳反應生成Ca(NO2)2和水,結合氧化還原反應的特征書寫;(3)工業上電解NO制備 NH4NO3,由裝置圖可知陽極發生氧化反應,NO被氧化生成NO3-,陰極發生還原反應,NO被還原生成NH4+,陽極反應為NO-3e-+2H2O=NO3-+4H+,陰極反應為:NO+5e-+6H+=NH4++H2O,結合電極反應式解答該題.
(1)a.PM2.5是指大氣中直徑小于或等于2.5μm的顆粒物;它的主要來源是日常發電、工業生產、汽車尾氣排放等過程中經過燃燒而排放的殘留物,故a正確; b.PM2.5表面積大,具有吸附性,能吸附大量有毒物質,對人體有害,故b錯誤; c.膠體微粒直徑在10-7m~10-9m之間,PM2.5粒子的大小不符合,所以直徑介于1 ~2.5μm的顆粒物分散到空氣中不能形成膠體,故c錯誤; d.減少機動車尾氣排放,減少了煙塵,能降低空氣中PM2.5,故d正確。(2)①硫酸型酸雨形成過程是SO2溶于水生成亞硫酸,SO2+H2O![]() H2SO3;再被空氣中的氧氣氧化成硫酸,2H2SO3+O2═2H2SO4;②尾氣中SO2與氧氣和石灰乳反應生成CaSO4和水,反應方程式為:2SO2+O2+2Ca(OH)2═2CaSO4+2H2O;③尾氣中NO、NO2與石灰乳反應生成Ca(NO2)2和水,反應方程式為:NO+NO2+Ca(OH)2═Ca(NO2)2+H2O;(3)工業上電解NO制備 NH4NO3,陽極反應為NO-3e-+2H2O=NO3-+4H+,陰極反應為:NO+5e-+6H+=NH4++H2O,從兩極反應可看出,要使得失電子守恒,陽極產生的NO3-的物質的量大于陰極產生的NH4+的物質的量,總反應方程式為:8NO+7H2O
H2SO3;再被空氣中的氧氣氧化成硫酸,2H2SO3+O2═2H2SO4;②尾氣中SO2與氧氣和石灰乳反應生成CaSO4和水,反應方程式為:2SO2+O2+2Ca(OH)2═2CaSO4+2H2O;③尾氣中NO、NO2與石灰乳反應生成Ca(NO2)2和水,反應方程式為:NO+NO2+Ca(OH)2═Ca(NO2)2+H2O;(3)工業上電解NO制備 NH4NO3,陽極反應為NO-3e-+2H2O=NO3-+4H+,陰極反應為:NO+5e-+6H+=NH4++H2O,從兩極反應可看出,要使得失電子守恒,陽極產生的NO3-的物質的量大于陰極產生的NH4+的物質的量,總反應方程式為:8NO+7H2O![]() 3NH4NO3+2HNO3,因此若要使電解產物全部轉化為NH4NO3,需補充NH3·H2O。
3NH4NO3+2HNO3,因此若要使電解產物全部轉化為NH4NO3,需補充NH3·H2O。


科目:高中化學 來源: 題型:
【題目】稀H2SO4 和稀HNO3的混合液1L,其物質的量濃度分別為0.4mol·L-1和0.1mol·L-1。若向該混合液中加入足量的銅粉,則最多能溶解銅粉的質量為( )
A. 2.4gB. 3.2gC. 6.4gD. 9.6g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將下列各組物質按單質、氧化物、酸、堿分類順序排列,其中正確的是
A. 氧氣、干冰、硫酸、燒堿 B. 碘酒、冰、鹽酸、燒堿
C. 氫氣、二氧化硫、硝酸、純堿 D. 銅、硫酸鈉、醋酸、石灰水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在反應3NO2+H2O=2HNO3+NO中,若NA為阿伏加德羅常數,下列說法正確的是
A.NO2只是氧化劑B.H2O既不是氧化劑,也不是還原劑
C.NO2只是還原劑D.每生成1mol NO,轉移1 NA電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組比較Cl-、Br-、I- 的還原性,實驗如下:
實驗1 | 實驗2 | 實驗3 | |
裝置 |
|
|
|
現象 | 溶液顏色無明顯變化;把蘸濃氨水的玻璃棒靠近試管口,產生白煙 | 溶液變黃;把濕KI淀粉試紙靠近試管口,變藍 | 溶液變深紫色;經檢驗溶液含單質碘 |
下列對實驗的分析不合理的是
A. 實驗1中,白煙是NH4Cl B. 根據實驗1和實驗2判斷還原性:Br->Cl-
C. 根據實驗3判斷還原性:I->Br- D. 上述實驗利用了濃H2SO4的強氧化性、難揮發性等性質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校興趣小組對SO2與新制Cu(OH)2懸濁液的反應進行探究,實驗如下:
裝置 | 序號 | 試管中的藥品 | 現象 |
持續通入
| 實驗Ⅰ | 1.5 mL1 mol/L CuSO4溶液和3.5 mL 1mol/L NaOH溶液混合 | 開始時有磚紅色沉淀出現,一段時間后,磚紅色沉淀消失,靜置,試管底部有少量紫紅色固體,溶液呈綠色 |
實驗Ⅱ | 1.5 mL1 mol/L CuCl2溶液和3.5 mL 1 mol/L NaOH溶液混合 | 開始時有黃色沉淀出現,一段時間后,黃色沉淀消失,靜置,生成大量白色沉淀,溶液呈綠色 |
(1)制取新制Cu(OH)2懸濁液的離子方程式為__________________________________。
(2)甲同學重新用實驗II的方法制備新制Cu(OH)2懸濁液,過濾,用蒸餾水洗滌干凈。向洗凈后的Cu(OH)2中加入5 mL蒸餾水,再持續通入SO2氣體,現象與實驗I相同,此步實驗證明:__________________,檢驗Cu(OH)2洗滌干凈的方法是____________________________________________。
(3)同學們對白色沉淀的成分繼續進行探究。查閱資料如下:CuCl為白色固體,難溶于水,能溶于濃鹽酸。它與氨水反應生成Cu(NH3)2+,在空氣中會立即被氧化成含有藍色Cu(NH3)42+溶液。
①甲同學向洗滌得到的白色沉淀中加入氨水,得到藍色溶液,此過程中反應的離子方程式為:CuCl+2NH3·H2O
=Cu(NH3)2++Cl-+2H2O、____________________________。
②乙同學用另一種方法證明了該白色沉淀為CuCl,參考如下實驗方案填寫表格:

填寫下表空格:
試劑1 | _________________ | 試劑2 | 蒸餾水 |
現象1 | _________________ | 現象2 | _________________ |
③寫出實驗II中由Cu(OH)2生成白色沉淀的離子方程式:_________________。
(4)丙同學通過實驗證明:實驗Ⅰ中觀察到的磚紅色沉淀是Cu2O。完成合理的實驗方案:取少量Cu2O固體于試管中,_________________________________,則說明磚紅色沉淀是Cu2O。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
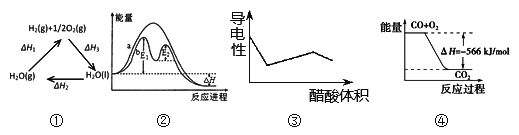
A. 圖①中△H1=△H2+△H3
B. 圖②在催化劑條件下,反應的活化能等于E1+E2
C. 圖③表示醋酸溶液滴定 NaOH 和氨水混合溶液的導電性變化曲線
D. 圖④可表示由CO(g)生成CO2(g)的反應過程和能量關系
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列依據實驗操作及現象得出的結論正確的是( )
選項 | 實驗操作 | 現象 | 結論 |
A | 向亞硫酸鈉試樣中滴入鹽酸酸化的Ba(C1O)2 溶液 | 產生白色沉淀 | 試樣已氧化變質 |
B | 向Co2O3中滴入濃鹽酸 | 產生黃綠色氣體 | 氧化性:Co2O3 > C12 |
C | 向待測液中依次滴入氯水和KSCN 溶液 | 溶液變為紅色 | 待測液中含有Fe2+ |
D | 向NaHCO3溶液中滴加NaAlO2溶液 | 有白色沉淀和氣體產生 | AlO2-與HCO3-發生了雙水解反應 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com