
�ϳɰ����g(sh��)�Ą�(chu��ng)���_(k��i)�����˹��̵�����Ҫ;�������о���(l��i)�����_����Փָ��(d��o)���ϳɰ�����(y��ng)��ƽ�ⳣ��(sh��)Kֵ�͜ضȵ��P(gu��n)ϵ���£�
| �� �ȣ��棩 | 360 | 440 | 520 |
| Kֵ | 0.036 | 0.010 | 0.0038 |
 CO(g)+3H2(g) �@ȡ����֪ԓ����(y��ng)�У���(d��ng)��ʼ��Ϛ�
CO(g)+3H2(g) �@ȡ����֪ԓ����(y��ng)�У���(d��ng)��ʼ��Ϛ�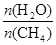 �㶨�r(sh��)���ضȡ�����(qi��ng)��(du��)ƽ���Ϛ�CH4������Ӱ����D��ʾ��
�㶨�r(sh��)���ضȡ�����(qi��ng)��(du��)ƽ���Ϛ�CH4������Ӱ����D��ʾ��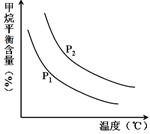
 CO2 (g)+H2(g) �@ȡ��
CO2 (g)+H2(g) �@ȡ����1����N2+3H2  2 NH3��2�֣�
2 NH3��2�֣�
�� �S�ض����ߣ�����(y��ng)��ƽ�ⳣ��(sh��)K�pС��2�֣� �� a��d��2�֣�
��2���� ����1�֣� �����ᣨ1�֣� ��3���� 60 %��2�֣��� ��2.25��2�֣� �� c��d��2�֣�
��2.25��2�֣� �� c��d��2�֣�
����ԇ�}��������1���ٹ��I(y��)�Ϻϳɰ���ԭ���ǵ�?d��)�͚�⣬��һ���ضȡ����?qi��ng)�ʹ������������ɰ��⣬����(y��ng)�Ļ��W(xu��)����ʽ��N2+3H2  2 NH3��
2 NH3��
�ڸ���(j��)���Д�(sh��)��(j��)��֪���S���ضȵ����ߣ�ƽ�ⳣ��(sh��)K�pС���@�f(shu��)�����ߜض�ƽ�����淴��(y��ng)�����Ƅ�(d��ng)�����������(y��ng)�Ƿşᷴ��(y��ng)��
�۸���(j��)����ʽ��֪��ԓ����(y��ng)���w�e�pС�ġ��ş�Ŀ��淴��(y��ng)��a������(qi��ng)��ƽ����������(y��ng)�����Ƅ�(d��ng)�������D(zhu��n)��������a���_��b������ֻ�ܸ�׃����(y��ng)���ʣ������ܸ�׃ƽ���B(t��i)�����ʹ�ú��m�Ĵ���������ߚ����D(zhu��n)���ʣ�b�����_��c��������(y��ng)�Ƿşᷴ��(y��ng)�����ߜض�ƽ�����淴��(y��ng)�����Ƅ�(d��ng) �������D(zhu��n)���ʽ��ͣ�c�����_��d�����r(sh��)���x���a(ch��n)���е�NH3�����������ﰱ��ĝ�ȣ�ƽ����������(y��ng)�����Ƅ�(d��ng)�������D(zhu��n)��������d���_�����xad��
��2���ٸ���(j��)����(y��ng) CH4(g)+H2O (g) CO(g)+3H2(g) ��֪��ԓ����(y��ng)���w�e����Ŀ��淴��(y��ng)���������Խ��(qi��ng)��ƽ�����淴��(y��ng)�����Ƅ�(d��ng)������ĺ����������Ը���(j��)�D���֪���ڜض���ͬ�ėl���£�p1��ʾ�ļ��麬���ͣ��@�f(shu��)��Խ��(qi��ng)��P1С��P2��
CO(g)+3H2(g) ��֪��ԓ����(y��ng)���w�e����Ŀ��淴��(y��ng)���������Խ��(qi��ng)��ƽ�����淴��(y��ng)�����Ƅ�(d��ng)������ĺ����������Ը���(j��)�D���֪���ڜض���ͬ�ėl���£�p1��ʾ�ļ��麬���ͣ��@�f(shu��)��Խ��(qi��ng)��P1С��P2��
�ڸ���(j��)�D���֪����Խ��(qi��ng)��ͬ�ėl���£��S���ضȵ����ߣ�����ĺ������͡��@�f(shu��)�����ߜض�ƽ����������(y��ng)�����Ƅ�(d��ng)�����ԓ����(y��ng)�����ᷴ��(y��ng)��
��3���� CO(g)+H2O(g) CO2 (g)+H2(g)
CO2 (g)+H2(g)
��ʼ��ȣ�mol/L�� 0.2 0.2 0 0
�D(zhu��n)����ȣ�mol/L�� 0.12 0.12 0.12 0.12
ƽ���ȣ�mol/L�� 0.08 0.08 0.12 0.12
����ƽ��r(sh��)CO���D(zhu��n)���ʣ�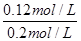 ��100%��60%
��100%��60%
���W(xu��)ƽ�ⳣ��(sh��)����һ���l���£���(d��ng)���淴��(y��ng)�_(d��)��ƽ���B(t��i)�r(sh��)���������ȵă�֮�e�ͷ���(y��ng)���ȵă�֮�e�ı�ֵ������ԓ�ض��·���(y��ng)��ƽ�ⳣ��(sh��)K�� =
=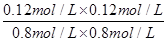 ��
�� ��
��
����һ���l���£���(d��ng)���淴��(y��ng)��������(y��ng)���ʺ��淴��(y��ng)������ȕr(sh��)��������0��������(y��ng)�wϵ�и��N���|(zh��)�ĝ�Ȼ������ٰl(f��)��׃���Ġ�B(t��i)���Q�黯�W(xu��)ƽ���B(t��i)����(j��)�˿����Дࡣa������(y��ng)ǰ���w�e��׃�����Խ��(qi��ng)ʼ�K�Dz�׃�ģ��t������(n��i)����(qi��ng)���S�r(sh��)�g��׃�����f(shu��)������(y��ng)�_(d��)��ƽ���B(t��i)��a�����_��b���ܶ��ǻ�Ϛ���|(zh��)���������ݷe�ı�ֵ���ڷ���(y��ng)�^(gu��)�����|(zh��)�����ݷeʼ�K�Dz�׃�ģ����ܶ�ʼ�K�Dz�׃�ģ����Ի�Ϛ��w���ܶȲ��S�r(sh��)�g��׃�����f(shu��)������(y��ng)�_(d��)��ƽ���B(t��i)��b�����_��c����λ�r(sh��)�g��(n��i)����a mol CO2��ͬ�r(sh��)����a mol H2�����چ�λ�r(sh��)�g��(n��i)����a mol CO2��ͬ�r(sh��)߀����amol��⣬�@�f(shu��)�����淴��(y��ng)������ȣ������f(shu��)���_(d��)��ƽ���B(t��i)��c���_��d�����ڷ���(y��ng)ǰ���w�e��׃���t���������|(zh��)���������ȣ��������Ϛ���n (CO) : n (H2O) : n (CO2) : n (H2)��1 : 16 : 6 : 6���t�˕r(sh��) =
=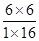 ��
�� �����ǡ����ƽ���B(t��i)��d���_�����xcd��
�����ǡ����ƽ���B(t��i)��d���_�����xcd��
���c(di��n)������ϳɰ�ԭ�������l����(du��)ƽ���B(t��i)��Ӱ푣�����(y��ng)���ʺ�ƽ�ⳣ��(sh��)��Ӌ(j��)�㡢ƽ���B(t��i)���Д��Լ��D������c��(y��ng)�õ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� С�W(xu��)��10��犑�(y��ng)���}ϵ�д�
С�W(xu��)��10��犑�(y��ng)���}ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
��һ���w�e�����]�����У��M(j��n)�����»��W(xu��)����(y��ng)��
Fe2O3(s)��3CO(g)  2Fe(s)��3CO2(g)���仯�W(xu��)ƽ�ⳣ��(sh��)K�͜ض�t���P(gu��n)ϵ���±���
2Fe(s)��3CO2(g)���仯�W(xu��)ƽ�ⳣ��(sh��)K�͜ض�t���P(gu��n)ϵ���±���
| t�� | 1000 | 1150 | 1300 |
| K | 64.0 | 50.7 | 42.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
��(du��)��A(g)+B(g)  xC��g�� ��H ��:
xC��g�� ��H ��: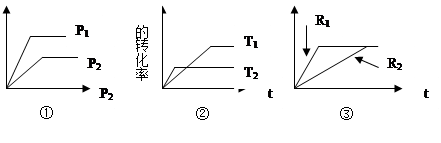
��1���وD����P1 P2 ,��x��ֵ�� ��
��2���ڈD����T1 T2 ���Ҧ�H 0��
��3������ۈDR1,R2�քe��ʾ��׃����(qi��ng)���tR1 R2 ,x��ֵ�� ��
��4������ۈD�քe��ʾ�Пo(w��)�������tR1��ʾ ������
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
(6��)��֪��T�桢P kpa�r(sh��)���ݷe��V �����]�����г���1molA��2molB�����ֺ�غ㉺ʹ����(y��ng)�_(d��)ƽ�⣺A(g)+B(g) C(g)��ƽ��r(sh��)C ���w�e��?j��n)?sh��)��40�G��
C(g)��ƽ��r(sh��)C ���w�e��?j��n)?sh��)��40�G��
(1)�����֜ضȡ�����(qi��ng)�������l���²�׃�������]�����г���2molA��4molB���tƽ��r(sh��)�wϵ�ݷe�� ��C���w�e��?j��n)?sh��)�� ��
(2)��ȡһ��(g��)�ݷe�̶���׃�����]�������Կ��ƜضȞ�T(m��n)�棬����1molB��1molC��Ҫʹƽ��r(sh��)C ���w�e��?j��n)?sh��)�Ԟ�40�G���tԓ���]�����w�e�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
��2L���]������(n��i)��800��r(sh��)����(y��ng)��2NO(g)+O2(g)  2NO2(g)�wϵ�У�n(NO)�S�r(sh��)�g��׃�������
2NO2(g)�wϵ�У�n(NO)�S�r(sh��)�g��׃�������
| �r(sh��)�g(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
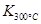 ��
��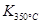 ���tԓ����(y��ng)�� �ᷴ��(y��ng)��
���tԓ����(y��ng)�� �ᷴ��(y��ng)��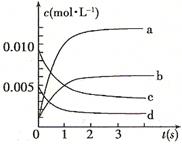
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
ú�����г����о���ͬ�ض���ƽ�ⳣ��(sh��)��Ͷ�ϱȼ���ֵ�Ȇ�(w��n)�}����֪��
CO(g)+H2O(g) H2(g)+CO2(g)ƽ�ⳣ��(sh��)�S�ضȵ�׃�����±���
H2(g)+CO2(g)ƽ�ⳣ��(sh��)�S�ضȵ�׃�����±���
| �ض�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��(sh��)K | 9.94 | 9 | 1 |
 H2(g)+CO2(g)����(d��ng)����(y��ng)�_(d��)ƽ��r(sh��)��CO���w�e��?j��n)?sh��)��X�����S���������w�e�͜ضȲ�׃����ʼ���|(zh��)�������ķN��ȳ���ԓ�����У��_(d��)��ƽ��r(sh��)CO���w�e��?j��n)?sh��)������X����
H2(g)+CO2(g)����(d��ng)����(y��ng)�_(d��)ƽ��r(sh��)��CO���w�e��?j��n)?sh��)��X�����S���������w�e�͜ضȲ�׃����ʼ���|(zh��)�������ķN��ȳ���ԓ�����У��_(d��)��ƽ��r(sh��)CO���w�e��?j��n)?sh��)������X���� �鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
��һ���w�e�����]�����У��M(j��n)�����·���(y��ng)��A��g�� B��g��+C��g�����仯�W(xu��)ƽ�ⳣ��(sh��)K�͜ض�t���P(gu��n)ϵ���±���ʾ��
| toC | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

| �r(sh��)�gt/min | 0 | 1 | 2 | 4 | 8 | 16 | 20 |
| C��A��/��mol��L��1�� | 10.4 | 8.6 | 7.5 | 6.6 | 5.9 | 5.5 | 5.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
��D��ú�����a(ch��n)�I(y��)朵�һ���֣�ԇ�\(y��n)�����W(xu��)֪�R(sh��)����Q���І�(w��n)�}��
��1����֪ԓ�a(ch��n)�I(y��)���ij����(y��ng)��ƽ�ⳣ��(sh��)���_(d��)ʽ�飺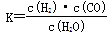 ��������(du��)��(y��ng)����(y��ng)�Ļ��W(xu��)����ʽ��
��������(du��)��(y��ng)����(y��ng)�Ļ��W(xu��)����ʽ��
_________________________________��
��2���ϳɼ״�����Ҫ����(y��ng)�ǣ�2H2��g��+CO��g�� CH3OH��g��+90.8kJ��t���´˷���(y��ng)��ƽ�ⳣ��(sh��)��160���˜ض��£������]�������_(k��i)ʼֻ����CO��H2������(y��ng)l0min��y(c��)�ø��M�ֵĝ�����£�
CH3OH��g��+90.8kJ��t���´˷���(y��ng)��ƽ�ⳣ��(sh��)��160���˜ض��£������]�������_(k��i)ʼֻ����CO��H2������(y��ng)l0min��y(c��)�ø��M�ֵĝ�����£�
| ���|(zh��) | H2 | CO | CH3OH |
| ��ȣ�mol/L�� | 0.2 | 0.1 | 0.4 |
| ����(y��ng) | ���̵� | ���I(y��)�̵� | ||||
| �ض�/�� | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84��10-31 | 0.1 | 5��108 | 1.847 | 0.507 | 0.152 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
��һ�w�e��10 L�������У�ͨ�^(gu��)һ������CO��H2O,850 ��r(sh��)�l(f��)������(y��ng)��
CO(g)��H2O(g)  CO2(g)��H2(g)
CO2(g)��H2(g)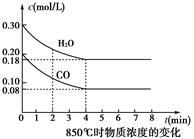
��1��CO��H2O���׃����D���t0��4 min��ƽ������(y��ng)����v(CO)��______mol��L��1��min��1��
��2����D��4��5min֮�gԓ����(y��ng)________(��ǡ���)̎��ƽ���B(t��i)���Д�����________________________________________________________________________��
�鿴�𰸺ͽ���>>
��(gu��)�H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com