
��D��ʾij�ضȕr������(y��ng)N2O4(g) 2NO2(g)��ǰ110 s��(n��i)�ķ���(y��ng)�M����r��Ո����(j��)�D��ش����І��}��
2NO2(g)��ǰ110 s��(n��i)�ķ���(y��ng)�M����r��Ո����(j��)�D��ش����І��}��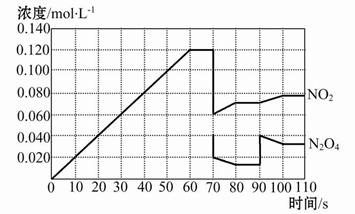
(1)ԓ���淴��(y��ng)�_��ƽ��ĕr�g�Ξ� ��
(2)����(y��ng)�M�е�70 s�r����׃�ėl�������� (����ĸ����ͬ),����(y��ng)�M�е�90 s�r����׃�ėl�������� ��
| A��������� | B��?d��ng)U�������w�e |
| C�����ߜض� | D������N2O4�ĝ�� |

| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
��ij���]�����м���0.15 mol/L A��0.05 mol/L C��һ������B���N���w��һ���l���°l(f��)������(y��ng)�������|(zh��)����S�r�g׃����D�мD��ʾ[t0�rc(B)δ������t1�r����0.05 mol/L]���҈D��t2�r�̺��׃����(y��ng)�l����ƽ���wϵ�������淴��(y��ng)�����S�r�g׃������r��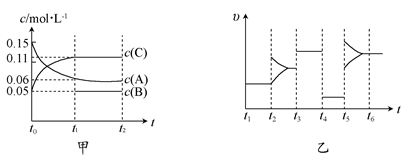
(1)��t4�r��׃�ėl����pС�������tB����ʼ���|(zh��)������Ȟ�_____mol/L��
(2)��t5�r��׃�ėl�������أ��˕rv(��)>v(��)����A�����|(zh��)�����p��0.03 mol�r�������c���ğύ�Q������akJ������ԓ����(y��ng)�ğữ�W(xu��)����ʽ_______��
(3)��t1��15s���tt0��t1�A����C���׃����ʾ��ƽ������(y��ng)���ʞ�v(C)��_______ mol/L��A���D(zhu��n)���ʞ�________��
(4)t3�r��׃��ijһ����(y��ng)�l��������________(�x����̖)��
a��ʹ�ô���
b������
c������(y��ng)����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�ü�����̼���}��ϡ�}�ᷴ��(y��ng)��ȡ������̼���w��Ո�ش�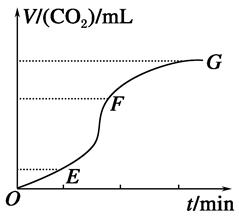
��1������^����D��ʾ�������Дࣺ__________�λ��W(xu��)����(y��ng)������죬________���ռ��Ķ�����̼���w��ࡣ
��2�����˜p����������(y��ng)�Ļ��W(xu��)���ʣ�������Һ�м����������|(zh��)�����J����е���________������ĸ��̖����
| A�����sˮ | B��NaCl���w | C��NaCl��Һ | D�����}�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
��1.0 L���]�����з���0.10 mol A (g)����һ���ض��M�����·���(y��ng)��A(g)  B(g)��C(g)����H����85.1 kJ��mol��1
B(g)��C(g)����H����85.1 kJ��mol��1
����(y��ng)�r�g(t)�c������(n��i)���w������(p)�Ĕ�(sh��)��(j��)Ҋ�±���
| �r�gt/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| ������p /100 kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
| ����(y��ng)�r�gt/h | 0 | 4 | 8 | 16 |
| c(A)/(mol��L��1) | 0.10 | a | 0.026 | 0.006 5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�_�l(f��)����Դ�����U̎�����ǿɳ��m(x��)�l(f��)չ����Ҫ���档
��1����̼��������ֱ�Ӻϳ��Ҵ�ȼ�����M���Ҏ(gu��)ģ���a(ch��n)�����ȡ��CO��H2��ԭ�Ϻϳ��Ҵ������W(xu��)����(y��ng)����ʽ��2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)�������]�����г���10 mol CO�c20mol H2���ڴ��������·���(y��ng)�����Ҵ���CO���D(zhu��n)����(��)�c�ضȡ��������P(gu��n)ϵ���D��ʾ��
CH3CH2OH(g)+H2O(g)�������]�����г���10 mol CO�c20mol H2���ڴ��������·���(y��ng)�����Ҵ���CO���D(zhu��n)����(��)�c�ضȡ��������P(gu��n)ϵ���D��ʾ��
����A��B���c��ʾ��ij�r���_����ƽ���B(t��i)���˕r��A�c�r�������w�e��10L���tԓ�ض��µ�ƽ�ⳣ��(sh��)��K�� ��
����A��C���c����ʾ�_����ƽ���B(t��i)���t�Է���(y��ng)�_ʼ���_ƽ���B(t��i)����ĕr�gtA tC������ڡ�����С�ڡ����ڡ�����
�۹��I(y��)��߀���Բ�ȡ��CO2��H2��ԭ�Ϻϳ��Ҵ������Ҹ������W(xu��)�������Ƴ磬��������ͬ�l���£���CO��ȡCH3CH2OH��ƽ�ⳣ��(sh��)�h�h������CO2��ȡCH3CH2OH��ƽ�ⳣ��(sh��)��Ո�Ɯy���W(xu��)�������J����CO2��ȡCH3CH2OH�ă�(y��u)�c��Ҫ�ǣ� ��
��2��Ŀǰ���I(y��)��Ҳ������CO2�����a(ch��n)�״���һ���l���°l(f��)������(y��ng)CO2(g)��3H2(g) CH3OH(g)��H2O(g)����6mol CO2��8 mol H2����2L�����]�����У��y��H2�����|(zh��)�����S�r�g׃�����������҈D��ʾ����������
CH3OH(g)��H2O(g)����6mol CO2��8 mol H2����2L�����]�����У��y��H2�����|(zh��)�����S�r�g׃�����������҈D��ʾ����������
��Ո�ڴ��}��D���L���״������|(zh��)�����S�r�g׃��������
�ڃH��׃ijһ���l�����M�ЃɴΌ��y��H2�����|(zh��)�����S�r�g׃����D��̓����ʾ������I����(y��ng)�Č��l����׃�� ��������?q��)��?y��ng)�Č��l����׃�� ��
��3��Hg��ˮ�w��Ⱦ���ؽ���Ԫ��֮һ��ˮ��Һ�ж��r������Ҫ�����ΑB(t��i)�cCl����OH���ĝ���P(gu��n)ϵ���҈D��ʾ�ۈD�е����|(zh��)������ֻ��Hg(OH)2���y���pCl=��1gc(Cl��)��
�������f�������_���� ��
A�����˷�ֹHg2��ˮ�⣬����Hg(NO3)2��Һ�r��(y��ng)��Hg(NO3)2���w���ڝ��������ϡ�
B����(d��ng)c(C1��) ��10��1 mol��L��1�r����Ԫ��һ��ȫ����HgCl42����ʽ����
C��HgCl2��һ�N��늽��|(zh��)������x����ʽ�ǣ�HgCl2��HgCl�� + C1��
D����(d��ng)��ҺpH������4��pCl��2��׃��6�r����ʹHgCl2�D(zhu��n)����Hg(OH)2
��HgCl2�ַQ�������������c549K���ӟ������A���侧�w�� ����w��ͣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
T �桢2 L���]������ijһ����(y��ng)�ڲ�ͬ�r�̵ĸ����|(zh��)������D��ʾ(E����w,��������w)���ش����І��}��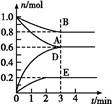
(1)����ԓ����(y��ng)�Ļ��W(xu��)����ʽ: ��
(2)����(y��ng)�_ʼ��3 min�r,��D��ʾ��ƽ������(y��ng)���ʞ� mol��L-1��min-1��
(3)T ��r,ԓ����(y��ng)�Ļ��W(xu��)ƽ�ⳣ��(sh��)K= ��
(4)��6 min�r,���֜ضȲ�׃,���������w�e�sС��ԭ����һ��,�����_��ƽ���,D���w�e�֔�(sh��)�� ��
(5)����һ��2 L�����]����,T �桢ijһ�r��,�����и����|(zh��)�����|(zh��)���������ʾ��
| ���|(zh��) | A | B | D | E |
| ���|(zh��)����(mol) | 0.8 | 1.0 | 0.4 | 0.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
25 ��r�����w�e��2 L�����]�����У���B(t��i)A��B��C�����|(zh��)����n�S�r�gt��׃����D1��ʾ����֪�_��ƽ����͜ضȣ�A���D(zhu��n)���ʌ�����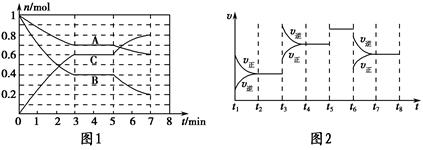
| t2��t3 | t4��t5 | t5��t6 | t7��t8 |
| K1 | K2 | K3 | K4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
��ˮú���D(zhu��n)���ɺϳɚ⣬Ȼ��ϳɸ��N��Ʒ��ʯ���a(ch��n)Ʒ�ǻ����ĘO����Ҫ���I(l��ng)��ȥˮ������ˮú����Ҫ��H2��CO��CO2��������H2S��CH4���^�m(x��)��ȥH2S�ɲ��ô���Ǵ��D(zhu��n)�����g(sh��)����CH4�D(zhu��n)����CO���õ�CO��CO2��H2�Ļ�Ϛ��w��������ĺϳɼ״�ԭ�Ϛ⡣
(1)��ˮú�����Ҫ���W(xu��)����(y��ng)����ʽ�飺C(s)+H2O(g) CO(g)+H2(g)���˷���(y��ng)�����ᷴ��(y��ng)��
CO(g)+H2(g)���˷���(y��ng)�����ᷴ��(y��ng)��
�ٴ˷���(y��ng)�Ļ��W(xu��)ƽ�ⳣ��(sh��)���_ʽ�� ��
������������̼���D(zhu��n)���ʵĴ�ʩ�� ��
| A������C(s) | B������H2O(g) | C�����ߜض� | D������ |
 CO(g)+2H2O(g) ��H="-519" kJ/mol�����I(y��)��Ҫ�x����m�Ĵ������քe��X��Y��Z���N�����M�������(�����l����ͬ)
CO(g)+2H2O(g) ��H="-519" kJ/mol�����I(y��)��Ҫ�x����m�Ĵ������քe��X��Y��Z���N�����M�������(�����l����ͬ)�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�ֽ�ˮ�ƚ��Ĺ��I(y��)�Ʒ�֮һ������ѭ�h(hu��n)����Ҫ�漰���з���(y��ng)��
I SO2+2H2O+I2��H2SO4+2HI
II 2HI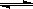 H2+I2
H2+I2
III 2H2SO4 �� 2SO2+O2+2H2O
��1��������������(y��ng)�����������_����_________
a������(y��ng)III���ڳ������M�� b������(y��ng)I��SO2߀ԭ�Ա�HI��
c��ѭ�h(hu��n)�^�������a��H2O d��ѭ�h(hu��n)�^���Юa(ch��n)��1molO2��ͬ�r�a(ch��n)��1molH2
��2��һ���ض��£���2L���]�����м���1molHI��g�����l(f��)������(y��ng)II��H2���|(zh��)�����S�r�g��׃����D��ʾ��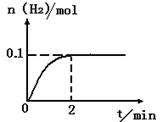
0��2min��(n��i)��ƽ������(y��ng)����v(HI)= _________ ��ԓ�ض��£�����(y��ng)2HI��g��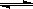 H2��g��+I2��g����ƽ�ⳣ��(sh��)���_ʽ��K=_______________________����ͬ�ض��£����_ʼ����HI��g�������|(zh��)������ԭ����2�����t_________��ԭ����2����
H2��g��+I2��g����ƽ�ⳣ��(sh��)���_ʽ��K=_______________________����ͬ�ض��£����_ʼ����HI��g�������|(zh��)������ԭ����2�����t_________��ԭ����2����
a��ƽ�ⳣ��(sh��) b��HI��ƽ����
c���_��ƽ��ĕr�g d��ƽ��rH2���w�e�֔�(sh��)
��3��SO2��һ���l���¿���������SO3����������(y��ng)�飺2SO2 (g) + O2(g)  2SO3(g) + Q�����˷���(y��ng)��ʼ�����|(zh��)������ͬ���t�����P(gu��n)ϵ�D���_����_________ (����̖)
2SO3(g) + Q�����˷���(y��ng)��ʼ�����|(zh��)������ͬ���t�����P(gu��n)ϵ�D���_����_________ (����̖)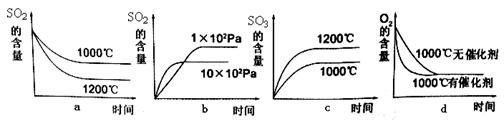
���H���I(y��)���a(ch��n)ʹ�õėl���ǣ�������____________________________________�x��ԓ�l����ԭ����__________________��
��4�����H���a(ch��n)�ð�ˮ����SO2���Ɂ�������@�}���F(xi��n)ȡa��ԓ�@�}�������е�SO2ȫ������(y��ng)��������(y��ng)����18.4 mol/L��������Һ���w�e������______________��
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com