
二氧化氯(ClO2)為一種黃綠色氣體,是國際上公認的高效、廣譜、快速、安全的殺菌消毒劑。
(1)工業上制備ClO2的反應原理常采用:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①濃鹽酸在反應中顯示出來的性質是_______(填序號)。
| A.只有還原性 | B.還原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
(1)①B ② 0.1
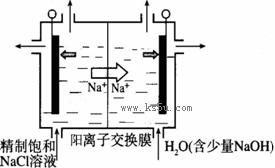
(2)①Cl- - 5e-+2H2O=ClO2↑+4H+
②0.01 在陰極發生2H++2e-=H2↑,H+濃度減小,使得H2O OH-+H+的平衡向右移動,OH-濃度增大,pH增大
OH-+H+的平衡向右移動,OH-濃度增大,pH增大
(3)2ClO2+2CN-=N2↑+2CO2↑+2Cl- 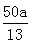 (或3.85a)
(或3.85a)
解析試題分析:(1)濃鹽酸在反應中的產物是Cl2和NaCl,一部分化合價升高,一部分沒變生成鹽,故選B;在反應2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl中每生成1molClO2轉移1mol電子,故若反應中產生0.1molClO2,則轉移電子的物質的量為0.1mol;(2)陽極發生氧化反應,即Cl-放電生成ClO2。陰極H+放電生成H2,每生成112 mL H2,即有0.01molH+放電,那么通過陽離子交換膜的陽離子的物質的量為0.01mol(3)100 m3污水中含有CN-的物質的量為:100 m3*1000L/ m3*a mg/L*10-3g/mg/26g/mol=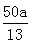
考點:本題綜合考查氧化還原和電化學、化學平衡理論。


 智能訓練練測考系列答案
智能訓練練測考系列答案科目:高中化學 來源: 題型:填空題
I(1)在淀粉碘化鉀溶液中通入少量氯氣,立即會看到溶液變藍色,反應的離子方程式是 。
(2)在碘和淀粉形成的藍色溶液中通入SO2氣體,發現藍色逐漸消失,反應的離子方程是 。
(3)對比(1)和(2)實驗所得的結果,將Cl 、I
、I SO2按還原性由強到弱順序排列為 。
SO2按還原性由強到弱順序排列為 。
II (4) 除去鐵粉中混有鋁粉的試劑是 ,離子方程式為
(5) 1mol過氧化鈉與2mol碳酸氫鈉固體混合后,在密閉容器中加熱充分反應,排出氣體物質后冷卻,殘留的固體物質是
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知制取氯氣也可用濃鹽酸與高錳酸鉀為原料,其化學方程式為
2KMnO4+16HCl(濃)=2MnCl2+2KCl+5Cl2↑+8H2O。請回答下列問題:
(1)用雙線橋法標出該化學式電子轉移的方向與數目:
2KMnO4+16HCl(濃)=2MnCl2+2KCl+5Cl2↑+8H2O。
(2)反應中被還原的元素為 (寫名稱);標準狀況下當生成112 L氯氣時,反應中轉移的電子數目為 。
(3)若有4 molHCl被氧化,則可生成標準狀況下的氯氣 L。
(4)若有1.58g高錳酸鉀和100mL10moL/L濃鹽酸充分反應(不考慮鹽酸揮發,忽略溶液體積的前后變化),反應至終點時高錳酸鉀紫色完全褪去,則被氧化的HCl的物質的量
為 mol。將反應后的溶液取出10mL,加入足量的硝酸銀溶液,可得到沉淀的物質的量為 mol。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)某化學課外小組用海帶為原料制取少量碘水,現在用四氯化碳在碘水中萃取碘單質,并用分液漏斗分離兩種溶液。其實驗操作可分解為如下幾步:
| A.把盛有溶液的分液漏斗敖在鐵架臺的鐵圈中: |
| B.把50mL碘水和15mL四氯化碳加入分液漏斗中,并蓋好玻璃塞: |
| C.檢驗分液漏斗活塞和上口玻璃塞是否漏液; |
| D.倒轉漏斗,用力振蕩,并不時旋開活塞放氣,最后關閉活塞: |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氧化還原反應規律是化學學科的重要規律之一。按要求回答下列問題:
(1) 被稱為萬能還原劑的NaBH4溶于水并和水反應:NaBH4+2H2O=NaBO2+4H2↑,此反應中B元素的化合價沒有發生變化,則NaBH4中H的化合價為___________,該反應氧化產物是______________,還原產物是______________。
(2) 有下列三個反應:
①Cl2+FeI2=FeCl2+I2 ;②2Fe2++Br2=2Fe3++2Br-;③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
①根據以上方程式可以得到Fe2+、Co2+、Br-、I-還原性由強的弱的順序為_________;
②1molCo2O3能氧化HCl的物質的量_____________。
(3) 完成并配平下列化學反應方程式:
□KMnO4+□H2C2O4+□________ □CO2+□K2SO4+□MnSO4+□H2O
□CO2+□K2SO4+□MnSO4+□H2O
(4)一個完整的氧化還原反應方程式可以拆寫成兩個“半反應式”,一個是“氧化反應式”,一個是“還原反應式”。如2H+ +Zn=Zn2++H2↑,可拆寫為氧化反應式:Zn-2e-=Zn 2+,還原反應式:2H++ 2e-=H2↑。并由此實現了化學能與電能的相互轉化。據此,回答下列問題:
①將2Fe3++Cu= 2Fe2+ +Cu2+拆寫為兩個“半反應式”:其中,氧化反應式為 。
②由①中的反應,可設計成如右圖所示的原電池:
若電極a為Cu ,電解質溶液甲的化學式為 ;
電極b處的電極反應式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)鑒別Fe(OH)3膠體和FeCl3溶液的方法是
(2)除去KNO3溶液中的I2雜質,主要操作步驟是:加CCl4后,振蕩,靜置, 。水溶液最終從分液漏斗的 分離出來
(3)黑火藥是中國的“四大發明”之一。黑火藥在發生爆炸時,發生如下的反應:
2KNO3+C+S=K2S+2NO2↑+CO2↑。其中被氧化的元素是 ,氧化劑是 ,生成1molCO2時轉移的電子數目為(NA表示阿伏伽德羅常數的值)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鈣是自然界存在最廣泛的IIA族元素,常以化合物N存在。從鈣單質起始發生的一系列化學反應可由下圖表示: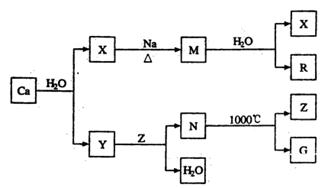
(1)鈣元素在周期表中位于第______周期;Y中存在的化學鍵類型為_______________;N的化學式是______________。
(2)M與水反應的化學方程式為______________________________________________.
(3)Z和G的電子式分別為_______________________和_________________________.
(4)Z與R反應可能生成的鹽有________________________________(填化學式)。
(5)實際生產中,可由N為原料制備單質鈣,簡述一種制備方法:
_________________________________________________________________________.
(6)金屬鈣線是煉制優質鋼材的脫氧脫磷劑。某鈣線的主要成分含Fe元素和Ca元素。
請配平下列用鈣線脫氧脫磷的化學方程式: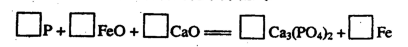
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
美國科學家理查德·海克和日本科學家根岸英一、伶木彰因在研發“有機合成中的鈀催化的交叉偶聯”而獲得諾貝爾化學獎。有機合成常用的鈀/活性炭催化劑,長期使用催化劑會被雜質(如:鐵、有機物等)污染而失去活性,成為廢催化劑,需對其再生回收,一種由廢催化劑制取氯化鈀的工藝流程如下: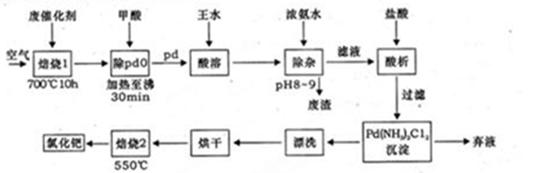
(1)甲酸還原氧化鈀的化學方程式為 。
(2)鈀在王水(濃硝酸與濃鹽酸按體積比1:3)中轉化為H2PdC14,硝酸被還原為NO,該反應的化學方程式為: 。
(3)鈀精渣中鈀的回收率高低主要取決于王水溶解的操作條件,已知反應溫度、反應時間和王水用量對鈀回收率的影響如下圖1—圖3所示,則王水溶液鈀精渣的適宜條件(溫度、時間和王水用量)為 、 、 。
(4)加濃氨水時,鈀轉變為可溶性[Pd(NH3)4]2—。此時鐵的存在形式是 (寫化學式)
(5)700℃焙燒1的目的是: ;550℃焙燒2的目的是: 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(10分)為探究H2O2、SO2、Br2氧化性強弱,某小組同學設計如下實驗(夾持及尾氣處理裝置已略去,氣密性已檢驗)。
| 實驗操作 | 實驗現象 |
| ⅰ.打開A中分液漏斗活塞,滴加濃硫酸 | A中有氣泡產生,B中紅棕色溴水褪色,C中有白色沉淀 |
| ⅱ.取C中沉淀加入鹽酸 | C中白色沉淀不溶解 |
| ⅲ.打開B中分流漏斗活塞,逐滴滴加H2O2 | 開始時顏色無明顯變化;繼續滴加H2O2溶液,一段時間后,混合液逐漸變成紅棕色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com