
【題目】淡黃色固體A和氣體X存在如下轉化關系:請回答下列問題:

(1)固體A的名稱___。
(2)將39克固體A投入到69克水中完全反應產生的氣體在標準狀況下的體積為多少毫升___?所得溶液的質量分數是多少___?(要求寫出計算過程)
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】甲醇既可用于基本有機原料,又可作為燃料用于替代礦物燃料。
(1)以下是工業上合成甲醇的反應:![]()
![]() 下表所列數據是該反應在不同溫度下的化學平衡常數
下表所列數據是該反應在不同溫度下的化學平衡常數![]() .
.
溫度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中數據判斷反應I為 ______ 熱反應(填“吸”或“放”) ![]() 某溫度下,將2molCO和6molH2充入2L的密閉容器中,充分反應,達到平衡后,測得
某溫度下,將2molCO和6molH2充入2L的密閉容器中,充分反應,達到平衡后,測得![]() ,則CO的轉化率為 ______ ,此時的溫度為 ______ 從表中選擇.
,則CO的轉化率為 ______ ,此時的溫度為 ______ 從表中選擇.
(2)已知在常溫常壓下:
①![]()
②![]()
③![]()
則反應![]() ______
______ ![]() 用
用![]() 、
、![]() 、
、![]() 表示
表示
(3)處理廢水時,最后![]() 以
以![]() 形式除去,當
形式除去,當![]() 時,
時,![]() 沉淀完全,此時溶液的
沉淀完全,此時溶液的![]() ______ (已知,
______ (已知,![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗不能達到實驗目的的是( )
A. 實驗室制取氨氣
實驗室制取氨氣
B.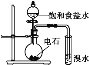 證明乙炔可使溴水褪色
證明乙炔可使溴水褪色
C.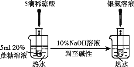 檢驗蔗糖的水解產物具有還原性
檢驗蔗糖的水解產物具有還原性
D.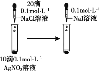 證明溶解度:AgCl>AgI
證明溶解度:AgCl>AgI
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用有機物甲可制備環己二烯(![]() ),其反應路線如圖所示:
),其反應路線如圖所示:

下列有關判斷不正確的是
A.甲的分子式為 C6H12
B.乙與環己二烯互為同系物
C.上述流程發生的反應類型有取代反應、消去反應、加成反應
D.環己二烯與溴水 1:1 反應可得 2 種產物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋅和鋁都是活潑金屬,其氫氧化物既能溶于強酸,又能溶于強堿。但是氫氧化鋁不溶于氨水,而氫氧化鋅能溶于氨水,生成![]() 。
。
回答下列問題:
(1)寫出鋅和氫氧化鈉溶液反應的化學方程式
_________________________________________________________________。
(2)下列各組中的兩種溶液,用相互滴加的實驗方法即可鑒別的是________。
①硫酸鋁和氫氧化鈉 ②硫酸鋁和氨水
③硫酸鋅和氫氧化鈉 ④硫酸鋅和氨水
(3)寫出可溶性鋁鹽與氨水反應的離子方程式
_________________________________________________________________。
(4)試解釋在實驗室不適宜用可溶性鋅鹽與氨水反應制備氫氧化鋅的原因
__________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由兩種常見金屬組成的混合物A,在合適的條件下可按下圖進行反應(部分產物和水省略),已知F為紅褐色沉淀,請回答:

回答下列問題:
(1)混合物A的成分是_________(請填化學式)。
(2)反應①的離子方程式為:__________。
(3)反應②的化學方程式為:__________。
(4)寫出E中加入過量NaOH的所有反應的離子方程式:_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】磷烯(如圖)是由磷原子六元環組成的蜂巢狀褶皺二維晶體,它是白磷(![]() )的同素異形體。設NA為阿伏加德羅常數,下列說法正確的是
)的同素異形體。設NA為阿伏加德羅常數,下列說法正確的是

A.3.1g白磷中含P—P鍵的數目為0.3NA
B.6.2g磷烯中含六元環的數目為0.1NA
C.0.1molP4與0.6molH2在密閉容器中發生反應P4+6H2![]() 4PH3,生成PH3分子的數目為0.4NA
4PH3,生成PH3分子的數目為0.4NA
D.0.1molP4發生反應P4+5O2=2P2O5,轉移的電子數為20NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,針對表中①到⑩10種元素,填寫下表空白:
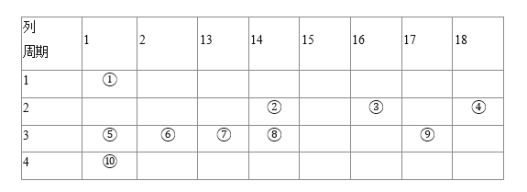
(1)在最高價氧化物對應的水化物中,酸性最強的化合物的化學式是______,堿性最強的化合物的化學式是______。![]() 均填化學式
均填化學式![]()
(2)最高價氧化物對應的水化物是兩性的元素是______![]() 填元素符號
填元素符號![]() ,寫出它的氫氧化物與⑤的氫氧化物反應的離子方程式______。
,寫出它的氫氧化物與⑤的氫氧化物反應的離子方程式______。
(3)③⑤⑥三元素形成的簡單離子具有相同的電子層結構,它們的離子半徑由大到小順序是![]() 用離子符號表示
用離子符號表示![]() ______。
______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com