
Ⅰ. 在水溶液中橙紅色的Cr2O72-與黃色的CrO42-有下列平衡關系:
Cr2O72-+H2O  2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液后,溶液呈 色,因為 。
(2)向已加入NaOH溶液的(1)中再加入過量稀H2SO4后,則溶液呈 色,因為 。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4為黃色沉淀)則平衡向 方向移動,溶液顏色將 。(填“變深”、“變淺”或“不變”)
Ⅱ.實驗室有一未知濃度的稀鹽酸,某學生為測定鹽酸的濃度在實驗室中進行如下實驗:
1.配制100mL 0.10mol/L NaOH標準溶液。
2.取20.00mL待測稀鹽酸溶液放入錐形瓶中,并滴加2~3滴酚酞作指示劑,用自己配制的標準NaOH溶液進行滴定。
3.重復上述滴定操作2~3次,記錄數據如下。
| 實驗編號 | NaOH溶液的濃度 (mol/L) | 滴定完成時,NaOH溶液滴入的體積(mL) | 待測鹽酸溶液的體積 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.58 | 20.00 |
| 3 | 0.10 | 22.60 | 20.00 |



Ⅰ.每空1分(1)黃;中和H+,使c(H+)減小,平衡向正反應方向移動
(2)橙紅色;增加生成物c(H+),平衡向逆反應方向移動 (3)正反應(右) 變淺
Ⅱ.(1)①最后一滴氫氧化鈉溶液加入,溶液由無色恰好變淺紅色,且半分鐘內不褪色 ②8.2~10 (2)0.1130mol/L(不寫單位扣1分) (3)丙 (4)EF(2分)
解析試題分析:Ⅰ.(1)向上述溶液中加入NaOH溶液后,溶液中OH-濃度增大,中和氫離子,降低氫離子的濃度。則根據Cr2O72-+H2O  2CrO42-+2H+可知,平衡向正反應方向移動,所以溶液呈黃色。
2CrO42-+2H+可知,平衡向正反應方向移動,所以溶液呈黃色。
(2)向已加入NaOH溶液的(1)中再加入過量稀H2SO4后,增加生成物c(H+),平衡向逆反應方向移動因此溶液呈橙紅色。
(3)向原溶液中加入Ba(NO3)2溶液,則Ba2+結合CrO42-生成BaCrO4黃色沉淀,降低CrO42-的濃度,所以平衡向正反應方向移動。由于離子的濃度降低,因此溶液顏色將變淺。
Ⅱ.(1)①由于堿能使酚酞顯紅色,而酸使酚酞不白色。所以用氫氧化鈉溶液滴定鹽酸時,滴定達到終點的現象是最后一滴氫氧化鈉溶液加入,溶液由無色恰好變淺紅色,且半分鐘內不褪色、由于酚酞的變色范圍是8.2~10.0,所以此時錐形瓶內溶液的pH范圍為8.2~10.0。
(2)根據表中數據可知,三次實驗中消耗氫氧化鈉溶液的體積分別是22.62ml-0.10ml=22.52ml、22.58ml-0.10ml=22.48ml、22.60ml-0.10ml=22.50ml,所以三次實驗中平均消耗氫氧化鈉溶液的體積是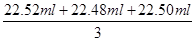 =22.50ml。因此鹽酸的濃度是
=22.50ml。因此鹽酸的濃度是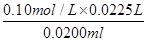 =0.1130mol/L。
=0.1130mol/L。
(3)由于堿式滴定管的下面是含有玻璃球的橡膠管,因此擠壓玻璃球使尖嘴部分充滿堿液的正確操作是選項丙。
(4)根據 可知,由于C標、V待均為定植,所以C測的大小取決于V標的大小,即V標:偏大或偏小,則C測偏大或偏小,據此可以判斷。A、滴定終點讀數時俯視讀數,則讀數偏小,因此消耗氫氧化鈉溶液的體積偏小,測定結果偏低;B、酸式滴定管使用前,水洗后未用待測鹽酸溶液潤洗,則鹽酸被稀釋,濃度降低。因此消耗氫氧化鈉溶液的體積偏小,測定結果偏低;C、錐形瓶水洗后未干燥,不改變溶質的物質的量,不影響結果;D、配制NaOH標準溶液時,沒有等溶解液降至室溫就轉移至容量瓶中,則實際所配的氫氧化鈉溶液濃度偏高。因此中和鹽酸時消耗氫氧化鈉溶液的體積偏小,測定結果偏低;E、配制NaOH標準溶液時,定容時仰視容量瓶的刻度線,則所配濃度偏低,所以中和鹽酸時消耗氫氧化鈉溶液的體積偏大,測定結果偏高;F、堿式滴定管尖嘴部分有氣泡,滴定后消失,則實際消耗氫氧化鈉溶液的體積偏大,測定結果偏高,所以答案選EF。
可知,由于C標、V待均為定植,所以C測的大小取決于V標的大小,即V標:偏大或偏小,則C測偏大或偏小,據此可以判斷。A、滴定終點讀數時俯視讀數,則讀數偏小,因此消耗氫氧化鈉溶液的體積偏小,測定結果偏低;B、酸式滴定管使用前,水洗后未用待測鹽酸溶液潤洗,則鹽酸被稀釋,濃度降低。因此消耗氫氧化鈉溶液的體積偏小,測定結果偏低;C、錐形瓶水洗后未干燥,不改變溶質的物質的量,不影響結果;D、配制NaOH標準溶液時,沒有等溶解液降至室溫就轉移至容量瓶中,則實際所配的氫氧化鈉溶液濃度偏高。因此中和鹽酸時消耗氫氧化鈉溶液的體積偏小,測定結果偏低;E、配制NaOH標準溶液時,定容時仰視容量瓶的刻度線,則所配濃度偏低,所以中和鹽酸時消耗氫氧化鈉溶液的體積偏大,測定結果偏高;F、堿式滴定管尖嘴部分有氣泡,滴定后消失,則實際消耗氫氧化鈉溶液的體積偏大,測定結果偏高,所以答案選EF。
考點:考查外界條件對平衡狀態的影響;酸堿中和滴定操作、計算、誤差分析


 黃岡課堂作業本系列答案
黃岡課堂作業本系列答案 單元加期末復習先鋒大考卷系列答案
單元加期末復習先鋒大考卷系列答案科目:高中化學 來源: 題型:填空題
2012年11月16日,5名男孩被發現死于貴州省畢節市七星關區街頭垃圾箱內,經當地公安部門初步調查,5名男孩是因在垃圾箱內生火取暖導致CO中毒而死亡。
(1)CO中毒是由于CO與血液中血紅蛋白的血紅素部分反應生成碳氧血紅蛋白,反應的化學方程式可表示為CO+HbO2 O2+HbCO,實驗表明,c(HbCO)即使只有c(HbO2)的
O2+HbCO,實驗表明,c(HbCO)即使只有c(HbO2)的 ,也可造成人的智力損傷。已知t ℃時上述反應的平衡常數K=200,吸入肺部O2的濃度約為1.0×10-2 mol·L-1,若使c(HbCO)小于c(HbO2)的
,也可造成人的智力損傷。已知t ℃時上述反應的平衡常數K=200,吸入肺部O2的濃度約為1.0×10-2 mol·L-1,若使c(HbCO)小于c(HbO2)的 ,則吸入肺部CO的濃度不能超過________mol·L-1。
,則吸入肺部CO的濃度不能超過________mol·L-1。
(2)有如下三個與CO相關的反應:
Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=Q1,平衡常數K1
FeO(s)+CO(g) ΔH=Q1,平衡常數K1
Fe(s)+H2O(g) FeO(s)+H2(g) ΔH=Q2,平衡常數為K2
FeO(s)+H2(g) ΔH=Q2,平衡常數為K2
H2(g)+CO2(g) CO(g)+H2O(g) ΔH=Q3,平衡常數為K3
CO(g)+H2O(g) ΔH=Q3,平衡常數為K3
在不同的溫度下K1、K2、K3的數值如下:
| T/℃ | K1 | K2 | K3 |
| 700 | 1.47 | 2.38 | 0.62 |
| 900 | 2.15 | 1.67 | |
 CO(g)+H2O(g)已經建立的平衡逆向移動,可采取的措施有________。
CO(g)+H2O(g)已經建立的平衡逆向移動,可采取的措施有________。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化學反應原理在科研和生產中有廣泛應用。
(1)利用“化學蒸氣轉移法”制備TaS2晶體,發生如下反應:
TaS2(s)+2I2(g) TaI4(g)+S2(g) (Ⅰ)
TaI4(g)+S2(g) (Ⅰ)
某溫度反應(Ⅰ)的K=4,向某恒容密閉容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡轉化率為 。
(2)如下圖所示,反應(Ⅰ)在石英真空管中進行,先在溫度高(T2)的一端放入未提純的TaS2粉末和少量I2(g),加熱一段時間后,在另一端溫度低(T1)的一端得到了純凈的TaS2晶體,則該正反應的△H 0(填“>”或“<”),上述反應體系中循環使用的物質是 。
(3)上圖為鈉硫高能電池的結構示意圖。該電池的工作溫度為320℃左右,電池反應為2Na + xS=Na2Sx,正極的電極反應式為____________________________。M(由Na2O和Al2O3制得)的兩個作用是________________________________________________和隔離鈉與硫。
(4)寫出Na2S溶液水解的離子方程式_______________________________________,Na2S溶液中c(H+)+ c(Na+)=________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
由于溫室效應和資源短缺等問題,如何降低大氣中的CO2含量并加以開發利用,引起了各國的普遍重視。目前工業上有一種方法是用CO2生產燃料甲醇。一定條件下發生反應: CO2(g)+3H2(g) CH3OH(g)+H2O(g),如圖表示該反應進行過程中能量(單位為kJ·mol-1)的變化。
CH3OH(g)+H2O(g),如圖表示該反應進行過程中能量(單位為kJ·mol-1)的變化。
(1)關于該反應的下列說法中,正確的是 。(填字母)
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)該反應平衡常數K的表達式為 。
(3)溫度降低,平衡常數K (填“增大”、“不變”或“減小”)。
(4)為探究反應原理,現進行如下實驗:在體積為1L的恒容密閉容器中,充入1molCO2和3molH2,測得CO2和CH3OH(g)的濃度隨時問變化如下圖所示。從反應開始到平衡,用氫氣濃度變化表示的平均反應速率v(H2)為 mol·L-1·min-1。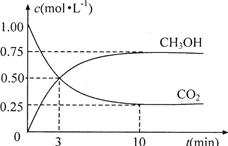
(5)下列措施中能使(4)中n(CH3OH)/n(CO2)增大的有 。(填字母)
A.升高溫度
B.加入催化劑
C.將H2O(g)從體系中分離
D.再充入1molCO2和3molH2
E.充入He(g),使體系總壓強增大
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Ⅰ.在體積恒定的密閉容器中,充入2mol CO2和5mol H2,一定條件下發生反應: CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。測得CO2和CH3OH(g)的濃度隨時間變化如圖所示:
CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。測得CO2和CH3OH(g)的濃度隨時間變化如圖所示: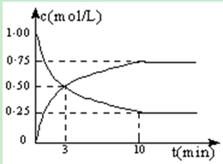
(1)從反應開始到第10min,H2的轉化率為 ,在 該條件下,反應的平衡常數K= ,如果在某一時刻保持溫度不變,只改變濃度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,則平衡 (選填序號)。
a.向正向移動 b.向逆向移動
c.不移動 d.無法確定平衡移動方向
(2)下列措施中能使n(CH3OH)/n(CO2)增大的是 (選填序號)。
a.升高溫度 b.充入He(g),使體系壓強增大
c.將H2O(g)從體系中分離 d.再充入l mol CH3OH(g)
II.熔融碳酸鹽燃料電池(MCFS),發明于1889年。現有一個碳酸鹽燃料電池,以一定比例Li2CO3和Na2CO3低熔混合物為電解質,操作溫度為650℃,在此溫度下以鎳為催化劑,以煤氣(CO、H2的體積比為1:1)直接作燃料,其工作原理如圖所示。請回答下列問題:
(1)A電極的電極反應方程式為 。
(2)常溫下,用石墨作電極,以此電源電解一定量的CuSO4 溶液。當兩極產生的氣體體積相同時停止通電,若電解后溶液的體積為2L,溶液的pH=1(不考慮水解產生的H+),則陽極產生的氣體的物質的量是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業上一般在密閉容器中采用下列反應合成甲醇:CO(g)+2H2(g) 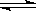 CH3OH(g)
CH3OH(g)
(1)不同溫度下的平衡轉化率與壓強的關系如圖所示。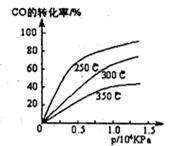
①該反應△H 0,△S 0(填“>”或“<”),則該反 自發進行(填“一定能”、“一定不能”、“不一定”)實際生產條件控制在250℃、l.3×l04kPa左右,選擇此壓強的理由是 。
(2)某溫度下,將2molCO和6molH2充入2L的密閉容器中,充分反應后,達到平衡時測得c(CO)="0.l" mol·L -1。
①該反應的平衡常數K= :
②在其他條件不變的情況下,將容器體積壓縮到原來的1/2,與原平衡相比,下列有關說法正確的是 (填序號)。
| A.氫氣的濃度減少 |
| B.正反應速率加快,逆反應速率也加快 |
| C.甲醇的物質的量增加 |
| D.重新平衡時n(H2)/n(CH3OH)增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
二甲醚是一種重要的清潔燃料,可替代氟利昂作制冷劑,對臭氧層無破壞作用。工業上可利用水煤氣合成二甲醚,其反應為:3H2(g)+3CO(g)  CH3OCH3(g)+CO2(g) ΔH<0
CH3OCH3(g)+CO2(g) ΔH<0
(1)在一定條件下的密閉容器中,該反應達到平衡后,只改變一個條件能同時提高反應速率和CO的轉化率的是________(填字母代號,下同)。
a.降低溫度 b.加入催化劑
c.縮小容器體積 d.減少CO2的濃度
(2)若反應在體積恒定的密閉容器中進行,下列能判斷反應已達平衡狀態的是________
a.3V正(CO2)=V逆(CO) b.生成a mol CO2的同時消耗3a mol H2
c.氣體的密度不再改變 d.混合氣體的平均相對分子質量不變
(3)300℃時,在體積為2L的容器中充入4 mol H2、6 mol CO。5min時,反應恰好達平衡,此時H2的轉化率為75%。
① 5min時V(CO)=_________mol/(L·min)。該溫度下,此反應的平衡常數為:_______
② 保持溫度不變,在以上已達反應平衡的容器中,將每種物質同時增加1mol,則此時平衡將_______移動(填“正向”、“逆向”、“不”)
(4).下圖中,甲裝置為CH3OCH3、O2、KOH三者構成的燃燒電池,其電極均為Pt電極。裝置乙中,C、D電極為Pb電極,其表面均覆蓋著PbSO4,其電解液為稀H2SO4溶液。
① 寫出甲裝置中A極的電極反應式___________________________________________
② 寫出乙裝置中C極的電極反應式___________________________________________
③ 當有23克甲醚參加反應時,D電極的質量變化為______克。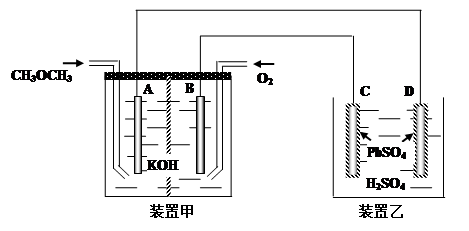
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知重鉻酸鉀(K2Cr2O7)是一種主要的的無機試劑。
(1)強氧化性的K2Cr2O7溶液中,存在如下平衡: Cr2O72-(橙色)+H2O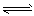 2CrO42-(黃色)+2H+,
2CrO42-(黃色)+2H+,
①若要使溶液的橙色加深,下列可采用的方法是 。
| A.加入適量稀鹽酸 | B.加入適量稀硫酸 | C.加入適量燒堿固體 | D.加水稀釋。 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某學生為了探究鋅與鹽酸反應過程中速率變化。在100mL稀鹽酸中加入足量的鋅粉,標準狀況下測得數據累計值如下:
| 時間(min) | 1 | 2 | 3 | 4 | 5 |
| 氫氣體積(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com