
由于溫室效應和資源短缺等問題,如何降低大氣中的CO2含量并加以開發(fā)利用,引起了各國的普遍重視。目前工業(yè)上有一種方法是用CO2生產(chǎn)燃料甲醇。一定條件下發(fā)生反應: CO2(g)+3H2(g) CH3OH(g)+H2O(g),如圖表示該反應進行過程中能量(單位為kJ·mol-1)的變化。
CH3OH(g)+H2O(g),如圖表示該反應進行過程中能量(單位為kJ·mol-1)的變化。
(1)關于該反應的下列說法中,正確的是 。(填字母)
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)該反應平衡常數(shù)K的表達式為 。
(3)溫度降低,平衡常數(shù)K (填“增大”、“不變”或“減小”)。
(4)為探究反應原理,現(xiàn)進行如下實驗:在體積為1L的恒容密閉容器中,充入1molCO2和3molH2,測得CO2和CH3OH(g)的濃度隨時問變化如下圖所示。從反應開始到平衡,用氫氣濃度變化表示的平均反應速率v(H2)為 mol·L-1·min-1。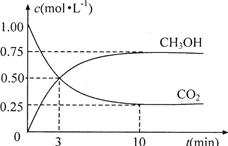
(5)下列措施中能使(4)中n(CH3OH)/n(CO2)增大的有 。(填字母)
A.升高溫度
B.加入催化劑
C.將H2O(g)從體系中分離
D.再充入1molCO2和3molH2
E.充入He(g),使體系總壓強增大
(1)C (2)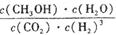 (3)增大(4) 0.225 (5)CD
(3)增大(4) 0.225 (5)CD
解析試題分析:(1)由方程式可知:氣體的物質的量減少,△S<0;由題圖可知:生成物的能量比反應物低,則△H<0。故選項為:C。(2)該反應平衡常數(shù)K的表達式為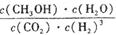 。(3)由于該反應的正反應是放熱反應。溫度降低,化學平衡向正反應方向移動,平衡常數(shù)K增大。(4)由圖-2可知:反應進行到10min時達到平衡。此時C(CH3OH)=0.75mol/L,則V(CH3OH)= ΔC(CH3OH)/Δt= 0.75mol/L÷10min =0.075mol/( L·min). v(H2)=3V(CH3OH)= 0.225 mol/( L·min). (5)A.根據(jù)化學平衡移動原理,升高溫度化學平衡向吸熱方向即逆反應方向移動,n(CH3OH)/n(CO2)減小。錯誤。B.加入催化劑對化學平衡無影響,n(CH3OH)/n(CO2)不變。錯誤。C.將H2O(g)從體系中分離,減小生成物的濃度,平衡向正反應方向移動,n(CH3OH)/n(CO2)增大。正確。D.再充入1molCO2和3molH2。增大反應物的濃度,化學平衡向正反應方向移動,n(CH3OH)/n(CO2)增大。正確。E.充入He(g),使體系總壓強增大,由于不能使反應混合物的濃度改變,所以n(CH3OH)/n(CO2)不變。錯誤。正確選項為:C D。
。(3)由于該反應的正反應是放熱反應。溫度降低,化學平衡向正反應方向移動,平衡常數(shù)K增大。(4)由圖-2可知:反應進行到10min時達到平衡。此時C(CH3OH)=0.75mol/L,則V(CH3OH)= ΔC(CH3OH)/Δt= 0.75mol/L÷10min =0.075mol/( L·min). v(H2)=3V(CH3OH)= 0.225 mol/( L·min). (5)A.根據(jù)化學平衡移動原理,升高溫度化學平衡向吸熱方向即逆反應方向移動,n(CH3OH)/n(CO2)減小。錯誤。B.加入催化劑對化學平衡無影響,n(CH3OH)/n(CO2)不變。錯誤。C.將H2O(g)從體系中分離,減小生成物的濃度,平衡向正反應方向移動,n(CH3OH)/n(CO2)增大。正確。D.再充入1molCO2和3molH2。增大反應物的濃度,化學平衡向正反應方向移動,n(CH3OH)/n(CO2)增大。正確。E.充入He(g),使體系總壓強增大,由于不能使反應混合物的濃度改變,所以n(CH3OH)/n(CO2)不變。錯誤。正確選項為:C D。
考點:考查CO2的綜合利用、化學平衡常數(shù)的表達、計算及外界條件對化學平衡的影響的知識。


科目:高中化學 來源: 題型:填空題
(1)(浙江高考)對于氣相反應,用某組分(B)的平衡壓強(pB)代替物質的量濃度(cB)也可表示平衡常數(shù)(記作Kp),則反應CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=206.2 kJ·mol-1的Kp=________,隨著溫度的升高,該平衡常數(shù)________(填“增大”“減小”或“不變”)。
CO(g)+3H2(g) ΔH=206.2 kJ·mol-1的Kp=________,隨著溫度的升高,該平衡常數(shù)________(填“增大”“減小”或“不變”)。
(2)(天津高考)寫出WO3(s)+3H2(g)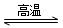 W(s)+3H2O(g)的化學平衡常數(shù)表達式為________。
W(s)+3H2O(g)的化學平衡常數(shù)表達式為________。
(3)(福建高考)在恒容絕熱(不與外界交換能量)條件下進行2A(g)+B(g)??2C(g)+D(s)反應,按下表數(shù)據(jù)投料,反應達到平衡狀態(tài),測得體系壓強升高。簡述該反應的平衡常數(shù)與溫度的變化關系:________。
| 物質 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在容積為1 L的密閉容器中,進行如下反應:A(g)+2B(g) 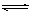 C(g)+D(g),在不同溫度下,D的物質的量n(D)和時間t的關系如圖。
C(g)+D(g),在不同溫度下,D的物質的量n(D)和時間t的關系如圖。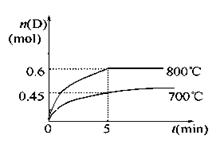
請回答下列問題:
(1)700℃時,0~5min內(nèi),以B表示的平均反應速率為_________。
(2)能判斷反應達到化學平衡狀態(tài)的依據(jù)是__________。
A.容器中壓強不變
B.混合氣體中c(A)不變
C.v正(B)=2v逆(D)
D.c(A)=c(C)
(3)若最初加入1.0 mol A和2.2 mol B,利用圖中數(shù)據(jù)計算800℃時的A的轉化率 。
(4)800℃時,某時刻測得體系中物質的量濃度如下:c(A)=0.06 mol/L,c(B)=0.50 mol/L,c(C)=0.20 mol/L,c(D)=0.018 mol/L,則此時該反應 (填“向正方向進行”、“向逆方向進行”或“處于平衡狀態(tài)”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知2A2(g) + B2(g) 2C(g)
2C(g)  H=" -a" kJ/mol(a>0),在一個有催化劑的固定容積的密閉容器中加入2molA2和1molB2,在500℃是充分反應達到平衡后C的濃度為w mol/L,放出熱量b kJ。
H=" -a" kJ/mol(a>0),在一個有催化劑的固定容積的密閉容器中加入2molA2和1molB2,在500℃是充分反應達到平衡后C的濃度為w mol/L,放出熱量b kJ。
(1)a b(填“>”“=”或“<”)。
(2)若將反應溫度升高到700℃,該反應的平衡常數(shù)將 (填“增大”“減小”或“不變”)。
(3)若在原來的容器中,只加入2mol C,500℃時充分反應達到平衡后,吸收熱量c kJ,C的濃度 w mol/L(填“>”“=”或“<”),a,b,c之間滿足何種關系: (用等式表示)。
(4)能說明該反應已經(jīng)達到平衡的狀態(tài)的是 。
a.ν(C)=2ν(B2) b.容器內(nèi)壓強保持不變
c.ν(逆)(A2)=ν(正)(B2) d.容器內(nèi)的密度保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
甲醇被稱為2l世紀的新型燃料,工業(yè)上通過下列反應I和II,用CH4和H2O為原料來制備甲醇:
CH4(g)+H2O(g) 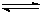 CO(g)+3H2 (g)……I CO(g)+2H2(g)
CO(g)+3H2 (g)……I CO(g)+2H2(g) 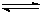 CH3OH(g) ……II。
CH3OH(g) ……II。
(1)將1.0 mol CH4和2.0 mol H2O(g)通入容積為100L反應室,在一定條件下發(fā)生反應I,CH4的平衡轉化率與溫度、壓強的關系如圖。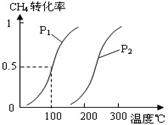
①已知100℃時達到平衡所需的時間為5min,則用H2表示的平均反應速率為____________________。
②圖中的P1_________P2(填“<”、“>”或“=”),100℃時平衡常數(shù)的值為__________ 。
(2)在壓強為0.1 MPa條件下, 將a mol CO與 3a mol H2的混合氣體在催化劑作用下,自發(fā)反應Ⅱ,生成甲醇。
③該反應的△H ____ 0;若容器容積不變,下列措施可增加甲醇產(chǎn)率的是________。
| A.升高溫度 | B.將CH3OH(g)從體系中分離 |
| C.充入He,使體系總壓強增大 | D.再充入1mol CO和3mol H2 |
| 實驗編號 | T(℃) | N(CO)/n(H2) | P(Mpa) |
| i | 150 | 1/3 | 0.1 |
| ii | | | 5 |
| iii | 350 | | 5 |
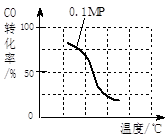
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Ⅰ.(4分)在一體積為10L密閉的容器中,通入一定量的CO和H2O(g),在850℃時發(fā)生如下反應:CO(g)+H2O(g)  CO2(g)+H2(g) △H<0
CO2(g)+H2(g) △H<0
(1)CO和H2O濃度變化如圖,則0~4 min的平均反應速率ν(CO)=_______ mol/(L·min),此時該反應的平衡常數(shù)為 。 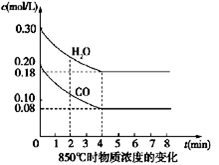
(2)當下列哪些物理量不再發(fā)生變化時,表明上述反應已達到平衡狀態(tài)的是 。
| A.混合氣體的壓強 |
| B.混合氣體的密度 |
| C.CO的物質的量濃度 |
| D.密閉容器中放出熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Ⅰ. 在水溶液中橙紅色的Cr2O72-與黃色的CrO42-有下列平衡關系:
Cr2O72-+H2O  2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液后,溶液呈 色,因為 。
(2)向已加入NaOH溶液的(1)中再加入過量稀H2SO4后,則溶液呈 色,因為 。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4為黃色沉淀)則平衡向 方向移動,溶液顏色將 。(填“變深”、“變淺”或“不變”)
Ⅱ.實驗室有一未知濃度的稀鹽酸,某學生為測定鹽酸的濃度在實驗室中進行如下實驗:
1.配制100mL 0.10mol/L NaOH標準溶液。
2.取20.00mL待測稀鹽酸溶液放入錐形瓶中,并滴加2~3滴酚酞作指示劑,用自己配制的標準NaOH溶液進行滴定。
3.重復上述滴定操作2~3次,記錄數(shù)據(jù)如下。
| 實驗編號 | NaOH溶液的濃度 (mol/L) | 滴定完成時,NaOH溶液滴入的體積(mL) | 待測鹽酸溶液的體積 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.58 | 20.00 |
| 3 | 0.10 | 22.60 | 20.00 |



查看答案和解析>>
科目:高中化學 來源: 題型:填空題
用氮化硅(Si3N4)陶瓷代替金屬制造發(fā)動機的耐熱部件, 能大幅度提高發(fā)動機的熱效率。工業(yè)上用化學氣相沉積法制備氮化硅, 其反應如下: 3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) ΔH <0
Si3N4(s)+12HCl(g) ΔH <0
完成下列填空:
(1)在一定溫度下進行上述反應, 若反應容器的容積為2 L, 3 min后達到平衡, 測得固體質量增加了2. 80 g, 則轉移電子的物質的量為 ,H2的平均反應速率為 mol/(L·min); 該反應的平衡常數(shù)表達式K= 。
(2)上述反應達到平衡后, 下列說法正確的是 。
a. 其他條件不變, 壓強增大, 平衡常數(shù)K減小
b. 其他條件不變, 溫度升高, 平衡常數(shù)K減小
c. 其他條件不變, 增大Si3N4物質的量,平衡向左移動
d. 其他條件不變, 增大HCl物質的量,平衡向左移動
(3)一定條件下, 在密閉恒容的容器中, 能表示上述反應達到化學平衡狀態(tài)的是 。
| A.3v逆(N2)=v正(H2) | B.v正(HCl)=4v正(SiCl4) |
| C.混合氣體密度保持不變 | D.c(N2)∶c(H2)∶c(HCl)=1∶3∶6 |
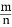 , 保持其他條件不變, 降低溫度后達到新的平衡時, H2和HCl的物質的量之比
, 保持其他條件不變, 降低溫度后達到新的平衡時, H2和HCl的物質的量之比 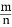 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
300℃時,將2mol A和2mol B兩種氣體混合于2L密閉容器中,發(fā)生如下反應:3A(g)+B(g) 2C(g)+2D(g) △H,2min末達到平衡,生成0.8mol D。
2C(g)+2D(g) △H,2min末達到平衡,生成0.8mol D。
(1)在2min末時,A的平衡濃度為_____________,B的轉化率___________,0-2min內(nèi)D的平均反應速率為_____________。
(2)該反應的平衡常數(shù)表達式為:K=_____________。該溫度下的化學平衡常數(shù)數(shù)值為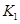 =____________。
=____________。
已知350℃時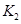 =l,則△H________0(填“>”或“<”)。
=l,則△H________0(填“>”或“<”)。
(3)在300℃時,將該反應容器壓縮體積為lL。則A的轉化率___________(填“增大”、“減小”或“不變”),原因是__________________。該條件下的平衡常數(shù)為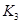 。 則K3________
。 則K3________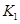 ,(填“<”或“>”或“=”)。原因是_______________________。
,(填“<”或“>”或“=”)。原因是_______________________。
(4)能判斷該反應是否達到化學平衡狀態(tài)的依據(jù)是__________________(多選扣分)。
A.容器中壓強不變 B.混合氣體中c(A)不變
C.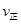 (A)=
(A)=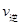 (C) D.混合氣體密度不變
(C) D.混合氣體密度不變
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com