
純堿是主要的化工原料,化學家發明了其不同的工業制法,其中法國化學家尼古拉斯·勒布朗早在1791年發明的工業合成碳酸鈉的方法,簡稱勒布朗制堿法。該方法包括以下兩個階段:首先從原料氯化鈉與濃硫酸在高溫下的反應得到中間產物硫酸鈉,然后通過硫酸鈉與木炭和碳酸鈣的反應來得到碳酸鈉。各步驟反應的化學方程式如下:
2NaCl+H2SO4 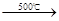 Na2SO4+2HCl↑
Na2SO4+2HCl↑
Na2SO4+2C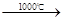 Na2S+2CO2↑
Na2S+2CO2↑
Na2S+CaCO3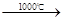 Na2CO3+CaS
Na2CO3+CaS
完成下列計算(計算過程保留3位有效數字)
(1)假設每一步反應物的量足夠,反應完全,理論上每獲得1kg純度為80%的純堿需要氯化鈉的的質量是_________kg。
(2)步驟②碳單質過量時也同樣可以反應獲得Na2S,此時所發生的反應的化學方程式是___________________________________。若其它條件不變,步驟②按此反應進行,每獲得1kg純度為80%的純堿需要氯化鈉的的質量是__________kg,此時消耗碳單質的量是原步驟②反應用碳量的____倍。
(3)通過定性分析,勒布朗制堿法獲得的純堿含有雜質CaCO3和CaS,為了測定產品純度,取10g樣品與稀硝酸反應,硫元素全部轉化成淡黃色固體,稱量其質量為0.16g,另取10g樣品與稀鹽酸反應,得到氣體(忽略氣體在水中的溶解),折算為標況下,體積為2.162L,計算求出該產品中Na2CO3的純度。
(4)若除氯化鈉和碳單質的量外,其它反應物足量,反應充分, 如果加入amol氯化鈉時,生成的Na2CO3為yg,電子轉移數為zmol,討論分析當氯化鈉與碳的物質的量之比x的值不同時,用函數式表示y和z的值是多少。
| x | y | z |
| | | |
| | | |
| | | |
(1)0.883(2分)
(2)Na2SO4+4C  Na2S + 4CO↑, 0.883 , 2 (1分+1分+分)
Na2S + 4CO↑, 0.883 , 2 (1分+1分+分)
(3)86.6% (5分)
(4)(每空1分)x y z x>1 53a/x 4a/x x≤1 53a 4a
解析試題分析:(1)根據Na元素守恒可得對應關系:2NaCl ~ Na2CO3,m(NaCl)=1kg×80%×117÷106=0.883kg。
(2)過量的C生成CO。配平可得化學方程式;Na元素守恒,需要的NaCl的質量不變,仍然是0.883kg;對比化學方程式,可知C的用量為原來的2倍。
(3)CaS的物質的量等于S,m(CaS)=0.16g÷32g/mol×72g/mol=0.36g,CaCO3、Na2CO3的質量和=10g-0.36g=9.64g,CaCO3、Na2CO3的物質的量和等于CO2的物質的量,m(CaCO3)="2.162L÷22.4L/mol" — 0.16g÷32g/mol =0.092mol,則m(Na2CO3)÷106g/mol +【9.64g—m(Na2CO3)】÷110g/mol=0.092mol,得m(Na2CO3)=8.86g,進而得Na2CO3的純度為86.6%。
(4)x≤1,C足量,根據2NaCl ~ Na2CO3,m(Na2CO3)= a÷2×106=53a,只有反應②為氧化還原反應,S元素由+4價變為0價,所以轉移電子物質的量為4a;x>1時,C不足,應根據C的物質的量進行計算,n(C)= a/xmol,m(Na2CO3)= ax÷2×106=53a/x,轉移電子物質的量為4a/x。
考點:本題考查化學計算、化學方程式的書寫。


 全優點練單元計劃系列答案
全優點練單元計劃系列答案科目:高中化學 來源: 題型:計算題
把5.1 g鋁鎂合金的粉末放入100 mL某鹽酸中,恰好完全反應得到標準狀況下氫氣5.6 L。試計算:(寫出計算過程)
(1)該鹽酸的物質的量濃度;
(2)該合金中鋁的質量分數。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
無機非金屬材料、金屬材料和有機高分子材料并稱為三大材料,是發展高新技術的基石,在未來科技發展中發揮著重要的作用。
(1)新型材料α-Fe粉具有超強的磁性能,用作高密度磁記錄的介質以及高效催化劑等。將5.60 g α-Fe粉與一定量水蒸氣在高溫下反應一定時間后冷卻,其質量變為6.88 g。
①產生的氫氣的體積為_________mL(標準狀況下)。
②將冷卻后的固體物質放入足量FeCl3溶液中充分反應(已知Fe3O4不溶于FeCl3溶液),計算最多消耗FeCl3的物質的量 mol。
(2)Nierite是一種高熔點高硬度的陶瓷材料。Nierite的摩爾質量為140 g/mol,其中硅元素的質量分數為60%。已知1 mol NH3與足量的化合物T充分反應后可得到35 g Nierite與3 mol HCl氣體。
Nierite的化學式為___________。T的化學式為____________。
(3)K金是常見的貴金屬材料,除黃金外,還含有銀、銅中的一種或兩種金屬。為測定某18K金樣品的組成,將2.832 g樣品粉碎后投入足量的濃硝酸中,充分溶解后,收集到NO2和N2O4的混合氣體224 mL(折算至標準狀況,下同),將該混合氣體與84 mL O2混合后緩緩通入水中,恰好被完全吸收。
①混合氣體的平均摩爾質量為______________。
②填寫該18K金的成分表(精確至0.01%,若不含該金屬則填0)。
| 18K金成分 | Au | Ag | Cu |
| 含量(質量分數) | 75.00% | _________ | _________ |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
將128 g銅置入一定量的濃硝酸中,并微熱,隨著銅的不斷減少,反應生成的氣體顏色逐漸變淺,當銅反應完畢時(銅片完全消失),共收集到NO2和NO的混合氣體44.8 L氣體(標準狀況),求:
(1)寫出上述過程中,有關反應的化學方程式(4分)。
______________________________________________________、
______________________________________________________。
(2)完成該反應至少需要量取10mol/L的濃硝酸_________mL(4分)。
(3)求混合氣體中NO2、NO的體積(6分,請寫出計算步驟)。
(4)將收集上述氣體的容器倒扣在盛有水的水槽中,并向其中緩慢通入O2,使其充分反應,若要使水恰好充滿容器,求理論上需要參加反應的O2的物質的量(4分,請寫出計算步驟)。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
(1)NA為阿伏加德羅常數。25℃時,1g水中含H+離子個數約為__________NA。
(2)通過氨的催化氧化法制取硝酸,在此全過程中,理論上氨與所耗氧氣的物質的量比為__________,這樣所得硝酸的質量分數為_____________。
(3)往含0.2 mol NaOH和0.1 mol Ca(OH)2的混合溶液中持續穩定地通入CO2氣體0.5 mol。請以CO2的量為橫坐標,以溶液中離子的總量為橫坐標,畫出離子總量隨CO2加入量變化的折線圖。(不計弱電解質的電離和鹽的水解)
(4)某研究性學習小組擬用銅屑與氧化銅混合物與硫酸和硝酸組成的混酸反應來制取CuSO4·5H2O晶體,混酸中硝酸的還原產物為NO,反應過程中不產生SO2,反應后的溶液中不含Cu(NO3)2, 反應中固體完全溶解,兩種酸均恰好完全反應。設固體混合物的總質量為480 g,其中銅屑的質量分數為0.4, 480g固體混合物與一定量混酸微熱后,充分反應,冷卻恰好只得到CuSO4·5H2O,試求原混酸中H2SO4的質量分數(寫出計算過程)
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
鐵鋁合金是一種新型高溫結構材料。
(1)圖9表示室溫時不同組份的Fe3Al在65%濃HNO3 中的腐蝕情況。由圖9可看出添加了 (填符號)元素的合金耐蝕性最差。
(2)高溫條件下,Al和Fe2O3按一定比例混合反應可制
|
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
氯化鈉溶液在生產、生活中都有廣泛的用途。現配置1 L 0.2 mol·L-1 NaCl溶液,請回答問題。
| 實驗步驟 | 有關問題 |
| (1)計算并稱量 | 用托盤天平稱量NaCl固體的質量為 g |
| (2)溶解 | 為加速溶解,可進行的操作是 |
(3)轉移 | 指出示意圖中的兩處錯誤: 錯誤1: 錯誤2: |
| (4)洗滌 | 用少量蒸餾水洗滌 2~3次,并將洗滌液轉移到容量瓶中 |
| (5)定容 | 若俯視容量瓶刻度線,定容后會造成所配溶液的物質的量濃度 (填“偏高”“偏低”或“無影響”) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
“化學是人類進步的關鍵”。下列說法不正確的是 ( )
| A.PM2.5是指空氣中直徑≤2.5 μm的固體顆粒或液滴的總稱 |
| B.根據分散質粒子的直徑大小,分散系可分為溶液、濁液和膠體,濁液的分散質粒子大小介于溶液與膠體之間 |
| C.科學家發現一種新細菌的DNA鏈中有砷(As)元素,該As元素最有可能取代了普通DNA鏈中的P元素 |
D.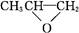 和CO2反應生成可降解聚合物 和CO2反應生成可降解聚合物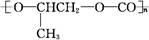 ,該反應符合綠色化學的原則 ,該反應符合綠色化學的原則 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com