
【題目】設NA為阿伏加德羅常數的值,下列敘述中正確的是( )
A. 1 L 1 mol/L的Na2CO3溶液中含有的CO32-數目為![]()
B. 常溫常壓下,8 g O2含有的電子數是4NA
C. 標準狀況下,2.24 L CCl4中含有的分子數為0.1NA
D. 25℃時,1 L pH=13的 Ba(OH)2溶液中含有的OH-數目為0.2![]()
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】H5IO6(正高碘酸)是用于光度法測定苯肼的試劑。工業上用NaIO3制備H5IO6的流程如圖:
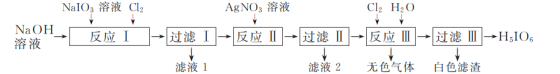
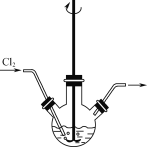
(1)“反應Ⅰ”可在如圖所示的裝置中進行。該反應生成不溶于水的Na2H3IO6的離子方程式為____。若要提高Cl2的利用率,可對裝置進行改進的措施為___。
(2)反應Ⅱ生成不溶于水的黑色Ag5IO6,“濾液2”呈__(填“酸”“堿”或“中”)性。
(3)“無色氣體”為__(填化學式)。
(4)工業上為降低成本,減少對環境的污染,整個流程需要控制加入Cl2和AgNO3的物質的量之比為n(Cl2)∶n(AgNO3)=__。
(5)H5IO6具有強氧化性,可將FeSO4氧化為H2FeO4,自身被還原為HIO3,該反應的化學方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈣和銅合金可用作電解制鈣的陰極電極材料,回答下列問題:
(1)基態銅原子的價電子排布式為_________________。
(2)CaCO3高溫分解可制得CaO。CaO與 C 在一定條件下可生成CaC2,CaC2與水反應生成 Ca(OH)2和一種 4 原子氣體分子。
①CaCO3中陰離子的空間構型為______________。
②該氣體分子中 σ 鍵與π鍵的數目之比為_____________。
③寫出 2 種與 ![]() 互為等電子體的分子的化學式______________。
互為等電子體的分子的化學式______________。
(3)工業上電解 CaCl2制Ca而不采用電解 CaO 的原因是_______________。
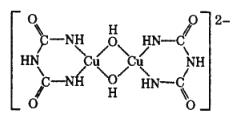
(4)在堿性溶液中,縮二脲 HN( CONH2)2與 CuSO4反應得到一種特征紫色物質,其結構如圖所示,該反應原理可用于檢驗蛋白質或其他含鍵的化合物。縮二脲分子中碳原子與氮原子的雜化類型分別為__________、________。
(5)一種鈣銅合金的結構可看作圖a、b 兩種原子層交替堆積排列而成c,其晶胞如圖d。
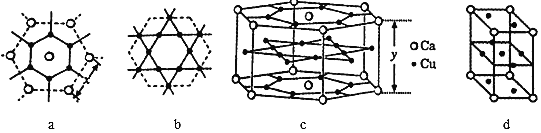
①a圖Ca-Ca 間距離為x pm,c圖中Ca-Ca間距離為y pm。已知原子擁有的盡可能多的相鄰原子的個數叫該原子的配位數,則晶胞c中Ca原子的配位數(Cu原子)為_______。
②設阿伏加德羅常數的值為 NA,則該鈣銅合金的密度是_______gcm-3(列出計算表達式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家開發出一種低成本光伏材料—蜂窩狀石墨烯。生產原理是Na2O+2CO  Na2CO3+C(石墨烯),然后除去Na2CO3,即可制得蜂窩狀石墨烯。下列說法不正確的是( )
Na2CO3+C(石墨烯),然后除去Na2CO3,即可制得蜂窩狀石墨烯。下列說法不正確的是( )
A.該生產石墨烯的反應屬于氧化還原反應
B.石墨烯與金剛石互為同素異形體
C.Na2O屬于堿性氧化物,CO屬于酸性氧化物,Na2CO3屬于鹽
D.自然界中鈉元素以化合態形式存在
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碲(Te)元素是當今新材料的主要成分之一。工業上從電解法精煉銅的陽極泥中提取純度較高的碲,經預處理后的陽極泥中含TeO2及鐵、鉛、銅的化合物等,通過以下流程得到:

已知:①TeO2是兩性氧化物,微溶于水,可溶于強酸或強堿。
②部分難溶物的Ksp如表:
化合物 | Fe(OH)2 | Pb(OH)2 | Cu(OH)2 | FeS | PbS | CuS |
Ksp | 8×10-16 | 1.2×10-15 | 1.3×10-20 | 4×10-19 | 1×10-28 | 6×10-36 |
回答下列問題:
(1)“堿浸”時TeO2發生反應的化學方程式為___________。
(2)加入Na2S溶液的主要目的是___________。
(3)“沉碲”發生反應的化學方程式為_______。
(4)“酸溶”后,將SO2通入溶液中進行“還原”得到粗碲,該反應的化學方程式是___________。
(5)電解法提純粗碲時,以Na2TeO3溶液為電解質溶液,陽極材料為___________。電解過程中陰極的電極反應式為___________。
(6)常溫下,向0.lmol/LNa2TeO3溶液中滴加鹽酸,當溶液pH=5時,溶液中c(TeO32-):c(H2TeO3)=___________。(已知:H2TeO3的Ka1=1.0×10-3Ka2=2.0×10-8)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過氧化氫俗名雙氧水,醫療上利用它有殺菌消毒作用來清洗傷口.關于雙氧水,回答下列問題:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反應中,不屬于氧化還原反應的是__________(填代號,下同),H 2 O 2 僅體現還原性的反應是__________。
(2)上述反應說明H2O2 、Ag2O、K2CrO 4 氧化性由強到弱的順序是_________________
(3)某強酸反應體系中發生的一個氧化還原的離子反應,反應物和生成物共六種微粒:O2、MnO4— 、H2O、Mn2+ 、H2O2 、H+ 。已知該反應中H2O2 只發生了如下過程:H2O2 →O2。
①反應體系選擇的酸是:____________ A.鹽酸 B.硫酸 C醋酸
②該反應的離子方程式為________________________________________。
③如果上述反應中有2.24L(標準狀況)氣體生成,轉移的電子為 _______mol.
(4)H2O2 有時可作為礦業廢液消毒劑,有“綠色氧化劑”的美稱;如消除采礦業膠液中的氰化物(如KCN),經以下反應實驗:KCN+H2O2 +H2O=A+NH3↑,試指出生成物A的化學式為_____________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室需要0.5 mol/L H2SO4溶液500 mL。根據溶液的配制情況回答下列問題:

(1)如圖所示的儀器中配制溶液肯定不需要的是________(填序號)。
(2)下列操作中,500ml容量瓶所不具備的功能有________(填序號)。
A.配制一定體積準確濃度的標準溶液 B.長期貯存溶液
C.用來加熱溶解固體溶質 D.量取220 mL溶液
(3)實驗中,其他操作均正確,若定容時仰視刻度線,則所配制溶液的濃度將____ 0.5mol/L(填“大于”“等于”或“小于”,下同)。若溶液未冷卻即轉移至容量瓶定容,則所配制溶液濃度將________0.5 mol/L。
(4)根據計算得知:所需質量分數為98%、密度為1.84 g/cm3的濃硫酸的體積為________mL(計算結果保留一位小數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃時,向Na2CO3溶液中滴入鹽酸,混合溶液的pH與離子濃度變化的關系如圖所示。

已知:lg X=lg c(CO32-)/c(HCO3-)或lg c(HCO3-)/c(H2CO3),下列敘述正確的是( )
A. 曲線m表示pH與c(HCO3-)/c(H2CO3)的變化關系
B. 當溶液呈中性時,c(Na+)=c(HCO3-)+2c(CO32-)
C. Ka1(H2CO3)=1.0×10-6.4
D. 25 ℃時,CO32-+H2O![]() HCO3-+OH-的平衡常數為1.0×10-7.6
HCO3-+OH-的平衡常數為1.0×10-7.6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酰氯(ClNO)是有機合成中的重要試劑,可由NO與Cl2在通常條件下反應得到,化學方程式為2NO(g)+Cl2(g)![]() 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物與懸浮在大氣中的海鹽粒子相互作用時會生成亞硝酰氯,涉及如下反應:① 2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)
NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)![]() 2ClNO(g) K3,則K1、K2、K3之間的關系為K3=_______________(用K1和K2表示);
2ClNO(g) K3,則K1、K2、K3之間的關系為K3=_______________(用K1和K2表示);
(2)已知幾種化學鍵的鍵能數據如下表:(亞硝酰氯的結構為Cl—N==O)
化學鍵 | N≡O | Cl-Cl | Cl-N | N==O |
鍵能/(kJ·mol-1) | 630 | 243 | a | 607 |
則2NO(g)+Cl2(g)![]() 2ClNO(g)的反應的 △H和a的關系為 △H = ___kJ·mol-1。
2ClNO(g)的反應的 △H和a的關系為 △H = ___kJ·mol-1。
(3)300℃時,2NO(g)+Cl2 (g)![]() 2ClNO(g)的正反應速率表達式為v正 = k·cn (ClNO),測得速率和濃度的關系如下表:
2ClNO(g)的正反應速率表達式為v正 = k·cn (ClNO),測得速率和濃度的關系如下表:
序號 | c(ClNO)/(mol·L-1) | v/(mol·L-1·s-l) |
① | 0. 30 | 3. 60×10-9 |
② | 0. 60 | 1. 44×10-8 |
③ | 0. 90 | 3. 24×10-8 |
n = ___;k = ____。
(4)若向絕熱恒容密閉容器中充入物質的量之比為2 : 1的NO和Cl2進行反應2NO(g)+Cl2(g)![]() 2ClNO(g),能判斷反應已達到化學平衡狀態的是__(填標號)。
2ClNO(g),能判斷反應已達到化學平衡狀態的是__(填標號)。
a.容器中的壓強不變 b.2v正(NO) = v逆(Cl2)c.氣體的平均相對分子質量保持不變 d.該反應平衡常數保持不變e.NO和Cl2的體積比保持不變
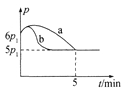
(5)25℃時,向體積為2 L且帶氣壓計的恒容密閉容器中通入0.08 mol NO和0.04 mol Cl2發生反應:2NO(g)+Cl2 (g)![]() 2ClNO(g)△H。
2ClNO(g)△H。
①若反應起始和平衡時溫度相同,測得反應過程中壓強(p)隨時間(t)的變化如圖甲曲線a所示,則 △H __(填“>”“<”或“不確定”)0;若其他條件相同,僅改變某一條件時,測得其壓強(p)隨時間(t)的變化如圖甲曲線b所示,則改變的條件是______。
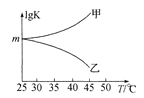
②圖是甲、乙同學描繪上述反應平衡常數的對數值(lg K)與溫度的變化關系,其中正確的曲線是____(填“甲”或“乙”),m值為_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com