
【題目】有關藥品的保存和使用不正確的是( )
A.溴水盛于帶磨砂玻璃塞的細口瓶中
B.硫酸銅粉末、氯化鈣等藥品應貯存于干燥器中
C.白磷浸入水中密封保存
D.用碳酸鈉滴定未知濃度的鹽酸,碳酸鈉盛于酸式滴定管中
科目:高中化學 來源: 題型:
【題目】某課外學習小組對日常生活中不可缺少的調味品M進行探究.已知C可在D中燃燒發出蒼白色火焰.M與其他物質的轉化關系如圖1所示(部分產物已略去): 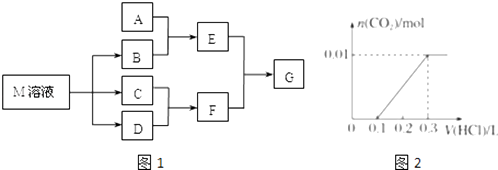
(1)寫出用惰性電極電解M溶液的離子方程式 . 寫出F的電子式 .
(2)若A是一種常見的酸性氧化物,且可用于制造玻璃,E溶液與F溶液反應可以制備一種膠體,則E溶液的俗稱是 .
(3)若A是CO2氣體,A與B溶液能夠反應,反應后所得的溶液再與鹽酸反應,如圖2所示,“則A與B溶液”反應后溶液中的溶質化學式為 .
(4)若A是一種化肥.實驗室可用A和B反應制取氣體E,E與F、E與D相遇均冒白煙,且利用E與D的反應檢驗輸送D的管道是否泄露,寫出E與D反應的化學方程式是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組物質的晶體中,化學鍵類型、晶體類型都相同的是( )
A.CO2和SiO2B.H2S和H2OC.NaCl和HClD.CF2Cl2和CH3COONa
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時加水稀釋10mL pH=11的氨水,下列判斷正確的是( )
A.原氨水的濃度為10﹣3mol?L﹣1
B.溶液中 ![]() 減小
減小
C.氨水的電離程度增大,溶液中所有離子的濃度均減小
D.再加入10 mL pH=3的鹽酸充分反應后混合液的pH值肯定大于7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于反應3Cl2+6NaOH==5NaCl+NaClO3+3H2O,以下敘述正確的是( )
A. Cl2是氧化劑,NaOH是還原劑
B. 被氧化的Cl原子和被還原的Cl原子的物質的量之比為5∶1
C. Cl2既做氧化劑又做還原劑
D. 氧化劑得電子數與還原劑失電子數之比為5∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,用濃度為0.1000molL﹣1 NaOH溶液分別滴定20.00mL濃度均為0.1000molL﹣1的三種酸HX、HY、HZ,滴定曲線如圖所示.下列說法正確的是( ) 
A.相同濃度時,三種酸的酸性強弱順序是:HX>HY>HZ
B.根據滴定曲線可得,Ka(HX)=10﹣3 molL﹣1
C.滴定HY,V(NaOH)=20 mL時,c(Na+)=c(Y﹣)>c(OH﹣)=c(H+)
D.滴定HZ,V(NaOH)=15 mL時,c(Z﹣)>c(Na+)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】KClO3和濃鹽酸在一定溫度下反應會生成黃綠色的易爆物二氧化氯。其變化可以表述為:
KClO3+ HCl(濃) → KCl+ ClO2↑+ Cl2↑+ H2O
(1)請完成該化學方程式并配平__________________
(2)濃鹽酸在反應中顯示出來的性質是_______(填寫編號,多選倒扣)。
①只有還原性 ②還原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)產生0.1molCl2,則轉移的電子的物質的量是為_________mol。
(4)ClO2具有很強的氧化性。因此,常被用作消毒劑,其消毒的效率(以單位質量得到的電子數表示)是Cl2的_______倍。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某種制取純堿的方法如下:

(1)寫出“反應I ”的化學方程式:__。
(2)“反應Ⅱ”為復分解反應,反應中所涉及物質的溶解度如圖所示。寫出“反應Ⅱ”的化學方程式:__。

(3)寫出“煅燒”反應的化學方程式:__。
(4) “蒸氨”時需要加熱,寫出“蒸氨”時反應的化學方程式:___。
(5)寫出將“蒸氨”產生的氨氣通入Al2(SO4)3溶液中時反應的離子方程式: __。
【答案】 NH3·H2O+CO2=NH4HCO3 NaCl+NH4HCO3=NaHCO3↓+NH4Cl 2NaHCO3![]() Na2CO3+CO2↑+H2O 2NH4Cl+Ca(OH)2
Na2CO3+CO2↑+H2O 2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O Al3++3NH3·H2O=Al(OH)3↓+3NH4+
CaCl2+2NH3↑+2H2O Al3++3NH3·H2O=Al(OH)3↓+3NH4+
【解析】(1)氨水顯堿性,CO2為酸性氧化物,二者反應生成鹽,CO2過量時生成酸式鹽即碳酸氫銨,故化學方程式為:NH3·H2O+CO2=NH4HCO3。
(2)氨氣極易溶于水,氨水的濃度非常大,可以溶解大量的氨氣,則反應I得到濃度較大的碳酸氫銨溶液。向碳酸氫銨溶液中加入食鹽后,溶液中主要存在四種離子:Na+、NH4+、HCO3-、Cl-,根據溶解度曲線可知,同溫度下NaHCO3的溶解度最小,溶液中會析出晶體NaHCO3。反應II為復分解反應,則反應方程式為NaCl+NH4HCO3=NaHCO3↓+NH4Cl。
(3)過濾得到NaHCO3晶體,加熱,NaHCO3分解為Na2CO3、H2O、CO2,反應方程式為:2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
(4)向NH4Cl溶液中加入石灰乳,NH4+與OH-結合為NH3·H2O,加熱條件下,促進NH3逸出,即為“蒸氨”,反應方程式為2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(5)氨氣溶于水得NH3·H2O,NH3·H2O堿性強于Al(OH)3,故將NH3通入Al2(SO4)3溶液中有Al(OH)3沉淀生成,離子方程式為:Al3++3NH3·H2O=Al(OH)3↓+3NH4+。
【題型】綜合題
【結束】
22
【題目】實驗室制備氯化亞銅(一種難溶于水的白色固體)的流程如下:

(1)“反應I”在加熱條件下進行,同時有MnCl2生成,該反應的化學方程式為 __。
(2) “反應Ⅱ”中雜質與Cl2反應的化學方程式為__。 ⑶實驗所用SO2氣體可由銅和濃硫酸反應制得,該反應的化學方程式為__
(4)“反應Ⅲ”的離子方程式為___。
(5)若將等物質的量的S02、Cl2通入水中,所得溶液幾乎沒有漂白性,該反應的離子方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】維生素B2也稱“核黃素”,其結構如下圖.維生素B2的磷酸鹽衍生物是某些氧化還原酶的輔基,為生長必需物質,缺少維生素B2會引起口角炎、皮膚和眼部疾病.下列有關維生素B2的說法中正確的是( ) 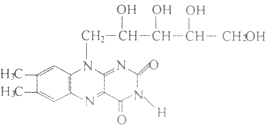
A.核黃素晶體屬于離子晶體
B.核黃素能發生銀鏡反應
C.核黃素能被酸性高錳酸鉀溶液氧化
D.核黃素能與氯化鐵溶液作用呈紫色
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com