
【題目】霧霾天氣頻繁出現,嚴重影響人們的生活和健康。其中首要污染物為可吸入顆粒物PM2.5,其主要來源為燃煤、機動車尾氣等。因此,對PM2.5、SO2、NOx等進行研究具有重要意義。請回答下列問題:
(1)將PM2.5樣本用蒸餾水處理制成待測試樣。
若測得該試樣所含水溶性無機離子的化學組分及其平均濃度如下表:
離子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
濃度mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根據表中數據判斷試樣的pH=_________。
(2)汽車尾氣中NOx和CO的生成:
①已知汽缸中生成NO的反應為:N2(g)+O2(g)![]() 2NO(g) △H>0恒溫,恒容密閉容器中,下列說法中能說明該反應達到化學平衡狀態的是____
2NO(g) △H>0恒溫,恒容密閉容器中,下列說法中能說明該反應達到化學平衡狀態的是____
A.混合氣體的密度不再變化 B.混合氣體的平均分子量不再變化
C.N2、O2、NO的物質的量之比為1∶1∶2 D.氧氣的百分含量不再變化
②汽車燃油不完全燃燒時產生CO,有人設想按下列反應除去CO,2CO(g)=2C(s)+O2(g),已知該反應的△H>0,則該設想能否實現______________(填“能”或“不能”)
(3)為減少SO2的排放,常采取的措施有:
①將煤轉化為清潔氣體燃料。已知:
H2(g)+ 1/2O2(g) =H2O(g) △H=-241.8kJ·mol-1
C(s)+1/2O2(g) =CO(g)△H =-110.5kJ·mol-1
寫出焦炭與水蒸氣反應的熱化學方程式:___________________。
②洗滌含SO2的煙氣。
(4)汽車尾氣凈化的主要原理:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g);△H<0,若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是_________(填序號)。(如圖中v正、K、n、w分別表示正反應速率、平衡常數、物質的量、質量分數)
2CO2(g)+N2(g);△H<0,若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是_________(填序號)。(如圖中v正、K、n、w分別表示正反應速率、平衡常數、物質的量、質量分數)

車輛排放的氮氧化物、煤燃燒產生的二氧化硫是導致霧霾天氣的“罪魁禍首”之一。活性炭可處理大氣污染物NO。在5L密閉容器中加入NO和活性炭(假設無雜質)。一定條件下生成氣體E和F。當溫度分別在T1℃和T2℃時,測得各物質平衡時物質的量(n/mol)如下表:
物質 溫度/℃ | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
(1)寫出NO與活性炭反應的化學方程式______________________;
(2)計算上述反應T1℃時的平衡常數K1=__________________;若T1<T2,則該反應的△H__________________0(填“>”、“<”或“=”)。
(3)上述反應T1℃時達到化學平衡后再通入0.1molNO氣體,則達到新化學平衡時NO的轉化率為________;
【答案】4D不能C(s)+H2O(g)=CO(g)+H2(g) △H= +131.3 kJmol-1BDC(s)+2NO(g)=CO2(g)+N2(g)4<80%
【解析】
(1)根據表格提供的離子可知,NH4+ 水解導致試樣溶液呈酸性,再根據電荷守恒可知,c(K+)+c(NH4+ )+c(Na+)+c(H+)=2c(SO42-)+c(Cl-)+c(NO3-),將表格中的數據代入得H+離子濃度為10-4,則PH值為4。
(2)①在恒容密閉容器中,混合氣體的質量和體積始終不變,混合氣體的密度也始終不變,密度不能作為達到平衡狀態的判據,A項錯誤;該反應是氣體體積不變的可逆反應,根據M=質量/n,則混合氣體的平均分子量始終不變,不能作為達到平衡的判據,B項錯誤;N2、O2、NO的物質的量之比為1∶1∶2不能說明反應各物質的濃度保持不變,C項錯誤;氧氣的百分含量不再變化,說明反應達到平衡狀態,D項正確;答案選D。
②化學反應2CO(g)=2C(s)+O2(g)是一個熵減、吸熱的反應,則△H-T△S>0,所以該設想不能實現。
(3)已知:①H2(g)+ 1/2O2(g) =H2O(g) △H=-241.8kJ·mol-1、②C(s)+1/2O2(g) =CO(g) △H =-110.5kJ·mol-1,利用蓋斯定律,將②-①可得C(s)+H2O(g)=CO(g)+H2(g)△H=(-110.51kJmol-1)-(-241.81kJmol-1)=+13l.3 kJmol-1,所以焦炭與水蒸氣反應的熱化學方程式為C(s)+H2O(g)=CO(g)+H2(g) △H= +131.3 kJmol-1 。
(4)可逆反應達化學平衡狀態時正逆反應速率不再變化,A項錯誤;該物質的濃度在化學平衡時保持不變,所以K不再變化,B項正確;對于恒容容器而言,各物質的物質的量不再改變,C項錯誤;平衡時NO的質量分數不再改變,D項正確,答案選BD。
(5)①由表中數據可知,C、NO、E、F的化學計量數之比為0.040:0.080:0.040:0.040 =1:2:1:1,反應中C被氧化,結合原子守恒可知,生成物為N2與CO2,且該反應為可逆反應,則反應方程式為C(s)+2NO(g) CO2(g)+N2(g)。
②從表中數據可知T1℃時的平衡濃度c(NO)=0.004mol/L,c(N2)=c(CO2)=0.008 mol/L,則T1℃時該反應的平衡常數為K1=(0.008×0.008)÷(0.004×0.004)=4;從T1到T2,NO的濃度增大,說明平衡逆向移動,若T1<T2,升高溫度,平衡向吸熱反應方向移動,則該反應的正向為放熱反應,則△H < 0。
③在T1時,K=4,設NO的轉化率為x,根據三段式解答:
C(s)+2NO(g) CO2(g)+N2(g)
起始濃度 0.04 0 0
變化濃度 0.04x 0.02x 0.02x
平衡濃度 0.04-0.04x 0.02x 0.02x
K=[0.02x×0.02x]÷[(0.04-0.04x)×(0.04-0.04x)=4,解得x=0.8,即達到新的平衡時,NO的轉化率為80%。


科目:高中化學 來源: 題型:
【題目】請根據題目要求回答以下問題:
(1)CuSO4·5H2O的摩爾質量是________; 0.1mol CH4含有的氫原子數為____; 0.2 mol·L-1的 AlCl3溶液中Cl—的物質的量濃度是________。
(2)現有以下物質:①NaCl ②氯水③醋酸 ④HCl ⑤酒精(C2H5OH)⑥CaCO3⑦Ba(OH)2屬于強電解質的是__________,屬于弱電解質的是_______。(填序號)
寫出Ba(OH)2的電離方程式_________________________,
寫出④與⑥反應的離子方程式____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲、乙、丙、丁、戊五種物質中,甲、乙、丙中均含有某種相同的元素,它們之間具有如圖所示轉化關系(反應條件及部分產物已略去)。下列有關物質的推斷不正確的是( )
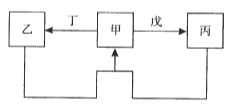
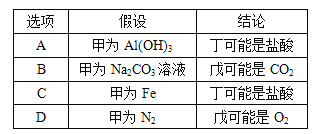
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[物質結構與性質]
原子序數小于36的X、Y、Z、W、R五種元素,原子序數依次增大。五種元素中,僅R為金屬元素,其原子序數為27。X價電子排布式為nsnnpn,元素Z基態原子s電子總數與p電子總數相等,W與其它四種元素能層數不同,且未成對電子數目為1個。
根據判斷出的元素回答下列問題:
(1)基態R原子核外電子排布式為 ,X、Y、Z三種原子第一電離能由大到小的順序為 (用具體元素符號表示)。
(2)1mol配合物[R(XY)6]4-中含有σ鍵的數目為 。
(3)XZW2是一種高毒類物質,結構與甲醛相似,X原子雜化方式為 ,其沸點高于甲醛的主要原因是 。
(4)YW3為黃色、油狀、具有刺激性氣味的液體,該分子的立體構型為 (用文字描述)。
(5)某晶體的晶胞結構如下圖所示,則該化合物的化學式為 (R、Z用具體元素符號表示)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外興趣小組進行電解原理的實驗探究,做了如下的實驗:以銅為電極,按如圖所示的裝置電解飽和食鹽水。
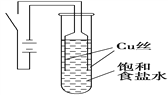
實驗現象:接通電源30 s內,陽極附近出現白色渾濁,之后變成橙黃色渾濁,此時測定溶液的pH約為10。一段時間后,試管底部聚集大量紅色沉淀,溶液仍為無色。
查閱資料:
物質 | 氯化銅 | 氧化亞銅 | 氫氧化亞銅(不穩定) | 氯化亞銅 |
顏色 | 固體呈棕色,濃溶液呈綠色,稀溶液呈藍色 | 紅色 | 橙黃色 | 白色 |
※ 相同溫度下CuCl的溶解度大于CuOH。
下列說法錯誤的是( )
A. 反應結束后最終溶液呈堿性 B. 陰極上發生的電極反應為:2H2O + 2e- == H2↑+ 2OH-
C. 電解過程中氯離子移向陽極 D. 試管底部紅色的固體具有還原性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在2 L的密閉容器中發生如下反應:A(s)+2B(g)![]() xC(g) ΔH<0,B、C的物質的量隨時間變化的關系如圖1,達平衡后在t1、t2、t3、t4時都只改變了一種條件,逆反應速率隨時間變化的關系如圖2。
xC(g) ΔH<0,B、C的物質的量隨時間變化的關系如圖1,達平衡后在t1、t2、t3、t4時都只改變了一種條件,逆反應速率隨時間變化的關系如圖2。
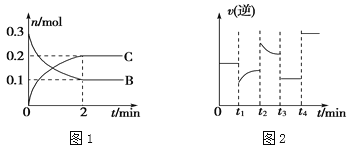
下列有關說法正確的是( )
A. x=2,反應開始2 min內,v(B)=0.1 mol/(L·min)
B. t1時改變的條件是降溫,平衡逆向移動
C. t2時改變的條件可能是增大c(C),平衡時B的物質的量分數增大
D. t3時可能是減小壓強,平衡不移動;t4時可能是使用催化劑,c(B)不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有四種物質的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④CuCl2 , 不用其他試劑就可將它們逐一鑒別出來,其鑒別順序是( )
A.④①②③
B.①③④②
C.④③②①
D.①④②③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生活離不開“柴米油鹽醬醋茶”,以下有關說法正確的是
A. 柴草是目前主要的新能源 B. 用汽油清洗衣物上的油漬利用了乳化原理
C. 加碘食鹽中加入了I2 D. 食醋可用于清洗熱水瓶中的水垢
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com