
化學反應變化過程及結果的研究。按要求回答問題:
(1)關于反應過程中能量變化的研究:

則:2CO(g)+O2(g)=2CO2(g)△H= kJ·mol-1。
(2)關于反應速率和限度的研究:
工業生產尿素的原理是以NH3和CO2為原料合成尿素[CO(NH2)2],反應的化學方程式為:
2NH3 (g)+ CO2 (g)  CO(NH2)2
(l) + H2O (l),該反應的平衡常數(K)和溫度(T / ℃)關系如下:
CO(NH2)2
(l) + H2O (l),該反應的平衡常數(K)和溫度(T / ℃)關系如下:
|
T / ℃ |
165 |
175 |
185 |
195 |
|
K |
111.9 |
74.1 |
50.6 |
34.8 |
①焓變ΔH _______0 (填“>”、“<”或“=”)。
②在一定溫度和壓強下,若原料氣中的NH3和CO2的物質的量之比(氨碳比) ,下圖(1)是氨碳比(x)與CO2平衡轉化率(α)的關系。α隨著x增大而增大的原因是 。
,下圖(1)是氨碳比(x)與CO2平衡轉化率(α)的關系。α隨著x增大而增大的原因是 。

③上圖中的B點處,NH3的平衡轉化率為 。
(3)關于電化學的研究:
鋁是日常生活中用途最多的金屬元素,下圖為Al-AgO電池的構造簡圖,電解質溶液為NaOH,它可用作水下動力電源,該電池中鋁電極反應式為 。用該電池電解尿素[CO(NH2)2]的堿性溶液制氫的裝置示意圖如下圖(電解池中隔膜僅阻止氣體通過,陰、陽極均為惰性電極)。電解時,陽極的電極反應式為 。


(4)關于電離平衡的研究:
人體血液里存在重要的酸堿平衡: ,使人體血液pH保持在7.35~7.45,否則就會發生酸中毒或堿中毒。其pH隨c(HCO3-)∶c(H2CO3)變化關系如下表:
,使人體血液pH保持在7.35~7.45,否則就會發生酸中毒或堿中毒。其pH隨c(HCO3-)∶c(H2CO3)變化關系如下表:
|
c(HCO3-) ∶c(H2CO3) |
1.0 |
17.8 |
20.0 |
22.4 |
|
pH |
6.10 |
7.35 |
7.40 |
7.45 |
試回答:
正常人體血液中,HCO3-的水解程度 電離程度(填“大于”、“小于”、“等于”);
②人體血液酸中毒時,可注射緩解 (填選項);
A.NaOH溶液 B.NaHCO3溶液 C.NaCl溶液 D.Na2SO4溶液
③ pH=7.00的血液中,c(H2CO3) c(HCO3-) (填“<”、“>”、“=”)
(1)-a+2b-4c(2分)
(2)① < (2分) ②c(NH3)增大,平衡正向移動(2分) ③32% (3分)
(3)Al+4OH-―3e-=AlO2-+2H2O(2分) CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O (2分)
(4)①大于(1分); ②B(1分) ③<(1分)
【解析】
試題分析:(1) 運用蓋斯定律,可得要求化學反應的∆H=∆H1-2∆H2+4∆H3。
(2)①隨著溫度升高,平衡常數K逐漸減少,所以正反應為放熱反應,∆H<0。
②c(NH3)增大,平衡正向移動,CO2的轉化率增大。
③B點氨碳比為4.0,設氨的物質的量為4n,CO2的物質的量為n,則轉化的CO2為0.64n,根據化學方程式可得轉化的氨為1.28n,則氨的轉化率為:1.28n÷4n×100%=32%
(3)Al在OH‾存在條件下失去3e‾, 生成AlO2-,根據圖(3)可以看出陽極產生N2,CO(NH2)2中的C轉化為CO32‾,H與OH‾轉化為H2O,配平可得電極方程式。
(4)正常人體血液pH保持在7.35~7.45,所以HCO3‾的水解程度大于電離程度,HCO3‾能調節pH,起到緩沖作用,所以選B NaHCO3溶液,因為等濃度的H2CO3的電離程度大于HCO3‾的水解程度,血液的pH為7.00,則H2CO3的程度小于H CO3‾的程度。
考點: 本題考查蓋斯定律、化學平衡移動、轉化率的計算、電極方程式的書寫和電解質溶液的電離和水解。


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |

| OH- |
| H+ |
| c(HCO3-):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 以下是對化學反應變化過程及結果的研究.按要求回答問題:
以下是對化學反應變化過程及結果的研究.按要求回答問題:| 弱酸化學式 | CH3COOH | HCN | H2CO |
| 電離平衡常數(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K1=5.6×10-11 |
| 放電 |
| 通電 |
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪專題沖刺第7講 水溶液中的離子平衡練習卷(解析版) 題型:選擇題
以下是對化學反應變化過程及結果的研究。按要求回答問題:
Ⅰ.關于反應速率和限度的研究
(1)已知25℃時有關弱酸的電離平衡常數:
弱酸化學式 | CH3COOH | HCN | H2CO3 |
電離平衡常數(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
則等物質的量濃度的①CH3COONa、②NaCN、③Na2CO3、④NaHCO3溶液的pH由大到小的順序為__________(填編號)。
(2)已知2SO2(g)+O2(g)??2SO3(g) ΔH=-196.6 kJ·mol-1,在一個容積為2 L的容器中加入2 mol SO2和1 mol O2,在某溫度下充分反應,經過30 min達到平衡,放出熱量176.94 kJ。如果用SO2表示該反應的反應速率,則v(SO2)=________。
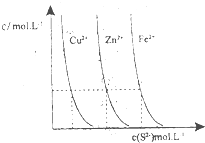
(3)下圖為某溫度下,CuS(s)、ZnS(s)、FeS(s)分別在溶液中達到沉淀溶解平衡后,溶液的S2-濃度、金屬陽離子濃度變化情況。如果向三種沉淀中加鹽酸,最先溶解的是________。

向新生成的ZnS濁液中滴入足量含相同濃度的Cu2+、Fe2+的溶液,振蕩后,ZnS沉淀會轉化為________(填化學式)沉淀。
Ⅱ.關于電化學的研究
全釩液流電池是一種新型的綠色環保儲能電池。其電池總反應為:VO2++2H++V2+ V3++VO2++H2O。則充電時陽極反應式為__________________________,用此電池電解1 L 1 mol·L-1的CuSO4溶液,當轉移0.1 mol電子時,溶液的pH=________(不考慮溶液體積變化)。
V3++VO2++H2O。則充電時陽極反應式為__________________________,用此電池電解1 L 1 mol·L-1的CuSO4溶液,當轉移0.1 mol電子時,溶液的pH=________(不考慮溶液體積變化)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com