
用Pt做電極,電解含C(Cu2+): C(Na+): C(Cl-)=1:2:4的混合溶液,在任何情況下,陰、陽兩極下不可能同時發生的反應是
| A.陰極:2H++2e-=H2↑陽極:4OH-- 4e-=2H2O+O2↑ |
| B.陰極:2H++2e-=H2↑陽極:2Cl--2e-=Cl2↑ |
| C.陰極:Cu2++2e-=Cu陽極:4OH-- 4e-=2H2O+O2↑ |
| D.陰極:Cu2++2e-="Cu" 陽極:2Cl--2e-=Cl2↑ |
 舉一反三同步巧講精練系列答案
舉一反三同步巧講精練系列答案 口算與應用題卡系列答案
口算與應用題卡系列答案 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源: 題型:單選題
在下圖裝置中,若通電一段時間后乙裝置左側電極質量增加,則下列說法錯誤的是( )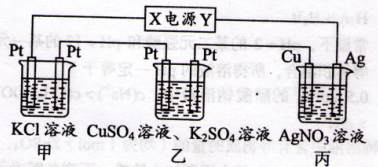
| A.乙中左側電極反應式:Cu2++2e-=Cu |
| B.電解過程中裝置丙的pH無變化 |
| C.向甲中通人適量的HCl氣體,可使溶液恢復到電解前的狀態 |
| D.當甲裝置中產生標準狀況下4.48 L氣體時,Cu電極上質量增加43.2 g |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
有關下列四個常用電化學裝置的敘述中,正確的是
 |  |  |  |
| 圖Ⅰ 堿性鋅錳電池 | 圖Ⅱ 鉛-硫酸蓄電池 | 圖Ⅲ 電解精煉銅 | 圖Ⅳ 銀鋅紐扣電池 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下圖為Mg—NaClO燃料電池結構示意圖。下列說法正確的是
| A.鎂作Y電極 |
| B.電池工作時Na+向負極移動 |
| C.廢液的pH大于NaClO溶液的pH |
| D.X電極上發生的反應為:ClO—+2H2O—4e—=ClO3—+4H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
硫化氫(H2S)是一種有毒的可燃性氣體,用H2S、空氣和KOH溶液可以組成燃料電池,其總反應式為2H2S+3O2+4KOH=2K2SO3+4H2O。
(1)該電池工作時正極應通入 。
(2)該電池的負極電極反應式為: 。
(3)該電池工作時負極區溶液的pH (填“升高”“不變”“降低”)
(4)有人提出K2SO3可被氧化為K2SO4,因此上述電極反應式中的K2SO3應為K2SO4,某學習小組欲將電池工作一段時間后的電解質溶液取出檢驗,以確定電池工作時反應的產物。實驗室有下列試劑供選用,請幫助該小組完成實驗方案設計。
0.01mol·L-1KMnO4酸性溶液,1mol·L-1HNO3,1mol·L-1H2SO4,1mol·L-1HCl,
0.1mol·L-1Ba(OH)2,0.1 mol·L-1 BaCl2。
| | 實驗步驟 | 實驗現象及相關結論 |
| ① | 取少量電解質溶液于試管中,用pH試紙測其pH。 | 試紙呈深藍色,經比對溶液的pH約為14,說明溶液中有殘余的KOH。 |
| ② | 繼續加入 溶液,再加入 溶液,振蕩。 | 若有白色沉淀產生,則溶液中含有K2SO4。 若無白色沉淀產生,則溶液中沒有K2SO4。 |
| ③ | 另取少量電解質溶液于試管中,先加 1 mol·L-1的H2SO4酸化,再滴入2~3滴0.01 mol·L-1KMnO4酸性溶液,振蕩。 | ; 。 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
(2013茂名一模,11)研究小組分別用鋅片、鋁片、Cu和稀硫酸進行原電池的相關的探究,所得部分實驗數據如下,下列說法正確的是
| 實驗 | 電極甲 | 電極乙 |
| I | Zn | Cu |
| II | Al | Cu |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
關于下列裝置說法正確的是 
| A.裝置①中,鹽橋中的K+移向ZnSO4溶液 |
| B.裝置②工作一段時間后,a極附近溶液的pH增大 |
| C.用裝置③精煉銅時,c極為粗銅 |
| D.裝置④中電子由Zn流向Sn,Sn為正極有氣泡生成 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
某小組為研究電化學原理,設計如圖裝置。下列敘述不正確的是
| A.a、b不連接時,只有鋅片上有氣泡逸出 |
| B.a和b用導線連接時,銅片上發生的反應為:2H+ + 2e-=H2 ↑ |
| C.a和b是否用導線連接,裝置中所涉及的化學反應都相同 |
| D.a和b用導線連接或接直流電源,鋅片都能溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
將純鋅片和純銅片按圖示方式插入同濃度的稀硫酸中一段時間,以下敘述正確的是( )
| A.兩燒杯中銅片表面均無氣泡產生 |
| B.甲中銅片是正極,乙中銅片是負極 |
| C.兩燒杯中溶液的pH均增大 |
| D.產生氣泡的速度甲比乙慢 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com