
四種鹽在不同溫度下的溶解度(g/100g水)表
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | - | - | - |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
①>35℃NH4HCO3會有分解
請回答:
(1)反應溫度控制在30~35℃,是因為若高于35℃,則 ,若低于30℃,則 ;為控制此溫度范圍,采取的加熱方法為 。
(2)加料完畢后,繼續保溫30分鐘,目的是 。靜置后只析出NaHCO3晶體的原因是 。用蒸餾水洗滌NaHCO3晶體的目的是除去 雜質(以化學式表示)。
(3)過濾所得的母液中含有 (以化學式表示),需加入 ,并作進一步處理,使NaCl溶液循環使用,同時可回收NH4Cl。
(4)測試純堿產品中NaHCO3含量的方法是:準確稱取純堿樣品W g,放入錐形瓶中加蒸餾水溶解,加1~2滴酚酞指示劑,用物質的量濃度為c(mol/L)的HCl溶液滴定至溶液由紅色到無色(指示CO32-+H+==HCO3-反應的終點),所用HCl溶液體積為V1 mL,再加1~2滴甲基橙指示劑,繼續用HCl溶液滴定至溶液由黃變橙,所用HCl溶液總體積為V2 mL。
寫出純堿樣品中NaHCO3質量分數的計算式:NaHCO3(%)=
答案:
(1)NH4HCO3分解
反應速率降低
水浴加熱
(2)使反應充分進行
NaHCO3的溶解度最小
NaCl NH4Cl NH4HCO3
(3)NaHCO3、NaCl、NH4Cl、NH4HCO3 HCl
(4)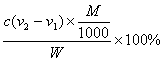
解析:侯德榜制堿法利用一定條件下NaHCO3溶解度相對較小的特點,在飽和食鹽水中先后通入NH3、CO2,獲得NaHCO3后灼燒生成Na2CO3。
根據表格,40 ℃以上NH4HCO3溶解度不再給出,因為在35 ℃以上NH4HCO3開始分解。在35 ℃下盡量提高溫度可以讓反應速度加快,有利于提高單位時間產率。反應液中存在Na+、Cl-、NH![]() 、HCO
、HCO![]() ,參照30 ℃時各物質溶解度可知,此時溶解度最小的NaHCO3最先析出。30 ℃時,NaHCO3溶解度為11.1g,說明Na+、HCO
,參照30 ℃時各物質溶解度可知,此時溶解度最小的NaHCO3最先析出。30 ℃時,NaHCO3溶解度為11.1g,說明Na+、HCO![]() 不可能全部沉淀。最終得到的母液中同時存在Na+、Cl-、NH
不可能全部沉淀。最終得到的母液中同時存在Na+、Cl-、NH![]() 、HCO
、HCO![]() ,向其中加入HCl,可使NaCl溶液循環使用,并能回收NH4Cl。
,向其中加入HCl,可使NaCl溶液循環使用,并能回收NH4Cl。
在滴定過程中,Na2CO3發生兩步反應:
Na2CO3 + HCl ==== NaHCO3+NaCl
cV1/1000 cV1/1000
NaHCO3 + HCl====NaCl+H2O+CO2↑
cV1/1000 cV1/1000
Na2CO3消耗的HCl共2cV1/1 000 mol,則NaHCO3消耗的HCl為(cV2/1000-2cV1/1000) mol,樣品中NaHCO3的純度為: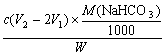 ×100%。
×100%。


科目:高中化學 來源: 題型:閱讀理解
| 溫度溶解度鹽 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
| c(V2-V1)M |
| 1000W |
| c(V2-V1)M |
| 1000W |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 物質 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | 35℃以上分解 | |||
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
| A、第一、二步反應的基本類型為化合反應、分解反應 |
| B、第一、二步反應之間的主要實驗操作是過濾、洗滌 |
| C、第一步反應控制溫度高于30℃目的是提高反應產率 |
| D、反應液加鹽酸處理可使NaCl循環使用并回收NH4Cl |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
四種鹽在不同溫度下的溶解度(g/100 g水)表
溫度 溶解度 鹽 | ||||||||
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | —① | — | — | — |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
①>
請回答:
(1)反應溫度控制在30—35 ℃,是因為若高于35 ℃,則_______________,若低于30 ℃,則_________________;為控制此溫度范圍,采取的加熱方法為_______________________。
(2)加料完畢后,繼續保溫30分鐘,目的是____________________。靜置后只析出NaHCO3晶體的原因是__________________。用蒸餾水洗滌NaHCO3晶體的目的是除去_______________雜質(以化學式表示)。
(3)過濾所得母液中含有_____________(以化學式表示),需加入_______________,并作進一步處理,使NaCl溶液循環使用,同時可回收NH4Cl。
(4)測試純堿產品中NaHCO3含水量的方法是:準確稱取純堿樣品W g,放入錐形瓶中加蒸餾水溶解,加1—2滴酚酞指示劑,用物質的量濃度為c(mol·L-1)的HCl溶液滴定至溶液由紅色到無色(指示![]() +H+
+H+![]()
![]() 反應的終點),所用HCl溶液體積為V1 mL,再加1—2滴甲基橙指示劑,繼續用HCl溶液滴定至溶液由黃變橙,所用HCl溶液總體積為V2mL。寫出純堿樣品中NaHCO3質量分數的計算式:
反應的終點),所用HCl溶液體積為V1 mL,再加1—2滴甲基橙指示劑,繼續用HCl溶液滴定至溶液由黃變橙,所用HCl溶液總體積為V2mL。寫出純堿樣品中NaHCO3質量分數的計算式:
NaHCO3(%)=___________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
根據侯德榜制堿法原理,實驗室用食鹽、氨水、大理石、鹽酸制取碳酸鈉。其實驗過程如下:①配制含氨的氯化鈉飽和溶液;②用石灰石和稀鹽酸制取純凈的CO2;③將CO2通入NaCl的氨溶液中,得到碳酸氫鈉晶體;④過濾,冷水洗滌沉淀;⑤焙燒NaHCO3得到Na2CO3。
試回答下列問題:
(1)某學生將實驗步驟①②③設計成下圖所示的裝置:

洗氣瓶B中的液體是_________,燒杯C中的液體是_________。裝置A中的離子方程式是____________________________________。
(2)實驗步驟④中過濾操作要求做到“一貼、二低、三靠”,其具體含義是:
一貼:_____________________________________________;
二低:_____________________________________________;
三靠:_____________________________________________。
洗滌沉淀的目的是___________________________________________________________。
(3)該學生設計下圖所示裝置進行NaHCO3的分解,并證實產物中有CO2產生。

①試管中發生的化學反應方程式是:____________________________________。
②指出該學生設計的裝置圖的錯誤之處,并改正(文字說明即可)。
③停止加熱時應該怎樣操作,為什么?
④燒杯中發生反應的離子方程式是:____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
四種鹽在不同溫度下的溶解度(g/100 g水)表
溫度 溶解度 鹽 | 0 ℃ | 10 ℃ | 20 ℃ | 30 ℃ | 40 ℃ | 50 ℃ | 60 ℃ | 100 ℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | —① | — | — | — |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
NH4C | l29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
①>35℃ NH4HCO3會有分解
請回答:
(1)反應溫度控制在30—35 ℃,是因為若高于35 ℃,則__________________________,若低于30 ℃,則______________________________________;為控制此溫度范圍,采取的加熱方法為__________________________________________________________。
(2)加料完畢后,繼續保溫30分鐘,目的是______________________________________。靜置后只析出NaHCO3晶體的原因是___________________________________________。用蒸餾水洗滌NaHCO3晶體的目的是除去_______________________________________雜質(以化學式表示)。
(3)過濾所得的母液中含有______________________________________(以化學式表示),需加入___________________,并作進一步處理,使NaCl溶液循環使用,同時可回收NH4Cl。
(4)測試純堿產品中NaHCO3含量的方法是:準確稱取純堿樣品W g,放入錐形瓶中加蒸餾水溶解,加1—2滴酚酞指示劑,用物質的量濃度為c( mol·L-1)的HCl溶液滴定至溶液由紅色到無色(指示![]() +H+====
+H+====![]() 反應的終點),所用HCl溶液體積為V1 mL,再加1—2滴甲基橙指示劑,繼續用HCl溶液滴定至溶液由黃變橙,所用HCl溶液總體積為V2 mL。寫出純堿樣品中NaHCO3質量分數的計算式:
反應的終點),所用HCl溶液體積為V1 mL,再加1—2滴甲基橙指示劑,繼續用HCl溶液滴定至溶液由黃變橙,所用HCl溶液總體積為V2 mL。寫出純堿樣品中NaHCO3質量分數的計算式:
w(NaHCO3)=___________________。
?
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com