
【題目】有濃度均為0.1molL﹣1的鹽酸、硫酸和醋酸三種溶液,試分析:
(1)若溶液的C(H+)分別為a、b、c,則它們的大小關系是(用“>”“<”“=”表示),
(2)分別用三種酸中和等物質的量的氫氧化鈉溶液,所需溶液的體積分別是a、b、c,則它們的大小關系是(用“>”“<”“=”表示).
(3)等體積的三種酸分別與足量的鋅粒反應,在相同條件下若產生氣體的體積分別為a、b、c,則它們的關系是 .
(4)可逆反應2Cl2(g)+2H2O(g)4HCl(g)+O2(g)△H>0,在一定條件下達到平衡后,分別采取下列措施(填“增大”、“減小”或“不變”):
①降低溫度,Cl2的轉化率;
②保持容器體積不變,加入He,則HCl的物質的量;
③保持容器壓強不變,加入He,則O2的體積分數 .
【答案】
(1)b>a>c
(2)a=c=2b
(3)a=c= ![]() b
b
(4)減小;不變;增大
【解析】解:(1)硫酸和鹽酸是強酸,醋酸是弱酸,則c(H+)=c(HCl)=0.1mol/L,c(H+)=2c(H2SO4)=0.2mol/L,c(H+)<c(CH3COOH)=0.1mol/L,所以它們的大小關系是b>a>c,所以答案是:b>a>c;(2)三種酸的濃度相等,鹽酸和醋酸都是一元酸,硫酸是二元酸,硫酸溶液中氫離子濃度是鹽酸溶液中的2倍,則完全中和物質的量均相同的三份NaOH溶液時,鹽酸和醋酸需要的體積相等,需要硫酸的體積是鹽酸的一半,所以需三種酸的體積大小關系是a=c=2b,所以答案是:a=c=2b;(3)等體積等濃度的三種酸中,氫元素的物質的量2n(HCl)=2n(CH3COOH)=n((H2SO4),根據氫原子守恒知,生成氫氣的體積大小順序是a=c= ![]() b,所以答案是:a=c=
b,所以答案是:a=c= ![]() b;(4)①該反應的正方向為吸熱反應,所以降低溫度,平衡逆移,Cl2的轉化率 減小;所以答案是:減小;②保持容器體積不變,加入He,容器體積不變,各物質的濃度不變,所以對反應無影響,所以HCl的物質的量不變,所以答案是:不變;③保持容器壓強不變,加入He,體積變大,反應物所占分壓減小,平衡正移,則O2的體積分數增大,所以答案是:增大.
b;(4)①該反應的正方向為吸熱反應,所以降低溫度,平衡逆移,Cl2的轉化率 減小;所以答案是:減小;②保持容器體積不變,加入He,容器體積不變,各物質的濃度不變,所以對反應無影響,所以HCl的物質的量不變,所以答案是:不變;③保持容器壓強不變,加入He,體積變大,反應物所占分壓減小,平衡正移,則O2的體積分數增大,所以答案是:增大.
【考點精析】本題主要考查了化學平衡狀態本質及特征和弱電解質在水溶液中的電離平衡的相關知識點,需要掌握化學平衡狀態的特征:“等”即 V正=V逆>0;“動”即是動態平衡,平衡時反應仍在進行;“定”即反應混合物中各組分百分含量不變;“變”即條件改變,平衡被打破,并在新的條件下建立新的化學平衡;與途徑無關,外界條件不變,可逆反應無論是從正反應開始,還是從逆反應開始,都可建立同一平衡狀態(等效);當弱電解質分子離解成離子的速率等于結合成分子的速率時,弱電解質的電離就處于電離平衡狀態;電離平衡是化學平衡的一種,同樣具有化學平衡的特征.條件改變時平衡移動的規律符合勒沙特列原理才能正確解答此題.


 提分百分百檢測卷單元期末測試卷系列答案
提分百分百檢測卷單元期末測試卷系列答案 小學期末標準試卷系列答案
小學期末標準試卷系列答案科目:高中化學 來源: 題型:
【題目】化學能可與熱能、電能等相互轉化。下列表述不正確的是( )
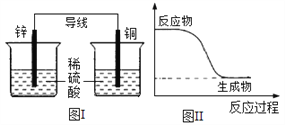
A. 有能量變化是化學反應的基本特征之一
B. 圖I所示的裝置能將化學能轉變為電能
C. 圖II所示的反應為放熱反應
D. 化學反應中能量變化的主要原因是化學鍵的斷裂與形成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在某容積一定的密閉容器中,有下列的可逆反應:A(g)+B(g)xC(g) , 有圖Ⅰ所示的反應曲線,試判斷對圖Ⅱ的說法中正確的是(T表示溫度,P表示壓強,C%表示C的體積分數)( ) 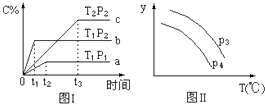
A.P3>P4 , y軸表示B的轉化率
B.P3<P4 , y軸表示B的體積分數
C.P3<P4 , y軸表示混合氣體的密度
D.P3<P4 , y軸表示混合氣體的平均摩爾質量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列檢驗銨鹽的方法中,正確的是
A.加入氫氧化鈉溶液,加熱試管,再滴入酚酞試液
B.加入氫氧化鈉溶液,加熱試管,并用濕潤的紅色石蕊試紙接近試管口上方
C.加熱試管,并用濕潤的紅色石蕊試紙接近試管口上方
D.加水溶解,再用紅色石蕊試紙檢驗其溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列生活生產中常見物質的化學式與名稱相對應的是( )
A.FeSO47H2O﹣綠礬
B.Na2O2﹣火堿
C.BaCO3﹣重晶石
D.C6Hl2O6﹣庶糖
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(12分)鋁是應用廣泛的金屬.以鋁土礦(主要成分為Al2O3 , 含SiO2和Fe2O3等雜質)為原料制備鋁的一種工藝流程如下: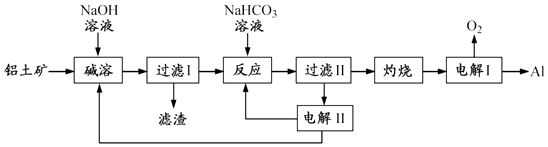
注:SiO2在“堿溶”時轉化為鋁硅酸鈉沉淀.
(1)“堿溶”時生成偏鋁酸鈉的離子方程式為 .
(2)向“過濾Ⅰ”所得濾液中加入NaHCO3溶液,溶液的pH (填“增大”、“不變”或“減小”).
(3)“電解Ⅰ”是電解熔融 Al2O3 , 電解過程中作陽極的石墨易消耗,原因是 .
(4)“電解Ⅱ”是電解Na2CO3溶液,原理如圖所示.
陽極的電極反應式為 , 陰極產生的物質A的化學式為 .
(5)鋁粉在1000℃時可與N2反應制備AlN.在鋁粉中添加少量NH4Cl固體并充分混合,有利于AlN的制備,其主要原因是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA代表阿伏加德羅常數,下列說法正確的是
A. 常溫下,5.6g鐵與足量的鹽酸反應,失去的電子數為0.2NA
B. 標準狀況下11.2L二氧化硫中含有的原于數為2NA
C. 標準狀況下,22.4L氯氣發生反應轉移電子數一定為2NA
D. 0.1mol/LCuCl2溶液中Cl-數目是0.2NA
【答案】A
【解析】 A、因為Fe和鹽酸反應氧化產物是Fe 2+ ,5.6 g鐵失去電子數為0.2 N A,選項A錯誤;B、B. 標準狀況下11.2L二氧化硫中含有的原子數為![]() 3NA=3NA,選項B錯誤;C、1 mol 氯氣參加反應時,氯氣可以只做氧化劑,也可以自身氧化還原反應,電子轉移數目可以為2NA或NA,選項C錯誤;D、溶液體積不明確,故溶液中的氯離子的個數無法計算,選項D錯誤。答案選A。
3NA=3NA,選項B錯誤;C、1 mol 氯氣參加反應時,氯氣可以只做氧化劑,也可以自身氧化還原反應,電子轉移數目可以為2NA或NA,選項C錯誤;D、溶液體積不明確,故溶液中的氯離子的個數無法計算,選項D錯誤。答案選A。
【題型】單選題
【結束】
23
【題目】實驗室利用以下反應制取少量氨氣:NaNO2+NH4Cl=NaC1+N2↑+2H2O,關于該反應的下列說法正確的是
A. NaNO2發生氧化反應
B. 每生成1molN2轉移的電子的物質的量為3mol
C. NH4Cl中的氯元素被還原
D. N2既是氧化劑,又是還原劑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com