
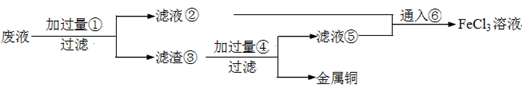
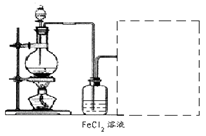
 MnCl2+Cl2↑+2H2O (2分)
MnCl2+Cl2↑+2H2O (2分) 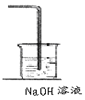 (2分)
(2分)

 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源:不詳 題型:單選題
| A.氯水和氯化亞鐵溶液 | B.鐵屑和氯化銅溶液 |
| C.鐵屑和過量稀硫酸 | D.過量鐵屑和氯化鐵溶液 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
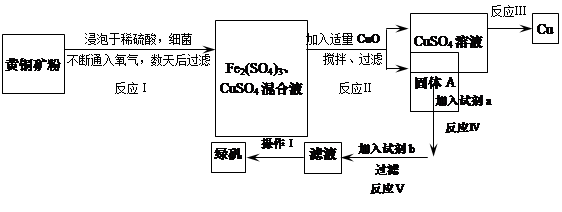
| | Fe2+ | Cu2+ | Fe3+ |
| 開始轉化成氫氧化物沉淀時的pH | 7.6 | 4.7 | 2.7 |
| 完全轉化成氫氧化物沉淀時的pH | 9.6 | 6.7 | 3.7 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題

| A.Na2SO3溶液與HNO3 | B.Na2SO3固體與濃硫酸 |
| C.固體硫在純氧中燃燒 | D.銅與熱濃H2SO4 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
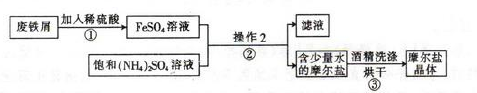
| A.酚酞 | B.石蕊 | C.甲基橙 | D.不需要 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

| 離子 | 開始沉淀時的pH | 完全沉淀時的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
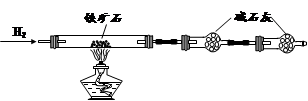
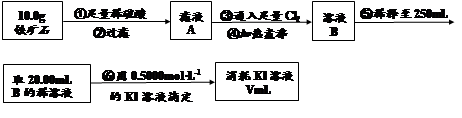
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
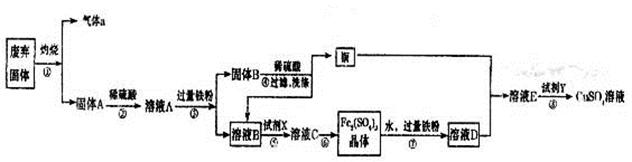
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com