
化學能與熱能、電能等能相互轉化。關于化學能與其他能量相互轉化的說法正確的是
| A.化學反應中能量變化的主要原因是化學鍵的斷裂與生成 |
| B.鋁熱反應中, 反應物的總能量比生成物的總能量低 |
| C.圖I所示的裝置能將化學能轉變為電能 |
| D.圖II所示的反應為吸熱反應 |
A
解析試題分析:化學反應中能量變化的主要原因是化學鍵的斷裂與生成,A正確;鋁熱反應是放熱反應, 所以反應物的總能量比生成物的總能量高,B不正確;圖I所示的裝置中沒有形成閉合回路,不能構成原電池,因此不能將化學能轉變為電能,C不正確;圖II所示的反應中反應物的總能量高于生成物的總能量,為放熱反應,D不正確,答案選A。
考點:考查化學反應中的能量變化、原電池的構成等
點評:該題是高考中的常見題型,屬于中等難度試題的考查。主要是考查學生對化學反應中能量變化對的原因、影響反應熱大小因素以及原電池構成條件的熟悉了解程度,旨在培養學生靈活運用基礎知識解決實際問題的能力,注意相關知識的積累和總結。


科目:高中化學 來源: 題型:單選題
已知25℃、10lkPa條件下: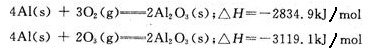
由此得出的正確結論是
| A.等質量的O2比O3能量低,由O2變O3為吸熱反應 |
| B.等質量的O2比O3能量低,由O2變O3為放熱反應 |
| C.O3比O2穩定,由O2變O3為吸熱反應 |
| D.O2比O3穩定,由O2變O3為放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
化學反應中的能量變化是由化學反應中舊化學鍵斷裂時吸收的能量與新化學鍵形成時放出的能量不同引起的。如圖為N2(g)和O2(g)反應生成NO(g)過程中的能量變化,下列說法正確的是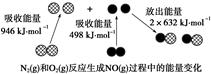
| A.1molN2(g)和NA個O2(g)反應放出的能量為180kJ |
| B.1molN2(g)和1molO2(g)具有的總能量小于2molNO(g)具有的總能量 |
| C.通常情況下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一種酸性氧化物,能與NaOH溶液反應生成鹽和水 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列反應中,生成物的總能量大于反應物的總能量的是
| A.氫氣在氧氣中燃燒 | B.焦炭在高溫下與水蒸氣反應 |
| C.鋁與三氧化二鐵高溫反應 | D.鐵絲在氧氣中燃燒 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
酒精燃燒的過程中,發生了能量的轉化。下列判斷中正確的是
| A.化學能部分轉化為熱能 | B.電能部分轉化為化學能 |
| C.熱能部分轉化為化學能 | D.光能部分轉化為化學能 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
金剛石和石墨都是碳的單質,石墨在一定條件下可以轉化為金剛石。已知12g石墨完全轉化為金剛石時,要吸收EkJ的能量,下列說法正確的是( )
| A.金剛石與石墨互為同位素 |
| B.石墨不如金剛石穩定 |
| C.金剛石與石墨互為同分異構體 |
| D.等質量的石墨與金剛石完全燃燒,金剛石放出的能量多 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
甲醇質子交換膜燃料電池中將甲醇蒸氣轉化為氫氣的兩種反應原理是
① CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0 kJ/mol
② CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9 kJ/mol
下列說法正確的是
| A.CH3OH的燃燒為吸熱反應 |
B.反應①中的能量變化如圖所示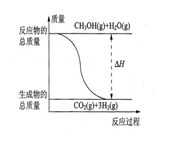 |
| C.CH3OH轉變成H2的過程一定要吸收能量 |
| D.根據②推知反應:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H >-192.9kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
合成氣(CO和H2)是重要的化工原料,在工業生產中有著廣泛的應用。
(1)工業上用甲烷和水蒸氣在高溫條件下發生反應制備合成氣(CO和H2),4g甲烷完全反應吸收51.5KJ熱量,寫該反應的熱化學方程式
(2)工業上常用合成氣來冶煉金屬,其中CO還原氧化鐵來冶煉生鐵方程式如下:
3CO(g)+Fe2O3(s) 3CO2(g)+ 2Fe(s) △H<0
3CO2(g)+ 2Fe(s) △H<0
①如果上述反應在體積不變的密閉容器中發生,當反應達到平衡時, 。
| A.容器中Fe2O3的質量不隨時間而變化 | B.反應物不再轉化為生成物 |
| C.n (CO) :n (CO2) = 1:1 | D.容器中氣體的壓強不隨時間而變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在容積固定不變的密閉容器中加入1mol N2和3mol H2發生反應:N2(g)+3H2(g) 2NH3(g) △H=" —92.4" kJ·mol-1,下列結論正確的是
2NH3(g) △H=" —92.4" kJ·mol-1,下列結論正確的是
| A.該反應達到平衡時,放出的熱量等于92.4kJ |
| B.達到平衡后向容器中通入1mol氦氣,平衡不移動 |
| C.降低溫度和縮小容器體積均可使該反應的平衡常數增大 |
| D.若達到平衡時N2的轉化率為20%,則平衡時容器內的壓強是起始時的90% |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com