
【題目】某學生對Na2SO3與AgNO3在不同pH下的反應進行探究,過程如下:
(1)調節pH,實驗記錄如下:
實驗 | pH | 現象 |
a | 10 | 產生白色沉淀,稍后溶解,溶液澄清 |
b | 6 | 產生白色沉淀,一段時間后,沉淀未溶解 |
c | 2 | 產生大量白色沉淀,一段時間后,產生海綿狀棕黑色物質X |
查閱資料得知:
I.Ag2SO3:白色,難溶于水,溶于過量Na2SO3的溶液
II.Ag2O:棕黑色,不溶于水,能和酸反應
①推測a中白色沉淀為Ag2SO3,離子方程式是____________________________。
②推測a中白色沉淀為Ag2SO4,推測的依據是_________________________________。
(2)取b、c中白色沉淀,置于Na2SO3溶液中,沉淀溶解。該同學設計實驗確認了白色沉淀不是Ag2SO4,實驗方法是:另取Ag2SO4固體置于_________溶液中,未溶解。
(3)將X從溶液中濾出、洗凈,為確認其組成,實驗如下:
I.向X中滴加稀鹽酸,無明顯變化
II.向X中加入過量濃HNO3,產生紅棕色氣體
III.用Ba(NO3)2溶液、BaCl2溶液檢驗II中反應后的溶液,前者無變化,后者產生白色沉淀
①實驗I的目的是_________________________。
②根據上述現象,分析X的性質和元素組成是__________________________。
③II中反應的化學方程式是________________________。
(4)該同學綜合以上實驗,分析產生X的原因,認為隨著酸性的增強,SO32-還原性增強,并通過進一步實驗確認了這種可能性,實驗裝置如圖所示:

①氣體Y是__________________。
②白色沉淀轉化為X的化學方程式是__________________________。
【答案】 2Ag++SO32-=Ag2SO3↓ SO32-有還原性,若被氧化為SO42-,即可與Ag+結合生成Ag2SO4沉淀 過量Na2SO3 判斷X是否是Ag2O 有還原性,含有Ag元素,不含S元素 Ag+2HNO3(濃)=AgNO3+NO2↑+H2O SO2 Ag2SO3+ H2O![]() 2Ag+H2SO4
2Ag+H2SO4
【解析】(1)①推測a中白色沉淀為Ag2SO3, Ag+與SO32-反應生成Ag2SO3, Ag2SO3溶于過量的 Na2SO3溶液,生成沉淀的離子方程式為: 2Ag++SO32-=Ag2SO3↓;正確答案: 2Ag++SO32-=Ag2SO3↓。
②推測a中白色沉淀為Ag2SO4,其根據為SO32-有還原性,可能被氧化為SO42-,與Ag+反應生成 Ag2SO4白色沉淀;正確答案:SO32-有還原性,若被氧化為SO42-,即可與Ag+結合生成Ag2SO4沉淀。
(2)Ag2SO3白色,難溶于水,溶于過量Na2SO3溶液,取B、C中白色沉淀,置于Na2SO3溶液中,沉淀溶解,說明B、C中白色沉淀為Ag2SO3;另取Ag2SO4固體,同樣條件置于足量 Na2SO3溶液中,進行對照試驗,發現沉淀不溶解;正確答案: 過量Na2SO3。
(3)①氧化銀能和鹽酸生成白色氯化銀沉淀和水, 溶液的pH=2,產生大量白色沉淀,一段時間后,產生海綿狀棕黑色物質X,向X中滴加稀鹽酸,無明顯變化,說明X不是Ag2O;正確答案:檢驗X是否為Ag2O 。
②向X中加入過量濃HNO3,產生紅棕色氣體為NO2,X與濃硝酸發生氧化還原反應,X具有還原性,X只能為金屬單質,只能為銀;因此X中含有Ag元素,不含S元素;正確答案:有還原性; 含有Ag元素,不含S元素。
③向X中加入過量HNO3(濃),產生紅棕色氣體為NO2,銀和硝酸反應,氮元素從+5變為+4價,同時生成硝酸銀和水,反應方程式為: Ag+2HNO3(濃)=AgNO3+NO2↑+H2O;正確答案:Ag+2HNO3(濃)=AgNO3+NO2↑+H2O。
(4)①海綿狀棕黑色物質X為Ag;隨著酸性的增強,+4價硫的還原性增強,能被+1價銀氧化;可通過+4價硫的氧化物二氧化硫進行實驗確認,通入二氧化硫后,瓶中白色沉淀Ag2SO3轉化為棕黑色Ag;正確答案是: SO2。
②X為Ag,白色沉淀轉化為Ag,在酸性條件下,亞硫酸銀中+4價的硫,被+1價銀氧化生成銀和硫酸,反應為: Ag2SO3+ H2O![]() 2Ag+H2SO4;正確答案:Ag2SO3+ H2O
2Ag+H2SO4;正確答案:Ag2SO3+ H2O![]() 2Ag+H2SO4。
2Ag+H2SO4。


 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學 來源: 題型:
【題目】25℃時,有關物質的電離平衡常數如下:
化學式 | CH3COOH | H2CO3 | H2SO3 |
電離平衡常數 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)請寫出H2SO3的電離平衡常數K1的表達式:________________。
(2) 常溫下,將體積為10mL pH=2的醋酸溶液與亞硫酸溶液分別加蒸餾水稀釋至1000mL,稀釋后溶液的pH,前者_____后者(填“>”、“<”或“=”)。
(3)一定條件下,冰醋酸加水稀釋過程中溶液導電能力I隨加水體積V變化曲線如右圖所示,則a、b、c三點溶液醋酸的電離程度由大到小為____________________。

(4)下列離子CH3COO-、CO32-、HSO3-、SO32-在溶液中結合H+的能力由大到小的關系為___________。
(5)體積相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三種酸溶液分別與同濃度的NaOH溶液完全中和時,消耗NaOH溶液的體積由大到小的排列順序是_____(填序號)。
(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。實驗測得稀醋酸與稀NaOH溶液反應生成1 mol H2O時放出57 kJ的熱,則醋酸溶液中,醋酸電離的熱化學方程式為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)32 g CH4,其摩爾質量為_____,約含有____mol電子,在標準狀況下所占的體積約為___L。
(2)等體積等物質的量濃度的Ca(OH)2溶液與NaHCO3溶液混合,離子方程式為:_____。
(3)H++HCO3-=H2O+CO2↑對應的一個化學方程式_______________________。
(4)制備氫氧化鐵膠體的離子方程式________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】己知下表為25℃時某些弱酸的電離平衡常數。依據所給信息判斷,下列說法正確的是
CH3COOH | HClO | H2CO3 |
Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
A. 向NaClO溶液中通入少量二氧化碳的離子方程式為:2ClO-+CO2+H2O=2HClO+CO32-
B. 相同濃度的CH3COONa和NaClO的混合溶液中,c(CH3COOH)+c(HClO)=c(OH-)-c(H+)
C. 25℃時,0.10mol·L-1Na2CO3溶液通入CO2至溶液的pH=7時,溶液中:c(Na+)=c(CO32-)+ c (HCO3-)+c(H2CO3)
D. 向0.1mol·L-1CH3COONa溶液中加入少量水,溶液中![]() 增大
增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙烯是合成食品外包裝材料聚乙烯的單體,可以由丁烷裂解制備。裂解的副反應為C4H10(g,正丁烷) ![]() CH4(g)+C3H6(g)
CH4(g)+C3H6(g)
請回答下列問題
(1)化學上,將穩定單質的能量定為0,由元素的單質化合成單一化合物時的反應熱叫該化合物的生成熱,生成熱可表示該物質相對能量。25℃、101kPa幾種有機物的生成熱如下表所示:
物質 | 甲烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 異丁烷 |
生成熱/ kJ·mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
由正丁烷裂解生成乙烯的熱化學方程式為_______________________________。
(2)一定溫度下,在恒容密閉容器中投入一定量正丁烷發生反應生成乙烯。
①下列情況能說明該反應達到平衡狀態的是__________(填標號)
A.氣體密度保持不變 B.c(C2H4)·c(C2H6)/c(C4H10)保持不變
C.反應熱保持不變 D.正丁烷分解速率利乙烷消耗速率相等
②為了提高反應速率和反應物的轉化率,可采收的措施是______________________________。
(3)向密閉容器中充入正丁烷,在一定條件(濃度、催化劑及壓強等)下發生反應,測得乙烯產率與溫度關系如圖所示。溫度高于600℃時,隨著溫度升高,乙烯產率降低,可能的原因是____________________________________________。

(4)在一定溫度下向10L恒容密閉容器中充入2mol正丁烷,反應生成乙烯和乙烷,經過10min達到平衡狀態,測得平衡時氣體壓強是原來的1.75倍。
①0~10min內乙烷的生成速率v(C2H6)=__________ mol·L-1·min-1
②上述條件下,正丁烷的平衡轉化率為______________,該反應的平衡常數K為____________。 (5)丁烷一空氣燃料電池以熔融的K2CO3(其中不含O2-和HCO3-)為電解質,以具有催化作用和導電性能的稀土金屬材料為電極。該燃料電池的正極反應式為26CO2+13O2+52e-=26CO32-,則負極反應式為_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)某學生用0.1500 mol/L NaOH溶液測定某未知濃度的鹽酸溶液,其操作可分解為如下幾步:
A.用蒸餾水洗凈滴定管
B.用待測定的溶液潤洗酸式滴定管
C.用酸式滴定管取稀鹽酸25.00 mL,注入錐形瓶中,加入酚酞
D.另取錐形瓶,再重復操作2~3次
E.檢查滴定管是否漏水
F.取下堿式滴定管用標準NaOH溶液潤洗后,將標準液注入堿式滴定管“0”刻度以上2~3 cm處,再把堿式滴定管固定好,調節液面至“0”刻度或“0”刻度以下
G.把錐形瓶放在滴定管下面,瓶下墊一張白紙,邊滴邊搖動錐形瓶直至滴定終點,記下滴定管液面所在刻度
完成以下填空:
(1)滴定時正確操作的順序是(用序號字母填寫):____→ → F → → → → D。
(2)操作F中應該選擇圖中滴定管_____(填標號)。

(3)滴定時邊滴邊搖動錐形瓶,眼睛應注意觀察_____。
(4)滴定結果如表所示:
滴定次數 | 待測液體積/mL | 標準溶液的體積/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 0.60 | 20.60 |
3 | 25.00 | 0.20 | 20.19 |
計算該鹽酸的物質的量濃度為_____(精確至0.0001)。
(5)下列操作會導致測定結果偏高的是_____。
A.堿式滴定管在裝液前未用標準NaOH溶液潤洗
B.滴定過程中,錐形瓶搖蕩得太劇烈,錐形瓶內有液滴濺出
C.堿式滴定管尖嘴部分在滴定前沒有氣泡,滴定終點時發現氣泡
D.達到滴定終點時,仰視讀數
(6)氧化還原滴定實驗與酸堿中和滴定類似(用已知濃度的氧化劑溶液滴定未知濃度的還原劑溶液或反之)。測血鈣的含量時,進行如下實驗:
①可將2mL血液用蒸餾水稀釋后,向其中加入足量草酸銨(NH4)2C2O4晶體,反應生成 CaC2O4沉淀,將沉淀用稀硫酸處理得H2C2O4溶液。
②將①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化產物為CO2,還原產物為Mn2+。
③終點時用去20mL l.0×l0﹣4 mol/L的KMnO4溶液。
Ⅰ、寫出用KMn04滴定H2C2O4的離子方程式_____________________。
Ⅱ、判斷滴定終點的方法是________________________。
Ⅲ、計算:血液中含鈣離子的濃度為_____mol/L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由一種短周期金屬元素和一種非金屬元素組成的化合物X可與水發生復分解反應。某校興趣小組用如圖裝置(夾持裝置略去)對其進行探究實驗。
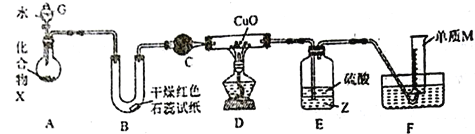
(1)儀器G的名稱是_____________________,B中紅色石蕊試紙變藍,則單質M的電子式為___________________。
(2)化合物X中含組成單質M的元素質量分數為16.9%,寫出X與水反應的化學方程式:_____________________________。
(3)C中的試劑名稱為___________________________。
(4)實驗時,裝置D中硬質玻璃管內的現象為_________________________。
(5)裝置E中試劑Z為___________(填化學式),裝置E的作用是_________________________。
(6)若不通過E、F兩裝置,請設計實驗方案證明D中發生了反應(不通過觀察D中固體顏色發生變化):__________________________________________________。
(7)若裝置A中固體樣品含有雜質(雜質不參與反應),某同學通過測定F中單質M在標準狀況下的體積和固體樣品的質量,以確定固體樣品中X的質量分數,判斷該方案是否可行,并說明原因:__________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】據權威刊物報道,1996年科學家在宇宙中發現H3分子。甲、乙、丙、丁四位學生對此報道的認識正確的是
A.甲認為上述發現絕對不可能,因為H3分子違背了共價鍵理論
B.乙認為宇宙中還可能存在另一種氫單質,因為氫元素有三種同位素必然有三種同素異形體
C.丙認為H3分子實質上是H2分子與H+以特殊共價鍵結合的產物,應寫成H
D.丁認為如果上述的發現存在,則證明傳統的價鍵理論有一定的局限性有待繼續發展
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com