
 2SO3(g) ?H=-196.6 kJ·mol-1
2SO3(g) ?H=-196.6 kJ·mol-1 2NO2(g) ?H=-113.0 kJ·mol-1
2NO2(g) ?H=-113.0 kJ·mol-1  SO3(g)+NO(g)的?H= kJ·mol-1。
SO3(g)+NO(g)的?H= kJ·mol-1。

 CH3OH(g)。CO在不同溫度下的平衡轉化率與壓強的關系如上圖(右)所示。該反應?H 0(填“>”或“ <”)。
CH3OH(g)。CO在不同溫度下的平衡轉化率與壓強的關系如上圖(右)所示。該反應?H 0(填“>”或“ <”)。 

科目:高中化學 來源:不詳 題型:單選題
 :的反應熱ΔH為 ( )
:的反應熱ΔH為 ( )| A.-1780kJ·mol-1 | B.-1220kJ·mol-1 | C.-450kJ·mol-1 | D.+430kJ·mol-1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

 2NH3 (g) ΔH<0,
2NH3 (g) ΔH<0,| T /K | 298 | 398 |
| 平衡常數K | K1 | K2 |

查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題


| A.縮小反應器容積 | B.增加Fe的物質的量 |
| C.升高溫度到900℃ | D.使用合適的催化劑 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

 2NH3(g)△H<0
2NH3(g)△H<0
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

 BaCO3(s)+SO42-(aq)
BaCO3(s)+SO42-(aq)查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題
 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H| | Fe2O3 | CO | Fe | CO2 |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
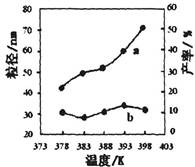
| 編號 | 溫度/K | 反應時間/h | 反應物物質的量配比 | 實驗目的 |
| ① | 378 | 4 | 3∶1 | 實驗②和④探究________ ______________________ 實驗②和__________探究 反應時間對產率的影響。 |
| ② | 378 | 4 | 4∶1 | |
| ③ | 378 | 3 | _______ | |
| ④ | 398 | 4 | 4∶1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 2SO3(g) 在一定條件下達到平衡,測得c(SO3)=0.040mol/L。則該條件下反應的平衡常數K的數值為___________,SO2的平衡轉化率為__________。
2SO3(g) 在一定條件下達到平衡,測得c(SO3)=0.040mol/L。則該條件下反應的平衡常數K的數值為___________,SO2的平衡轉化率為__________。| A.向平衡混合物中充入Ar | B.向平衡混合物中充入O2 |
| C.改變反應的催化劑 | D.降低反應的溫度 |
 2SO3(g) △H<0 , SO2的轉化率在起始溫度T1=673K下隨反應時間(t)的變化如下圖,其他條件不變,僅改變起始溫度為T2=723K,請在圖中畫出溫度T2下SO2的轉化率隨反應時間變化的預期結果示意圖。
2SO3(g) △H<0 , SO2的轉化率在起始溫度T1=673K下隨反應時間(t)的變化如下圖,其他條件不變,僅改變起始溫度為T2=723K,請在圖中畫出溫度T2下SO2的轉化率隨反應時間變化的預期結果示意圖。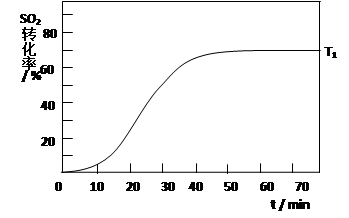
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 CO(g)+H2O(g),其化學平衡常數K和溫度t的關系如下表:
CO(g)+H2O(g),其化學平衡常數K和溫度t的關系如下表:| t(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
 2CO2+N2。為了測定在某種催化劑作用下的反應速率,在某溫度下用氣體傳感器測得不同時間的NO和CO濃度如表:
2CO2+N2。為了測定在某種催化劑作用下的反應速率,在某溫度下用氣體傳感器測得不同時間的NO和CO濃度如表:| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO) (mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com