
【題目】已知NaHSO3溶液顯酸性,溶液中存在以下平衡:HSO3﹣+H2OH2SO3+OH﹣①HSO3﹣H++SO32﹣②,向0.1molL﹣1的NaHSO3溶液中分別加入以下物質,下列有關說法正確的是( )
A.加入少量金屬Na,平衡①左移,平衡②右移,溶液中c(HSO3﹣)增大
B.加入少量Na2SO3固體,則c(H+)+c(Na+)=c(HSO3﹣)+c(OH﹣)+![]() c(SO32﹣)
c(SO32﹣)
C.加入少量NaOH溶液,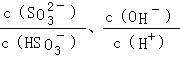 的值均增大
的值均增大
D.加入氨水至中性,則2c(Na+)=c(SO32﹣)>c(H+)=c(OH﹣)
【答案】C
【解析】A.加入少量金屬Na,Na與HSO3﹣電離出的H+反應,溶液中c(HSO3﹣)濃度減小,故A錯誤;
B.加入少量Na2SO3固體溶解后溶液中存在電荷守恒,c(H+)+c(Na+)=2c(SO32﹣)+c(HSO3﹣)+c(OH﹣),故B錯誤;
C.加入氫氧化鈉促進電離,平衡右移,抑制水解,平衡左移,c(SO32﹣),c(OH﹣)濃度增大;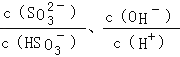 ,比值增大,故C正確;
,比值增大,故C正確;
D.0.1molL﹣1的NaHSO3溶液中加入氨水至中性,溶液中存在物料守恒,即:c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3),則c(Na+)>c(SO32﹣)>c(H+)=c(OH﹣),故D錯誤;故選C.


科目:高中化學 來源: 題型:
【題目】(1)質量之比為16∶7∶6的三種氣體SO2、CO、NO,分子數之比為________;氧原子數之比為________;相同條件下的體積之比為________。
(2)標準狀況下,1.7 g NH3的體積為________L,它與標準狀況下________L H2S含有相同數目的氫原子。
(3)某氣態氧化物的化學式為RO2,標準狀況下,1.28 g該氧化物的體積為448 mL,則該氧化物的摩爾質量為__________,R的相對原子質量為________。
(4)在同溫同壓下,2 g CO2的體積為120 mL,而2 g A氣體的體積為165 mL,則氣體A的摩爾質量為________。標準狀況下,11.2 L CO2和CO的質量是18 g,則其中含CO2的質量為________g,CO的體積為________。
(5)一儲氣瓶真空時質量為500 g。標準狀況下,充滿氧氣后質量為508 g,裝滿某氣體X后總質量為511 g。則該儲氣瓶的體積為________L,X的相對分子質量為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在下列反應中,水既未被氧化,也未被還原的是
A. 2H2O![]() 2H2↑+O2↑ B. 2F2+2H2O=4HF+O2
2H2↑+O2↑ B. 2F2+2H2O=4HF+O2
C. 3Fe+4H2O![]() Fe3O4+4H2 D. 3NO2+H2O=2HNO3+NO
Fe3O4+4H2 D. 3NO2+H2O=2HNO3+NO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】芳香酸是分子中羧基與苯環直接相連的一類有機物,通常用芳香烴的氧化來制備。反應原理如下:

反應試劑、產物的物理常數:
名稱 | 相對分子質量 | 性狀 | 熔點(℃) | 沸點(℃) | 密度(g/cm3) | 水中的溶解性 |
甲苯 | 92 | 無色液體易燃易揮發 | -95 | 110.6 | 0.8669 | 不溶 |
苯甲酸 | 122 | 白色片狀或針狀晶體 | 122.4 | 248 | 1.2659 | 微溶 |
主要實驗裝置和流程如下:

實驗方法:一定量的甲苯和KMnO4溶液里于圖l 裝置中,在90℃時,反應一段時間后,
停止反應,按如下流程分離出苯甲酸并回收未反應的甲苯。

(1)白色固體B中主要成分的分子式為________。操作Ⅱ為________。
(2)如果濾液呈紫色,需加入亞硫酸氫鉀,用離子方程式表示其原因__________。
(3)下列關于儀器的組裝或者使用正確的是__________。
A.抽濾可以加快過濾速度,得到較干燥的沉淀
B.安裝電動攪拌器時,攪拌器下端不能與三頸燒瓶底、溫度計等接觸
C.如圖 回流攪拌裝置應采用直接加熱的方法
D.冷凝管中水的流向是上進下出
(4)除去殘留在苯甲酸中的甲苯應先加入______,分液,然后再向水層中加入______,抽濾,洗滌,干燥即可得到苯甲酸。
(5)純度測定:稱取2.440g產品,配成100mL溶液,取其中25.00mL 溶液,進行滴定,消耗KOH物質的量為4.5×10-3mol。產品中苯甲酸質量分數為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有SO42-、CO32-、Cl-。為了檢驗其中是否含有SO42-,除BaCl2溶液外,還需要的溶液是 ( )
A.H2SO4B.HClC.NaOHD.NaNO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)甲烷(CH4)的摩爾質量為___________;
(2)3.2 g CH4中約含有_____________個分子、含有________mol電子,在標準狀況下所占的體積約為_________L;
(3)在標準狀況下,測得14.2 g某氣體的體積為4.48 L。則此氣體的摩爾質量為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】漢黃芩素是傳統中草藥黃芩的有效成分之一,對腫瘤細胞的殺傷有獨特作用。下列有 關漢黃芩素的敘述正確的是
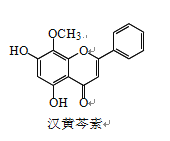
A. 漢黃芩素的分子式為 C16H13O5
B. 該物質遇 FeCl3 溶液顯色
C. 1 mol 該物質與溴水反應,最多消耗 1 mol Br2
D. 與足量 H2 發生加成反應后,該分子中官能團的種類減少 1 種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,水槽中的試管內有一枚鐵釘,放置數天觀察:
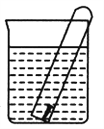
(1) 鐵釘在逐漸生銹,鐵釘的腐燭屬于______________________腐蝕。
(2) 若試管內的液面下降,則原溶液呈________性,發生________腐蝕;電極反應為負極:______________________,正極:_________________。
(3)若試管內的液面上升,則原溶液呈________性,發生________腐蝕;負極反應式為_____________,正極反應式為____________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com