
利用I2O5可消除CO污染或定量測定CO,反應為:5CO(g)+I2O5(s) 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1
(1)已知:2CO(g)+O2(g) 2CO2(g);ΔH 2
2CO2(g);ΔH 2
2I2(s)+5O2(g) 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3
則ΔH 1= (用含ΔH 2和ΔH 3的代數式表示)。
(2)不同溫度下,向裝有足量I2O5固體的2 L恒容密閉容器中通入2molCO,測得CO2的體積分數φ(CO2)隨時間t變化曲線如圖。請回答:
①從反應開始至a點時的反應速率為v(CO)= ,b點時化學平衡常數Kb= 。
②d點時,溫度不變,若將容器體積壓縮至原來的一半,請在圖中補充畫出CO2體積分數的變化曲線。
③下列說法正確的是 。(填字母序號)
| A.容器內氣體密度不變,表明反應達到平衡狀態 |
| B.兩種溫度下,c點時體系中混合氣體的平均相對分子質量相等 |
| C.增加I2O5的投料量有利于提高CO的轉化率 |
| D.b點和d點的化學平衡常數:Kb<Kd |
(1)2.5ΔH2-0.5ΔH3(3分)
(2)①0.6mol·L-1·min-1(2分,不帶單位扣1分),1024 或者45(3分)
②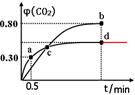
③AB(2分,選對一個得1分,有錯選得0分)
(3)8.96%(3分,三位有效數字,錯誤扣1分)
解析試題分析:(1)根據蓋斯定律,對照第1個反應和第2個反應中CO,對照第1個反應和第3個反應中I2或I2O5,可得ΔH 1=2.5ΔH2-0.5ΔH3。
(2)①設轉化的CO物質的量濃度為x,根據三段式進行計算:
5CO(g)+I2O5(s) 5CO2(g)+I2(s)
5CO2(g)+I2(s)
起始濃度(mol?L?1) 1 0
轉化濃度(mol?L?1) x x
平衡濃度(mol?L?1) 1-x x
a點CO2的體積分數為0.3,則x/1=0.3,可得x=0.3mol?L?1,則v(CO)=0.3mol/L÷0.5min = 0.6mol·L-1·min-1;類似a點計算,可求出b點CO的平衡濃度為0.2mol?L?1,CO2的 平衡濃度為0.8mol?L?1,則b點時化學平衡常數Kb=c5(CO2)÷c5(CO)=0.85÷0.25=45。
②d點時,溫度不變,若將容器體積壓縮至原來的一半,壓強增大,因為該反應前后氣體的系數相等,所以增大壓強,平衡不移動,CO2的體積分數不變,可畫出CO2體積分數的變化曲線。
③A、容器內氣體密度不變,說明氣體的質量不變,則反應達到平衡狀態,正確;B、c點時兩溫度下CO2的體積分數相等,說明氣體組成相同,則體系中混合氣體的平均相對分子質量相等,正確;C、因為I2O5為固體,增加I2O5的投料量,CO的轉化率不變,錯誤;D、b點CO2的體積分數大,說明b點平衡常數大,所以Kb > Kd,錯誤。
(3)根據化學方程式可得對應關系:5CO ~ I2~2Na2S2O3,n(CO)=5/2n(Na2S2O3)=5/2×0.0100mol·L-1×0.02L×4=0.002mol,則樣品氣中CO的體積分數為:0.002mol×22.4L/mol÷0.5L×100%=8.96%
考點:本題考查蓋斯定律、化學反應速率的計算、化學平衡的判斷和計算、體積分數的計算。


科目:高中化學 來源: 題型:單選題
氨氧化制硝酸的反應如下(未配平):①NH3 + O2 →NO + H2O ②NO + O2 → NO2
③NO2+H2O→HNO3+NO,如將氨全部氧化得2mol硝酸,理論上需氧氣的物質的量是( )
| A.2mol | B.3 mol | C.4 mol | D.5 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知銅和濃硫酸可以在加熱條件下發生如下反應(反應方程式已配平):
Cu+2H2SO4(濃)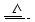 CuSO4+A↑+2H2O
CuSO4+A↑+2H2O
試通過計算和推理完成下面的問題:
(1)A物質可以導致酸雨的形成。則A應該屬于 (用字母代號填寫)
A.酸 B.堿 C.鹽 D.酸性氧化物 E.堿性氧化物
A物質可以使酸性KMnO4溶液褪色,此反應中 (填寫化學式,下同)失去電子,氧化劑是 。
(2)若A物質通入品紅溶液,觀察到溶液褪色,說明A物質具有 (填序號,下同);若A物質通入Na2S溶液,觀察到溶液中出現淡黃色渾濁,說明SO2具有 。
A.氧化性 B.還原性 C.漂白性
若A物質通入雙氧水,請大膽判斷所得溶液是 (填溶質的化學式)
(3)一定量的銅片與100mL 18mol/L 的濃H2SO4充分反應,如果該反應過程中轉移了0.2mol電子,生成的A氣體在標準狀況下體積為 L (假設氣體全部逸出)。若用4 mol·L-1的NaOH溶液吸收生成的A,并生成正鹽,寫出發生的反應方程式 計算需要NaOH溶液的體積 L。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
請將5種物質:N2O、FeCl2、Fe(NO3)3、HNO3和FeCl3分別填入下面對應的橫線上,組成一個未配平的化學方程式。
(1) + → + + +H2O(不需配平)
(2)反應過程中,N2O與FeCl2的物質的量之比為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
過氧化鈣晶體[CaO2·8H2O]較穩定,呈白色,微溶于水,能溶于酸性溶液。廣泛應用于環境殺菌、消毒等領域。
★過氧化鈣晶體的制備
工業上生產CaO2·8H2O的主要流程如下: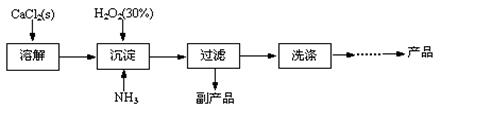
(1)用上述方法制取CaO2·8H2O的化學方程式是 。
(2)沉淀時常用冰水控制溫度在10℃以下和通入過量的NH3,其可能原因分別是
① ;② 。
★過氧化鈣晶體含量的測定
準確稱取0.3000g產品于錐形瓶中,加入30 mL蒸餾水和10 mL 2.000 mol·L-1 H2SO4,用0.0200mol·L—1 KMnO4標準溶液滴定至終點。重復上述操作兩次。H2O2和KMnO4反應的離子方程式為2MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O
(3)滴定終點觀察到的現象為 。
(4)根據表1數據計算產品中CaO2·8H2O的質量分數(寫出計算過程):
| 滴定次數 | 樣品的質量/g | KMnO4溶液的體積/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.3000 | 1.02 | 24.04 |
| 2 | 0.3000 | 2.00 | 25.03 |
| 3 | 0.3000 | 0.20 | 23.24 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
近年來地質、環境災難頻頻發生,為防止在大災之后疫病流行,災區需要大量的各種消毒劑、漂白劑等。
(1)二氧化氯是目前國際上公認的第四代高效、無毒的廣譜消毒劑,它可由KClO3與SO2在H2SO4作用下反應制得。請寫出反應的離子方程式: 。
(2)過碳酸鈉是一種新型固態漂白劑,化學式可表示為Na2CO3·3H2O2,它具有Na2CO3和H2O2的雙重性質。過碳酸鈉與下列物質均會發生化學反應而失效,其中過碳酸鈉只發生了氧化反應的是 。
| A.MnO2 | B.KMnO4溶液 | C.稀鹽酸 | D.Na2SO3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氧化還原反應在生產、生活中具有廣泛的用途,貫穿古今。
(1)水是人體的重要組成成分,是人體中含量最多的一種物質。而“四種基本反應類型
與氧化還原反應的關系”也可用如圖表達。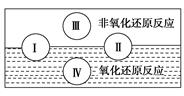
試寫出有水參加的符合反應類型Ⅳ的一個化學方程式:________________________,其中水為________劑。
(2)氯化銨常用作焊接。如:在焊接銅器時用氯化銨除去銅器表面的氧化銅以便焊接,其反應為:
CuO+____NH4Cl Cu+____CuCl2+N2↑+____H2O。
Cu+____CuCl2+N2↑+____H2O。
①配平此氧化還原反應方程式。
②該反應中,被氧化的元素是________(填元素名稱),氧化劑是________(填化學式)。
(3)(2011·福建高考卷節選)磷酸鈣與焦炭、石英砂混合,在電爐中加熱到1 500 ℃生成白磷,反應為:
2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10,10C+P4O10=P4+10CO。
每生成1 mol P4時,就有________mol電子發生轉移。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
將5.5 g鐵鋁混合物粉末加入900mL 1.00 mol/L HNO3溶液中,充分反應后,得a L(標準狀況)NO氣體。
(1)HNO3是否過量___________。
(2)若a=3.36L(標準狀況),則混合物中鋁的質量分數為_________%。
(3)若a=3.36L(標準狀況),往反應后的溶液中加入___________ mL 1.000 mol/L NaOH溶液時生成的沉淀量最大,還要加________ mL 1.000 mol/L NaOH溶液才能使沉淀的量保持不變。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
環境中常見的重金屬污染物有:汞、鉛、錳、鉻、鎘。處理工業廢水中含有的Cr2O72-和CrO42-,常用的方法有兩種。
方法1 還原沉淀法
該法的工藝流程為 。
。
其中第①步存在平衡2CrO42-(黃色)+2H+ Cr2O72-(橙色)+H2O。
Cr2O72-(橙色)+H2O。
(1)寫出第①步反應的平衡常數表達式_________________________________。
(2)關于第①步反應,下列說法正確的是________。
A.通過測定溶液的pH可以判斷反應是否已達平衡狀態
B.該反應為氧化還原反應
C.強酸性環境,溶液的顏色為橙色
(3)第②步中,還原0.1 mol Cr2O72-,需要________mol的FeSO4·7H2O。
(4)第③步除生成Cr(OH)3外,還可能生成的沉淀為________。在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq),常溫下,Cr(OH)3的溶度積Ksp=10-32,當c(Cr3+)降至10-5 mol·L-1時,認為c(Cr3+)已經完全沉淀,現將第③步溶液的pH調至4,請通過計算說明Cr3+是否沉淀完全(請寫出計算過程):____________________________________________________________________________。
Cr3+(aq)+3OH-(aq),常溫下,Cr(OH)3的溶度積Ksp=10-32,當c(Cr3+)降至10-5 mol·L-1時,認為c(Cr3+)已經完全沉淀,現將第③步溶液的pH調至4,請通過計算說明Cr3+是否沉淀完全(請寫出計算過程):____________________________________________________________________________。
方法2 電解法
(5)實驗室利用如圖裝置模擬電解法處理含Cr2O72-的廢水,電解時陽極反應式為________,陰極反應式為________,得到的金屬陽離子在陰極區可沉淀完全,從水的電離平衡角度解釋其原因是___________________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com