
亞硝酸鈉(NaNO2)是重要的防腐劑。某化學興趣小組嘗試制備亞硝酸鈉,查閱資料:①HNO2為弱酸,在酸性溶液中,NO2-可將MnO4-還原為Mn2+且無氣體生成。
②NO不與堿反應,可被酸性KMnO4溶液氧化為硝酸
探究一 亞硝酸鈉固體的制備
以碳和濃硝酸為起始原料,設計如下裝置利用一氧化氮與過氧化鈉反應制備亞硝酸鈉。(反應方程式為2NO+Na2O2=2NaNO2,部分夾持裝置和A中加熱裝置已略)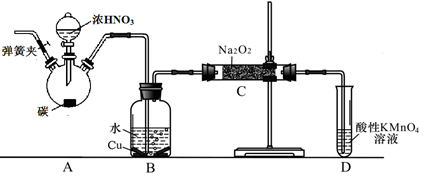
(1)寫出裝置A燒瓶中發生反應的化學方程式 。
(2)有同學認為裝置C中產物不僅有亞硝酸鈉,還有碳酸鈉和氫氧化鈉,為排除干擾應在B、C裝置間增加裝置E,E中盛放的試劑應是 (填字母)。
A.濃H2SO4 B.堿石灰 C.無水CaCl2
探究二 亞硝酸鈉固體含量的測定及性質驗證
稱取裝置C中反應后的固體4.000g溶于水配成250mL溶液,取25.00mL溶液于錐形瓶中,用0.1000
mol/L酸性KMnO4溶液進行滴定,實驗所得數據如下表所示:
| 滴定次數 | 1 | 2 | 3 | 4 |
| KMnO4溶液體積/mL | 20.60 | 20.02 | 20.00 | 19.98 |
(1)C +4HNO3 (濃) CO2↑+ 4NO2↑+ 2H2O (3分) (2)B(2分)
CO2↑+ 4NO2↑+ 2H2O (3分) (2)B(2分)
(3)A、C(2分)(4)86.25%(2分) (5)c(Na+)>c(NO2-)>c(Cl-)>c(H+)>c(OH-)(2分)
(6)A (2分) 2NO3- +6H2O +10e-=N2↑+12OH- (3分)
解析試題分析:(1)濃硝酸既有強氧化性,能把單質碳氧化生成CO2,而硝酸被還原為NO2,同時還有水生成,因此裝置A燒瓶中發生反應的化學方程式為C +4HNO3 (濃) CO2↑+ 4NO2↑+ 2H2O。
CO2↑+ 4NO2↑+ 2H2O。
(2)A裝置中產生的NO2和CO2通入到B裝置中,由于NO2溶于水生成NO和硝酸,在酸性條件下CO2的溶解度很小,因此從B裝置中出來的NO氣體中含有CO2以及水蒸氣,二者與過氧化鈉反應生成碳酸鈉、氫氧化鈉,因此要排出干擾,需要除去CO2和水蒸氣。濃硫酸和氯化鈣只能吸收水蒸氣,堿石灰既可以吸收水蒸氣,還能吸收CO2,因此答案選B。
(3)第一組實驗與其它組實驗相比,消耗高錳酸鉀溶液的體積偏多。A、酸式滴定管用蒸餾水洗凈后未用標準液潤洗,則高錳酸鉀溶液的濃度被稀釋,因此消耗高錳酸鉀溶液的體積增加,A正確;B、錐形瓶洗凈后未干燥,不影響測定結果,B不正確;C、滴定終了仰視讀數,則讀數偏大,因此消耗高錳酸鉀溶液的體積偏大,C正確,答案選AC。
(4)根據表中數據可知,三次實驗中消耗高錳酸鉀溶液體積的平均值=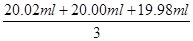 =20.00ml。在反應中Mn元素的化合價從+7價降低到+2價,得到5個電子。N元素的化合價從+3價升高到+5價,失去2個電子,因此根據電子得失守恒可知25.00mL待測液中亞硝酸鈉的物質的量=0.1000
=20.00ml。在反應中Mn元素的化合價從+7價降低到+2價,得到5個電子。N元素的化合價從+3價升高到+5價,失去2個電子,因此根據電子得失守恒可知25.00mL待測液中亞硝酸鈉的物質的量=0.1000
mol/L×0.0200L×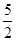 =0.00500mol,則原樣品中亞硝酸鈉的物質的量=0.00500mol×
=0.00500mol,則原樣品中亞硝酸鈉的物質的量=0.00500mol× =0.0500mol,其質量=0.0500mol×69g/mol=3.45g,所以亞硝酸鈉的質量分數=
=0.0500mol,其質量=0.0500mol×69g/mol=3.45g,所以亞硝酸鈉的質量分數=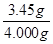 ×100%=86.25%。
×100%=86.25%。
(5)鹽酸的酸性強于亞硝酸的,因此將0.2mol·L-1的亞硝酸鈉溶液和0.1mol·L-1的鹽酸等體積混合后生成亞硝酸、氯化鈉,其中亞硝酸鈉過量,且生成的亞硝酸與過量的亞硝酸鈉以及氯化鈉的物質的量濃度均相等,都是0.05mol/L。由于溶液顯酸性,這說明亞硝酸的電離程度大于亞硝酸鈉的水解程度,因此溶液中離子濃度大小關系是c(Na+)>c(NO2-)>c(Cl-)>c(H+)>c(OH-)。
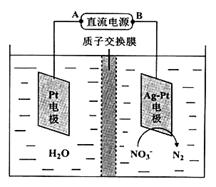
(6)根據電解池可知,硝酸轉化為氮氣,氮元素的化合價降低,硝酸得到電子,被還原,因此Ag-Pt電極是陰極,則B是電源的負極,所以A是電源的正極。又因為25℃時,反應進行10min,溶液的pH由7變為12,這說明反應中有OH-產生,所以陰極電極反應式為2NO3- +6H2O +10e-=N2↑+12OH-。
考點:考查濃硝酸的性質、氣體的凈化、滴定實驗判斷、計算與誤差分析、溶液中離子濃度大小比較以及電化學原理的應用與判斷


科目:高中化學 來源: 題型:填空題
硫酸是強酸,中學階段將硫酸在水溶液中看作完全電離。但事實是,硫酸在水中的第一步電離是完全的,第二步電離并不完全,其電離情況為:H2SO4=H++HSO4-,HSO4- H+ + S042-。
H+ + S042-。
請回答下列有關問題:
(1)Na2SO4溶液呈_(填“弱酸性”、“中性”或“弱堿性”),其理由是_
(用離子方程式表示)。
(2)H2SO4溶液與BaC12溶液反應的離子方程式為_ 。
(3)在0.l0mol·L-1的Na2SO4溶液中,下列離子濃度關系正確的是_ (填寫編號)。
| A.c(Na+)=c(SO42-)+c(HSO4一)+c(H2SO4) |
| B.c(OH-)="c(" HSO4-)+c(H+) |
| C.c( Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-) |
| D.c( Na+)=2c(SO42-)+2c(HSO4-) |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
化學能與電能之間的相互轉化與人的生活實際密切相關,在生產、生活中有重要的應用,同時也是學生形成化學學科素養的重要組成部分。
(1)熔融狀態下,鈉的單質和氯化亞鐵能組成可充電電池(如圖1),反應原理為:2Na+FeCl2 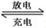 Fe+2NaCl,該電池放電時,正極反應式為 ________________ _____:
Fe+2NaCl,該電池放電時,正極反應式為 ________________ _____:
充電時,__________(寫物質名稱)電極接電源的負極;
該電池的電解質為________ _。
(2)某同學用銅片、石墨作電極電解一定濃度的硫酸銅溶液(如圖2),一段時間停止通電取出電極。若在電解后的溶液中加入0.98g氫氧化銅粉末恰好完全溶解,經測定所得溶液與電解前完全相同。請回答下列問題:
①Y電極材料是 ,發生 (填“氧化或還原”)反應。
②電解過程中X電極上發生的電極反方應式是:
③如在電解后的溶液中加入足量的小蘇打,充分反應后產生氣體在標準狀況下所占的體積是
(3)常溫時,BaSO4的Ksp=1.08×10-10,現將等體積的BaCl2溶液與2.0×10-3mol/l的Na2SO4
溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小濃度為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(12分)某學生用0.1000mol·L-1標準NaOH溶液滴定未知濃度的鹽酸,其操作可分解為以下幾步:
A移取25.00mL待測鹽酸溶液注入潔凈的錐形瓶中,并加入2~3滴酚酞溶液
B用標準NaOH溶液潤洗滴定管2~3次
C把盛有標準NaOH溶液的堿式滴定管固定好,擠壓玻璃珠,使滴定管尖嘴充滿溶液
D取標準NaOH溶液注入堿式滴定管到“0”刻度以上2~3cm
E.調節液面至“0”或“0”刻度以下,記下讀數
F.把錐形瓶放在滴定管的下面,用標準NaOH溶液滴定到終點,并記下滴定管液面的讀數
(1)下圖中屬于堿式滴定管的 (選填:“甲”、“乙”)。
(2)正確的操作順序是 (填字母序號)。
(3)上述B步操作的目的是 。
(4)判斷到達滴定終點的實驗現象是 。
(5)上述A步操作之前,若先用待測溶液潤洗錐形瓶,則對滴定結果的影響是 (填“偏大”或“偏小”或“無影響”)。
(6)若平行實驗三次,記錄的數據如下表
| 滴定次數 | 待測溶液的體積(/mL) | 標準NaOH溶液的體積 | |
| 滴定前讀數(/mL) | 滴定后讀數(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
酸堿中和滴定是利用中和反應,用已知濃度的酸(或堿)來測定未知濃度的堿(或酸)的實驗方法,其中溶液的pH變化是判斷滴定終點的依據。
(1)為了準確繪制上圖,在滴定開始時和________,滴液速度可以稍快一點,測試和記錄pH的間隔可大些;當接近________時,滴液速度應該慢一些,盡量每滴一滴就測試一次。
(2)在圖中A的pH范圍使用的指示劑是____________;C的pH范圍使用的指示劑是________________;D區域為________________。
(3)用0.1 032 mol·L-1的鹽酸溶液滴定未知濃度的氫氧化鈉溶液,重復三次的實驗數據如下表所示:
| 實驗序號 | 消耗0.1 032 mol·L-1的鹽酸溶液的體積/mL | 待測氫氧化鈉溶液的體積/mL |
| 1 | 28.84 | 25.00 |
| 2 | 27.83 | 25.00 |
| 3 | 27.85 | 25.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某同學用0.10 mol/L的HCl溶液測定未知濃度的NaOH溶液,其實驗操作如下:
| A.用酸式滴定管量取20.00 mL HCl溶液注入錐形瓶,同時滴加2-3滴酚酞試液; |
| B.用0.10 mol/L的HC!溶液潤洗酸式滴定管; |
| C.把滴定管用蒸餾水洗凈; |
| D.取下堿式滴定管,用待測NaOH溶液潤洗后,將待測NaOH溶液注入堿式滴定管至距離刻度“0”以上20 cm處,再把堿式滴定管固定好,調節液面; |

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某課外興趣小組欲測定某NaOH溶液的濃度,其操作步驟如下:
①將堿式滴定管用蒸餾水洗凈,待測溶液潤洗后,再注入待測溶液,調節滴定管的尖嘴部分充滿溶液,并使液面處于"0"刻度以下的位置,記下讀數;將錐形瓶用蒸餾水洗凈后,用待測溶液潤洗錐形瓶2~3次;從堿式滴定管中放入20.00mL待測溶液到錐形瓶中。
②將酸式滴定管用蒸餾水洗凈,再用標準酸液潤洗2-3次后,向其中注入0.1000 mol/L標準鹽酸,調節滴定管的尖嘴部分充滿溶液,并使液面處于"0"刻度以下的位置,記下讀數。
③向錐形瓶中滴入酚酞作指示劑,進行滴定。滴定至指示劑剛好變色,且半分鐘內顏色不再改變為止,測得所耗鹽酸的體積為V1mL。
④重復以上過程,但在滴定過程中向錐形瓶加入5mL的蒸餾水,測得所耗鹽酸的體積為V2 mL。試回答下列問題:
(1)錐形瓶中的溶液從 色變為 色時,停止滴定。
(2)該小組在步驟①中的錯誤是 ,
由此造成的測定結果 (偏高、偏低或無影響)。
(3)如圖,是某次滴定時的滴定管中的液面,其讀數為 mL。
(4)根據下列數據:
| 滴定次數 | 待測液體積(mL) | 標準鹽酸體積(mL) | |
| 滴定前讀數(mL) | 滴定后讀數(mL) | ||
| 第一次 | 20.00 | 0.50 | 22.60 |
| 第二次 | 20.00 | 1.00 | 24.50 |
| 第三次 | 20.00 | 2.10 | 24.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
粗CuO是將工業廢銅、廢銅合金等高溫焙燒而成的,雜質主要是鐵的氧化物及泥沙。以粗CuO為原料制備膽礬的主要流程如下:
已知Fe3+、Fe2+ 、Cu2+轉化為相應氫氧化物時,開始沉淀和沉淀完全時的pH如下表:
| | Fe3+ | Fe2+ | Cu2+ |
| 開始沉淀時的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀時的pH | 3.7 | 9.6 | 6.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
鎳鎘(Ni-Cd)可充電電池在現代生活中有廣泛應用。已知某鎳鎘電池的電解質溶液為KOH溶液,其充、放電按下式進行:Cd+2NiOOH+2H2O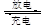 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
有關該電池的說法正確的是( )
| A.充電過程是化學能轉化為電能的過程 |
| B.充電時陽極反應:Ni(OH)2-e-+OH-=NiOOH+H2O |
| C.放電時負極附近溶液的堿性增強 |
| D.放電時電解質溶液中的OH-向正極移動 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com