
許多硫的含氧酸鹽在醫藥、化工等方面有著重要的用途。
(1))重晶石(BaS04)常作胃腸道造影劑。
已知:常溫下,Ksp(BaSO4)=1.1×10-10,向BaSO4懸濁液中加入硫酸,當溶液的pH=2時, 溶液中 c(Ba2+)= 。
(2)硫酸亞鐵銨晶體[(NH4)2Fe(SO4)2·6H20]常作分析劑。
①檢驗晶體中含有NH4+的方法為_______。
②等物質的量濃度的四種稀溶液:
a.(NH4)2Fe(SO4)2 b.NH4HSO4 c.(NH4)2SO4 d.(NH4)2SO3
其中C(NH4+)由大到小的順序為 (填選項字母)。
(3)過二硫酸鉀(K2S2O8)常作強氧化劑,Na2S2O3常作還原劑。
①K2S2O8溶液與酸性MnSO4溶液混合,在催化劑作用下,可以觀察到溶液變為紫色, 該反應的離子方程式為
②用鉑作電極,電解H2SO4和K2SO4的混合溶液可以制備K2S2O8,其陽極的電極反應式為_____ __電解過程中陰極附近溶液的pH將______ (填“增大”、“減小”或“不變”)
③產品中K2S2O8的含量可用碘量法測定。操作步驟為:稱取0.3g產品于碘量瓶中,加50 mL水溶解;加入4.000 g KI固體(稍過量),振蕩使其充分反應;加入適量醋酸溶液酸化,以______為指示劑,用0.1000 mol·L-1 Na2S2O3標準液滴定至終點(已知:I2+2S2O32-=2I-+S4O62-)。重復2次,測得平均消耗標準液21.00mL。該產品中K2S2O8的質量分數為(雜質不參加反應) (列式并計算)。
(1)2.2×10-8 mol/L (2分)
(2)① 取少量晶體,加水溶解,再加入足量NaOH濃溶液加熱,生成能使濕潤的紅色石蕊試紙變藍的氣體,則有NH4+。(其它合理答案也給分) (2分)
② a>c>d>b (2分,寫成a c d b 或b<d<c<a也可給分,但寫成b d c a不給分)
(3)① 5S2O82-+2Mn2++8H2O催化劑10SO42-+2MnO4-+16H+ (2分)
② 2SO42- -2e-=S2O82-(或2HSO4- -2e- = S2O82-+2H+) (2分)
增大 (1分)
③淀粉 (1分)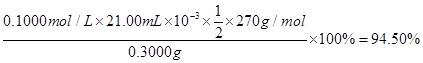
(3分,列式2分,結果1分。列式中不帶單位不扣分,寫成94.5%亦不扣分。)
解析試題分析:(1)pH=2時,c(SO42-)=0.5×10-2mol/L,Ksp(BaSO4)=c(Ba2+)·c(SO42-)=1.1×10-10,則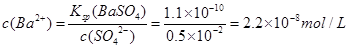 。
。
(2)①NH4+的檢驗通常是加堿,使其轉化為氨氣,用濕潤的石蕊試紙檢驗氨氣。
②NH4+是弱堿陽離子,在水中可水解使溶液顯酸性。a中NH4+與Fe2+的水解相互抑制,c中NH4+正常水解,d中NH4+與SO32-水解相互促進,因此c(NH4+)由大到小為a>c>d。因a、c、d分子中都有2個銨根離子,而b分子中只有1個銨根離子,水解畢竟是微弱的,因此b中的c(NH4+)最小,故整體順序為a>c>d>b。
(3)①溶液變紫色說明有高猛酸根生成,過二硫酸根被還原為硫酸根。
②電解時,陰離子在陽極失電子,故電極反應式為2SO42- -2e-=S2O82-。陰極陽離子得電子,發生反應為2H++2e—=H2↑,氫離子減少溶液酸性減弱,pH升高。
③根據題中所述滴定原理,Na2S2O3標準液用來滴定碘單質,碘遇淀粉變藍,因此用淀粉作指示劑。
滴定時發生的反應有:S2O82—+2I—=2SO42—+I2,I2+2S2O32-=2I-+S4O62-,則有S2O82—~2S2O32-,因此產品中K2S2O8的質量為0.1000×21×10-3×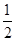 ×270=0.2835g,產品中K2S2O8的質量分數為
×270=0.2835g,產品中K2S2O8的質量分數為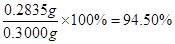 。
。
考點:考查溶度積的計算,鹽類的水解,離子檢驗,電解池原理,中和滴定原理。


科目:高中化學 來源: 題型:填空題
工業上用電解飽和NaCl溶液的方法來制取NaOH、Cl2和H2,并以它們為原料生產一系列化工產品,稱為氯堿工業。
(1)若采用無隔膜法電解冷的食鹽水時,Cl2會與NaOH充分接觸,導致產物僅是NaClO和H2。無隔膜法電解冷的食鹽水相應的離子方程式為 。
(2)氯堿工業耗能高,一種將電解池與燃料電池相組合的新工藝可以節(電)能30%以上。在這種工藝設計中,相關物料的傳輸與轉化關系如下圖所示,其中的電極未標出,所用的離子膜都只允許陽離子通過。
①經精制的飽和NaCl溶液應從圖中電解池的 (填寫“左” 或“右”)池注入。
②圖中X是____ __(填化學式);乙中右室的電極反應式為: _ ,圖示中氫氧化鈉溶液質量分數a%與b%的關系是 (填字母)。
A. a%=b% B. a%﹥b% C. a%﹤b%
③甲中的離子交換膜為 (填“陽離子交換膜”或“陰離子交換膜”)。
(3)氯堿工業的產物NaOH與不同物質反應可以生成不同的鹽。已知常溫下,濃度均為0.1 mol/L的4種鈉鹽溶液pH如下表:
| 溶質 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
水體中重金屬鉛的污染問題備受關注。水溶液中鉛的存在形態主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形態的濃度分數α隨溶液pH變化的關系如下圖所示: 
(1)Pb(NO3)2溶液中, ________2(填“>”“=”或“<”);往該溶液中滴入氯化銨溶液后,
________2(填“>”“=”或“<”);往該溶液中滴入氯化銨溶液后, 增加,可能的原因是________________________________。
增加,可能的原因是________________________________。
(2)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8時溶液中存在的陽離子(Na+除外)有__________,pH=9時主要反應的離子方程式為_______________________。
(3)某課題組制備了一種新型脫鉛劑,能有效去除水中的痕量鉛,實驗結果如下表:
| 離子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 處理前濃度/(mg·L-1) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 處理后濃度/(mg·L-1) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
 E2Pb(s)+2H+則脫鉛的最合適pH范圍為( )
E2Pb(s)+2H+則脫鉛的最合適pH范圍為( )查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫化鈉是重要的工業原料。
(1)高溫時,等物質的量甲烷與硫酸鈉在催化劑作用下恰好完全反應,制得硫化鈉。反應的化學方程式為__________________。
(2)甲同學往某Na2S樣品(含Na2CO3、Na2SO4雜質)溶液中加人少量BaS溶液,產生白色沉淀,過濾,向濾渣中加人過量鹽酸,沉淀完全溶解。由此得出結論:相同溫度下,Ksp(BaCO3)<Ksp(BaSO4)。
①沉淀溶于鹽酸的離子方程式是__________________。
②僅由上述實驗無法判斷Ksp(BaCO3)與Ksp(BaSO4)的大小關系,理由是______。
(3)利用Na2S為沉淀劑由鋅灰可制得ZnS。鋅灰經稀硫酸浸取后所得浸取液含Zn2+、Cd2+、Al3+、Fe2+, Fe3+等,由該浸取液制備ZnS的工藝流程如下圖所示。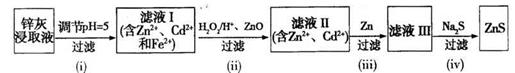
①步驟(i)所得濾渣中含有鋁元素的物質為______(填化學式)。
②步驟(ii)所加ZnO的作用為____________。
③步驟(iii)中得到Cd單質的離子方程式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
重鉻酸鹽廣泛用作氧化劑、皮革制作等。以鉻礦石(主要成分是Cr2O3,含FeO、Al2O3、 SiO2等雜質)為原料制取重鉻酸鈉的流程如下:
請回答下列問題:
(1)寫出Cr2O3在高溫焙燒時反應的化學方程式______________________
(2)寫出硫酸酸化使Na-2CrO4轉化為Na2Cr2O7的離子方程式 ______________。
(3)某工廠采用石墨電極電解Na2CrO4溶液,實 現了 Na2CrO4到 Na2Cr2O7的轉化,其原理如圖所示。
①鈉離子交換膜的一種材料是聚丙烯酸鈉( ),聚丙烯酸鈉單體的結構簡式是________;
),聚丙烯酸鈉單體的結構簡式是________;
②寫出陽極的電極反應式__________
(4) Na2Cr2O7可用于測定廢水的化學耗氧量(即COD,指每升水樣中還原性物質被氧化 所需要O2的質量)。現有某水樣100.00 mL,酸化后加入C1 mol/L的Na2Cr2O7溶液 V1 mL,使水中的還原性物質完全被氧化(Cr2O72-還原為Cr3+);再用C2mol/L的FeSO4溶液滴定剩 余的Cr2O72-,結果消耗FeSO4溶液V2 mL。
①該水樣的COD為______________mg/L;
②假設上述反應后所得溶液中Fe3+和Cr3+的物質的量濃度均為0.1 mol/L,要使Fe3 +沉 淀完全而Cr3+還未開始沉淀.則需調節溶液pH的范圍是 _______.
(可能用到的數據:KSPFe(OH)3=4.0×10-38, KSPCr(OH)3=6.0×10-31,
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D四種物質溶于水均完全電離,電離出的離子如下表。
| 陽離子 | Na+、Al3+、Ba2+、H+、NH4+ |
| 陰離子 | SO42-、OH-、CO32-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(15分)
制燒堿所用鹽水需兩次精制。第一次精制主要是用沉淀法除去粗鹽水中Ca2+、Mg2+、Fe3+、SO42-等離子,過程如下:
Ⅰ. 向粗鹽水中加入過量BaCl2溶液,過濾;
Ⅱ. 向所得濾液中加入過量Na2CO3溶液,過濾;
Ⅲ. 濾液用鹽酸調節pH,獲得一次精制鹽水。
(1)過程Ⅰ除去的離子是______。
(2)過程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如下表:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |

查看答案和解析>>
科目:高中化學 來源: 題型:計算題
已知在室溫時,Mg(OH)2的溶度積Ksp=5.6×10-12 (mol/L)3,要使0.2mol/lMgSO4溶液中的Mg2+沉淀較為完全[c(Mg2+)<5.6×10-6mol/L],則應向溶液中加入NaOH溶液,使溶液的pH最小為多少?
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
實驗室用NaOH固體配制0.1 000mol·L-1NaOH溶液500mL.
(1)用托盤天平稱取NaOH固體________g.溶液配制過程用到下列玻璃儀器,按首次使用的先后順序依次是________ (填儀器選項符號)
A.玻璃棒 B.膠頭滴管 C.燒杯 D.500mL容量瓶
(2)用所配制的0.1000mol·L-1NaOH溶液通過中和滴定測定一元弱酸HA溶液濃度,每次滴定取用的HA溶液均為20.00mL,使用酚酞溶液為指示劑,滴定終點的標志是____________________________。滴定的實驗數據記錄:
| 滴定次數 | NaOH溶液體積(mL) | |
| V1 | V2 | |
| 1 | 3.05 | 44 |
| 2 | 1.45 | 41.5 |
| 3 | 7.65 | 47.6 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com