
水體中重金屬鉛的污染問題備受關注。水溶液中鉛的存在形態主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形態的濃度分數α隨溶液pH變化的關系如下圖所示: 
(1)Pb(NO3)2溶液中, ________2(填“>”“=”或“<”);往該溶液中滴入氯化銨溶液后,
________2(填“>”“=”或“<”);往該溶液中滴入氯化銨溶液后, 增加,可能的原因是________________________________。
增加,可能的原因是________________________________。
(2)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8時溶液中存在的陽離子(Na+除外)有__________,pH=9時主要反應的離子方程式為_______________________。
(3)某課題組制備了一種新型脫鉛劑,能有效去除水中的痕量鉛,實驗結果如下表:
| 離子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 處理前濃度/(mg·L-1) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 處理后濃度/(mg·L-1) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
 E2Pb(s)+2H+則脫鉛的最合適pH范圍為( )
E2Pb(s)+2H+則脫鉛的最合適pH范圍為( )(1)> Pb2+與Cl-反應,Pb2+濃度減少
(2)Pb2+、Pb(OH)+、H+ Pb(OH)++OH- Pb(OH)2
Pb(OH)2
(3)Fe3+ (4)B
解析試題分析:(1)因為Pb(NO3)2是一種強酸弱堿鹽,在水溶液中存在如下水解平衡:2H2O+Pb2+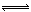 Pb(OH)2+2H+,使c(Pb2+)減小,所以
Pb(OH)2+2H+,使c(Pb2+)減小,所以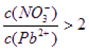 ;滴入氯化銨溶液后,Pb2+與Cl?反應生成難溶的PbCl2,所以Pb2+濃度減少。
;滴入氯化銨溶液后,Pb2+與Cl?反應生成難溶的PbCl2,所以Pb2+濃度減少。
(2)pH=8時,曲線上1、2、3表示的物質共存,所以此時溶液中存在的陽離子(Na+除外)有Pb2+、Pb(OH)+和H+。pH=9時,曲線2、3表示的物質共存,由圖可知Pb(OH)2的濃度分數比Pb(OH)+的大,所以主要反應是生成Pb(OH)2,離子方程式為:Pb(OH)++OH- Pb(OH)2。
Pb(OH)2。
(3)分析比較表中所給數據可知Cu2+、Mn2+、Cl-的濃度都降低不到原濃度的1/2,而Fe3+卻降低為原濃度的1/3,故對Fe3+的去除效果最好。
(4)由所給平衡可知,要使脫鉛效果好,鉛應以Pb2+的形式存在,pH<7,而c(H+)增大時2EH(s)+Pb2+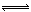 E2Pb(s)+2H+又會向逆反應方向移動,c(H+)不宜過大,所以脫鉛最適宜的pH為6~7。
E2Pb(s)+2H+又會向逆反應方向移動,c(H+)不宜過大,所以脫鉛最適宜的pH為6~7。
考點:本題考查鹽類的水解、離子及其濃度的判斷、離子方程式的書寫、試劑的選擇。


 課堂練加測系列答案
課堂練加測系列答案 輕松課堂單元測試AB卷系列答案
輕松課堂單元測試AB卷系列答案科目:高中化學 來源: 題型:填空題
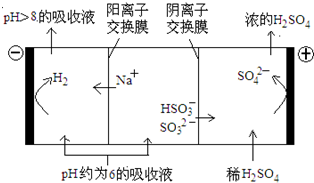
最近霧霾天氣肆虐我國大部分地區。其中SO2是造成空氣的污染的主要原因,利用鈉堿循環法可除去SO2。
(1)鈉堿循環法中,吸收液為Na2SO3溶液,該反應的離子方程式是________。
(2)已知H2SO3的電離常數為K1=1.54×10-2,K2=1.024×10-7;H2CO3的電離常數為K1=4.30×10-7,K2=5.60×10-11,則下列微粒可以大量共存的是______(填序號)。
A.CO32- HSO3- B. HCO3- HSO3- C. SO32- HCO3- D. H2SO3 HCO3-
(3)吸收液吸收SO2的過程中,pH隨n(SO32-):n(HSO3-)變化關系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、 D、 E五種溶液分別是NaOH、NH3·H2O、CH3COOH 、HCl、NH4HSO4中的一種。常溫下進行下列實驗:
①將1 L pH=3的A溶液分別與0.001mol·L-1 xL B溶液、0.001mol·L-1 yL D溶液充分反應至中性,x、y大小關系為: y<x;
②濃度均為0.1mol·L-1A和E溶液,pH:A<E;
③濃度均為0.1mol·L-1C與D溶液等體積混合,溶液呈酸性。
回答下列問題:
(1)D是 溶液,判斷理由是 。
(2)用水稀釋0.1 mol·L-1B時,溶液中隨著水量的增加而減小的是 (填寫序號)
①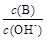 ②
② 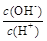 ③ c(H+)和c(OH-)的乘積 ④ OH-的物質的量
③ c(H+)和c(OH-)的乘積 ④ OH-的物質的量
(3)OH-濃度相同的等體積的兩份溶液A和E,分別與鋅粉反應,若最后僅有一份溶液中存在鋅粉,且放出氫氣的質量相同,則下列說法正確的是________(填寫序號)
①反應所需要的時間E>A
②開始反應時的速率A>E
③參加反應的鋅粉物質的量A=E
④反應過程的平均速率 E>A
⑤A溶液里有鋅粉剩余
⑥E溶液里有鋅粉剩余
(4)將等體積、等物質的量濃度B和C混合后溶液,升高溫度(溶質不會分解)溶液pH隨溫度變化如圖中的_________曲線(填寫序號) 。室溫下,向0.01mol·L-1 C溶液中滴加0.01mol·L-1 D溶液至中性,得到的溶液中所有離子的物質的 量濃度由大到小的順序為 。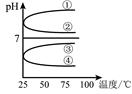
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
一定溫度下,冰醋酸加水稀釋過程中溶液的導電能力變化曲線如圖所示,請回答: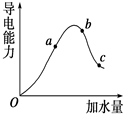
(1) “O”點為什么不導電________.
(2)a,b,c三點的pH由小到大的順序是____________.
(3) a、b、c三點中電離程度最大的是
電離平衡常數Ka、Kb、Kc的大小關系為________.
(4)若使c點溶液中的c(CH3COO-)增大,可以采取下列措施中的 ________(填序號).
A加熱;B加很稀的NaOH溶液;C加NaOH固體;D加水;E加固體CH3COONa;F加入鋅粒
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
結合下表回答下列問題(均為常溫下的數據):
| 酸 | 電離常數(Ka) | 酸 | 電離常數(Ka) |
| CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| HClO | 3×10-8 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
以食鹽為原料進行生產并綜合利用的某些過程如下圖所示: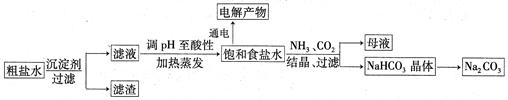
(1)為除去粗鹽中的Ca2+、Mg2+和SO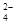 ,得到純凈的NaCl晶體,需加入以下試劑:
,得到純凈的NaCl晶體,需加入以下試劑:
| A.過量的NaOH溶液; | B.過量的Na2CO3溶液; | C.適量的鹽酸; | D.過量的BaCl2溶液。 |
 (OH-)的比值是_________。
(OH-)的比值是_________。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
對于弱酸,在一定溫度下達到電離平衡時,各微粒的濃度存在一種定量的關系。若25℃時有HA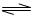 H++A―,則該弱酸的電離平衡常數的表達式為K=__________。下表是幾種常見弱酸的電離平衡常數(25℃)。
H++A―,則該弱酸的電離平衡常數的表達式為K=__________。下表是幾種常見弱酸的電離平衡常數(25℃)。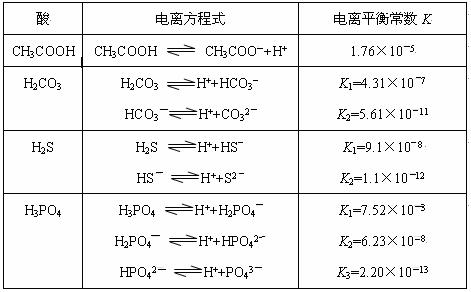
請回答下列各題:
(1)K只與溫度有關,當溫度升高時,K值______(填“增大”、“減小”或“不變”)。
(2)在溫度相同時,各弱酸的K值不同,那么K值的大小與酸性的相對強弱有何關系?_______________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最強的是_____________,最弱的是_____________。
(4)多元弱酸是分步電離的,每一步都有相應的電離平衡常數,對于同一種多元弱酸的K1、K2、K3之間存在著數量上的規律是K1:K2:K3≈1:10―5:10―10,產生此規律的原因是:________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
許多硫的含氧酸鹽在醫藥、化工等方面有著重要的用途。
(1))重晶石(BaS04)常作胃腸道造影劑。
已知:常溫下,Ksp(BaSO4)=1.1×10-10,向BaSO4懸濁液中加入硫酸,當溶液的pH=2時, 溶液中 c(Ba2+)= 。
(2)硫酸亞鐵銨晶體[(NH4)2Fe(SO4)2·6H20]常作分析劑。
①檢驗晶體中含有NH4+的方法為_______。
②等物質的量濃度的四種稀溶液:
a.(NH4)2Fe(SO4)2 b.NH4HSO4 c.(NH4)2SO4 d.(NH4)2SO3
其中C(NH4+)由大到小的順序為 (填選項字母)。
(3)過二硫酸鉀(K2S2O8)常作強氧化劑,Na2S2O3常作還原劑。
①K2S2O8溶液與酸性MnSO4溶液混合,在催化劑作用下,可以觀察到溶液變為紫色, 該反應的離子方程式為
②用鉑作電極,電解H2SO4和K2SO4的混合溶液可以制備K2S2O8,其陽極的電極反應式為_____ __電解過程中陰極附近溶液的pH將______ (填“增大”、“減小”或“不變”)
③產品中K2S2O8的含量可用碘量法測定。操作步驟為:稱取0.3g產品于碘量瓶中,加50 mL水溶解;加入4.000 g KI固體(稍過量),振蕩使其充分反應;加入適量醋酸溶液酸化,以______為指示劑,用0.1000 mol·L-1 Na2S2O3標準液滴定至終點(已知:I2+2S2O32-=2I-+S4O62-)。重復2次,測得平均消耗標準液21.00mL。該產品中K2S2O8的質量分數為(雜質不參加反應) (列式并計算)。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
(1)已知25℃時有關弱酸的電離平衡常數:
| 弱酸化學式 | HSCN | CH3COOH | HCN | H2CO3 |
| 電離平衡常數 | 1.3×10—1 | 1.8×10—5 | 4.9×10—10 | K1=4.3×10—7 K2=5.6×10—11 |



查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com