
【題目】A、B、C、W 均為中學常見的純凈物,它們之間有如下轉化關系(其它產物及反應條件已略去)。
![]()
(1)若單質 A 為黃色固體,B 為無色有刺激性氣味的氣體,C 能與水反應生成一種二元強酸.
①B→C 的化學方程式_____。
②向 NaOH 溶液中通入過量的氣體 B 的離子方程式______。
(2)若 A 是一種黃綠色的氣體,B 的飽和溶液滴入沸水中能生成紅褐色膠體。
①檢驗 B 溶液中陽離子的常用試劑是_____。
②B 與 W 轉化為 C 的離子反應方程式_____。
③一定條件下 W 與水反應的化學方程式______。
【答案】2SO2+O2![]() 2SO3 SO2+ OH-==== HSO3- KSCN 溶液(氫氧化鈉溶液) Fe + 2Fe3+ ==== 3Fe2+ 3Fe+4H2O(g)
2SO3 SO2+ OH-==== HSO3- KSCN 溶液(氫氧化鈉溶液) Fe + 2Fe3+ ==== 3Fe2+ 3Fe+4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
【解析】
(1)若單質A為黃色固體,B為無色有刺激性氣味的氣體,C能與水反應生成一種二元強酸,則A是S,W是O2、B是SO2、C是SO3,SO3和H2O反應生成H2SO4;
(2)若A是一種黃綠色的氣體,B的飽和溶液滴入沸水中能生成紅褐色膠體,則A是Cl2,W是Fe,B是FeCl3、C是FeCl2。
(1)若單質A為黃色固體,B為無色有刺激性氣味的氣體,C能與水反應生成一種二元強酸,則A是S,W是O2、B是SO2、C是SO3,SO3和H2O反應生成H2SO4。
①B→C的反應為二氧化硫氧化為三氧化硫,反應的方程式為:2SO2+O2![]() 2SO3,故答案為:2SO2+O2
2SO3,故答案為:2SO2+O2![]() 2SO3。
2SO3。
②向NaOH溶液中通入過量的SO2氣體,生成亞硫酸氫鈉,反應的離子方程式為:SO2+OH-=HSO3-,故答案為:SO2+ OH-=HSO3-。
(2)若A是一種黃綠色的氣體,B的飽和溶液滴入沸水中能生成紅褐色膠體,則A是Cl2,W是Fe,B是FeCl3、C是FeCl2。
①B為FeCl3,檢驗Fe3+的常用試劑是KSCN溶液(氫氧化鈉溶液),若用KSCN溶液,溶液變為血紅色,若用氫氧化鈉溶液,出現紅褐色的沉淀,故答案為:KSCN溶液(氫氧化鈉溶液)。
②W是Fe、B是FeCl3,Fe與FeCl3反應生成FeCl2,離子方程式為:Fe+2Fe3+=3Fe2+,故答案為:Fe+2Fe3+=3Fe2+。
③鐵與水蒸氣反應生成四氧化三鐵和氫氣,反應方程式為:3Fe+4H2O(g)![]() Fe3O4+4H2,故答案為:3Fe+4H2O(g)
Fe3O4+4H2,故答案為:3Fe+4H2O(g)![]() Fe3O4+4H2。
Fe3O4+4H2。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】莽草酸可用于合成藥物達菲,其結構簡式如圖,下列關于莽草酸的說法 正確的是
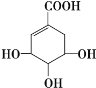
A. 分子式為C7H6O5
B. 分子中含有2種官能團
C. 可發生加成和酯化反應
D. 1mol莽草酸與足量的NaHCO3溶液反應可放出4molCO2氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用水稀釋0.1mol/L的氨水時,溶液中隨著水量增加而減少的是
A. c(H+) B. OH-的物質的量
C. c(OH-)/c(NH3·H2O) D. c(NH3·H2O)/ c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,從A處通入新制備的氯氣,關閉旋塞B時,C處紅色布條無明顯的變化,打開旋塞B 時,C處紅色布條逐漸褪色。由此可判斷D瓶中裝的試劑不可能是

A. 濃硫酸B. 溴化鈉溶液C. Na2SO3溶液D. 硝酸鈉溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】淀粉、脂肪、胰島素和DNA共有的化學元素是( )
A. C、H、O B. C、H、O、N
C. C、H、O、N、P D. C、H、O、N、P、S
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于硅的說法不正確的是
A.晶體硅的導電性介于金屬和絕緣體之間,是良好的半導體
B.加熱到一定溫度時,硅能與氯氣、氧氣等非金屬反應
C.利用二氧化硅與C反應能制得粗硅
D.二氧化硅性質較穩定,常溫下不與任何物質反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值.下列說法正確的是( )
A. 高溫下,0.2 mol Fe與足量水蒸氣反應,生成的H2分子數目為0.3NA
B. 室溫下,1 L pH=13的NaOH溶液中,由水電離的OH﹣離子數目為0.1NA
C. 氫氧燃料電池正極消耗22.4 L(標準狀況)氣體時,電路中通過的電子數目為2NA
D. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反應中,生成28 g N2時,轉移的電子數目為3.75NA
2HNO3+4N2↑+9H2O反應中,生成28 g N2時,轉移的電子數目為3.75NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖設計的串聯電池裝置,R為變阻器,以調節電路電流。
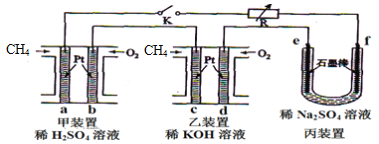
(1)寫出b、c電極的電極反應式:b______________,c_______________;
(2)寫出f電極的電極反應式____________________,向此電極區域滴入酚酞的現象為:_____________;該電極區域水的電離平衡被____________(填“促進”、“抑制”或“無影響”)。
(3)閉合K一段時間后,丙裝置的電解質溶液pH__________(填“變大”、“變小”或“不變”),原因是______________。
(4)電解一段時間后丙裝置析出芒硝(Na2SO4·10H2O),若此時通入CH4的體積為22.4L(標準狀況下),則向丙裝置中加入______g H2O就可以將析出的沉淀溶解并恢復到原有濃度。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知熱化學方程式:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列說法正確的是( )
2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列說法正確的是( )
A. 相同條件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量
B. 將2 mol SO2(g)和1 mol O2(g)置于一密閉容器中充分反應后,放出的熱量為Q kJ
C. 若使用催化劑,該反應的|ΔH|減小
D. 如將一定量SO2(g)和O2(g)置于某密閉容器中充分反應后放熱Q kJ,則此過程中有2 molSO2(g)被氧化
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com