
下列各組分子中,中心原子雜化軌道的類型不相同的是
| A.CO2與SO2 | B.CH4與NH3 | C.SO3與BF3 | D.H2S與CCl4 |
科目:高中化學 來源: 題型:問答題
【物質結構與性質】
X、Y、Z、M、N、Q為元素周期表前四周期的六種元素。其中X原子核外的M層中只有兩對成對電子,Y原子核外的L層電子數是K層的兩倍,Z是地殼內含量(質量分數)最高的元素,M的內層電子數是最外層電子數的9倍,N的原子序數比M小1, Q在元素周期表的各元素中電負性最大。請回答下列問題:
(1)X元素在周期表中的位置是 ,屬 區元素,它的最外層電子的電子排布圖為 。
(2)XZ2分子的立體結構是 ,YZ2分子中Y的雜化軌道類型為 ,相同條件下兩者在水中的溶解度較大的是 (寫分子式),理由是 。
(3)含有元素N的鹽的焰色反應為 色,許多金屬鹽都可以發生焰色反應,其原因是 。
(4)元素M與元素Q形成晶體結構如圖所示,設其晶胞邊長為a pm,則a位置與b位置之間的距離為_______pm(只要求列算式)。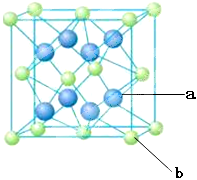
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
X、Y、Z、W是原子序數依次增大的四種短周期元素。X與W可形成四面體形的共價化合物,該化合物常用作滅火劑。Y的次外層電子數等于其最外層和最內層電子數之和的2倍,Y、Z的最外層電子數之和等于W的最外層電子數。
(1)用化學符號表示X的一種核素 。
(2)寫出Y的單質與X的最高價氧化物反應的化學方程式 。
(3)Z的單質在W的單質中燃燒,生成的產物中各原子的最外層均達到8電子穩定結構的分子為 。
(4)用電子式表示Y與W形成化合物的過程為 。
(5)XW4的電子式為 。
(6)W的氫化物R是實驗室一種常用試劑的主要成分,該試劑可用于實驗室多種氣體的制備,寫出實驗室制取氣體時滿足下列條件的離子方程式。
①R作氧化劑: 。
②R作還原劑: 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某研究性學習小組設計了一組實驗驗證元素周期律。
(1)甲同學在a、b、c三只燒杯里分別加入50 mL水,再分別滴加幾滴酚酞溶液,依次加入大小相近的鋰、鈉、鉀塊,觀察現象。
①甲同學設計實驗的目的是________________________________________________;
②反應最劇烈的燒杯是_______(填字母);
③寫出b燒杯里發生反應的離子方程式______ _____ __。
(2)乙同學設計實驗驗證非金屬元素的非金屬性越強,對應的最高價含氧酸的酸性就越強。他設計了下圖裝置以驗證碳、氮、硅元素的非金屬性強弱。
乙同學設計的實驗可直接證明三種酸的酸性強弱,已知A是強酸,常溫下可與銅反應;B是塊狀固體;打開分液漏斗的活塞后,C中可觀察到白色沉淀生成。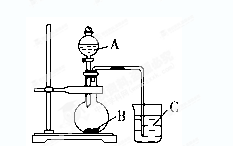
①寫出所選用物質的化學式:A、________; B、________;C、________。
②寫出燒瓶中發生反應的化學方程式:
___________________________________________________________。
③寫出燒杯中發生反應的化學方程式:
___________________________________________________________。
④碳、氮、硅元素的非金屬性強弱順序為_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列說法正確的是( )
| A.含有共價鍵的化合物一定是共價化合物 |
| B.分子中只有共價鍵的化合物一定是共價化合物 |
| C.離子鍵就是陰、陽離子間相互吸引 |
| D.只有非金屬原子間才能形成共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列關于σ鍵和π鍵的理解不正確的是( )
| A.σ鍵能單獨形成,而π鍵一定不能單獨形成 |
| B.σ鍵可以繞鍵軸旋轉,π鍵一定不能繞鍵軸旋轉 |
| C.HCl 分子中的σ鍵是由一個原子的s軌道和另一個原子的p軌道以“頭碰頭”方式重疊構建而成的 |
| D.氣體單質中一定存在σ鍵,可能存在π鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
實驗測得BeCl2為共價化合物,兩個Be—Cl鍵間的夾角為180°,以下判斷正確的是( )
| A.由極性鍵構成的極性分子 | B.由極性鍵構成的非極性分子 |
| C.由非極性鍵構成的極性分子 | D.BeCl2中Be采取sp2雜化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com