
【題目】X、Y、Z、W有如下所示的轉化關系,且△H=△H1+△H2 , 則X、Y可能是( )
①C,CO ②S,SO2 ③AlCl3、Al(OH)3 ④Na2CO3、NaHCO3 ⑤Fe、FeCl2 . ![]()
A.①②③④⑤
B.②④⑤
C.①③④
D.①②③
【答案】C
【解析】解:①由C+O2 ![]() CO2 , 可看成C+
CO2 , 可看成C+ ![]() O2
O2 ![]() CO、CO+
CO、CO+ ![]() O2
O2 ![]() CO2來完成,X、Y、Z的物質的量相等,符合△H=△H1+△H2,故①正確;
CO2來完成,X、Y、Z的物質的量相等,符合△H=△H1+△H2,故①正確;
②因S與氧氣反應生成二氧化硫,不會直接生成三氧化硫,則不符合轉化,故②錯誤;
③由AlCl3+4NaOH═3NaCl+NaAlO2+2H2O,可看成AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O來完成,X、Y、Z的物質的量相等,符合△H=△H1+△H2,故③正確;
④由Na2CO3+2HCl═CO2+2NaCl+H2O,可看成Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═CO2+NaCl+H2O來完成,X、Y、Z的物質的量相等,符合△H=△H1+△H2,故④正確;
⑤Fe和Cl2反應生成FeCl3 , 故⑤錯誤;
故選C.


 智能訓練練測考系列答案
智能訓練練測考系列答案科目:高中化學 來源: 題型:
【題目】微生物電池是指在微生物的作用下將化學能轉化為電能的裝置,其工作原理如圖所示.下列有關微生物電池的說法正確的是( ) 
A.b極為正極,發生氧化反應
B.外電路中電子的移動方向為:b→a
C.質子通過交換膜從b極區移向a極區
D.電池總反應為C6H12O6+6O2=6CO2+6H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于氧化劑與還原劑的判斷正確的是( )
A.反應CH4+2O2![]() CO2+2H2O中,O2是氧化劑,CH4是還原劑
CO2+2H2O中,O2是氧化劑,CH4是還原劑
B.反應Cl2+2NaOH=NaClO+NaCl+H2O中,Cl2是氧化劑,NaOH是還原劑
C.反應MnO2+4HCl(濃) ![]() MnCl2+Cl2↑+2H2O中,HCl是氧化劑,MnO2是還原劑
MnCl2+Cl2↑+2H2O中,HCl是氧化劑,MnO2是還原劑
D.反應2Na+2H2O=2NaOH+H2↑中,H2O既是氧化劑又是還原劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】地殼中含量第一和第三的兩元素形成的化合物不具有的性質是( )
A.熔點很高B.與鐵在高溫下發生放熱反應
C.能溶于氫氧化鈉溶液D.熔融后可以導電
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學學習小組的同學欲探究測定草酸晶體(H2C2O4xH2O)中x的值.通過查閱資料該小組同學得知:草酸易溶于水,其水溶液可以與酸性KMnO4溶液發生反應2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.該組同學利用該反應原理設計了滴定的方法測定x值.
①稱取1.260g純草酸晶體,將其制成100.00mL水溶液為待測液.
②取25.00mL待測液放入錐形瓶中,再加入適量的稀H2SO4
③用濃度為0.1000mol/L的KMnO4標準溶液進行滴定,實驗記錄有關數據如下:
滴定次數 | 待測草酸溶液體積(mL) | 0.1000mol/LKMnO4標準溶液體積(mL) | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 0.00 | 10.02 |
第二次 | 25.00 | 0.22 | 11.32 |
第三次 | 25.00 | 1.56 | 11.54 |
請回答: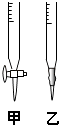
(1)滴定時,將KMnO4標準液裝在右圖中的(填“甲”或“乙”)滴定管中.
(2)本實驗滴定達到終點的標志可以是 .
(3)通過上述數據,計算出x= .
(4)①若滴定終點時俯視滴定管刻度,則由此測得的x值會(填“偏大”、“偏小”或“不變”,下同).
②若滴定時所用的KMnO4溶液因久置而導致濃度變小,則由此測得的x值會 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知砒霜As2O3與Zn可以發生如下反應:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O
(1)請用“雙線橋法”標出電子轉移的方向和數目:。
(2)As2O3在上述反應中________。
A.被氧化
B.被還原
C.既被氧化又被還原
D.既未被氧化又未被還原
(3)該反應的氧化產物是 , 氧化劑是。
(4)若生成0.1 mol AsH3 , 則轉移的電子數為。(用NA表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列每組分別給出了兩個量,不可以求出相應物質的量的是
A | B | C | D |
物質微粒數 | 溶液的質量分數 | 標準狀況下氣體的摩爾體積 | 物質的質量 |
阿伏加德羅常數 | 溶液體積 | 標準狀況下氣體的體積 | 物質的摩爾質量 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇是一種重要的可再生能源.
(1)2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=a kJ/mol
CO(g)+2H2(g)=CH3OH(g)△H=b kJ/mol
寫出由CH4和O2制取CH3OH(g)的熱化學方程式: .
(2)甲圖是反應時CO和CH3OH(g)的物質的量濃度隨時間(t)的變化曲線.從反應開始至達到平衡時,用H2表示的反應速率v(H2)= . 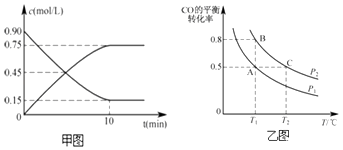
(3)在一容積可變的密閉容器中充入10mol CO和20mol H2 , 發生上述反應并達到平衡,CO的平衡轉化率隨溫度(T)、壓強(P)的變化曲線如乙圖所示.
能判斷該反應達到化學平衡狀態的是(填選項字母).
A.H2的消耗速率等于CH3OH的生成速率的2倍
B.H2的體積分數不再改變
C.H2的轉化率和CO的轉化率相等
D.混合氣體的平均相對分子質量不再改變
(4)以甲醇為燃料,O2為氧化劑,KOH溶液為電解質溶液,可制成燃料電池(電極材料為惰性電極).若KOH溶液足量,寫出燃料電池負極的電極反應式:
(5)如圖所示,以甲醇燃料電池作為電源實現下列電解過程.乙池中發生反應的離子方程式為 . 當甲池中增重16g時,丙池中理論上產生沉淀質量的最大值為g. 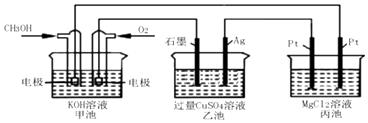
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某非金屬X的最低負價為﹣m.它的最高價氧化物對應的水化物中有b個氧原子,則這種酸的分子式為( )
A.H2b﹣8+mXOb
B.H2b﹣m+8XOb
C.H2b﹣8﹣mXOb
D.H2b+8+mXOb
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com