
【題目】實驗室測定鉻鐵礦中鉻(Cr)含量的步驟如下:
步驟1:準確稱取0.2000g鉻鐵礦試樣放入錐形瓶中,加入適量磷酸和硫酸的混合酸,加熱使試樣完全溶解,冷卻。
步驟2:向上述溶液中滴加5滴1%MnSO4溶液,再加入一定量的(NH4)2S2O8溶液,搖勻至溶液呈紫紅色[先后發生Cr3+![]() Cr2O72-、Mn2+
Cr2O72-、Mn2+![]() MnO4-]。
MnO4-]。
步驟3:上述溶液加熱煮沸至紫紅色褪去[除去過量的(NH4)2S2O8和生成的MnO4-],冷卻。
步驟4:用0.2000mol·L-1(NH4)2Fe(SO4)2標準溶液滴定上述溶液至終點(發生Cr2O72-![]() Cr3+),消耗19.50mL標準溶液。
Cr3+),消耗19.50mL標準溶液。
(1)(NH4)2S2O8中陰離子的結構如圖所示。從結構分析,(NH4)2S2O8置于棕色試劑瓶并于陰涼處保存的原因是__。
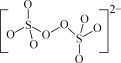
(2)“步驟2”中加入5滴1%MnSO4溶液的目的是__。
(3)“步驟3”中,如果繼續加熱煮沸時間不充足,會使鉻含量的測定結果___(填“偏大”“不變”或“偏小”)。
(4)計算鉻鐵礦中鉻的質量分數___(寫出計算過程)。
【答案】過氧鍵見光、受熱易斷裂而造成物質分解 判斷溶液中的Cr3+是否完全被氧化成Cr2O72- 偏大 33.8%
【解析】
(1)棕色試劑瓶是存放見光易分解的物質;
(2)加入5滴MnSO4溶液的目的是作為Cr3+與(NH4)2S2O8反應的指示劑;
(3)“氧化”過程中,如果繼續加熱煮沸時間不充足,溶液中過量的(NH4)2S2O8和生成的HMnO4不能完全分解除去,會消耗更多(NH4)2Fe(SO4)2標準溶液;
(4)6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,得到:6Fe2+~Cr2O72-,結合操作過程中的定量關系計算。
(1)從結構分析,(NH4)2S2O8置于棕色試劑瓶并于陰涼處保存的原因是過氧鍵見光、受熱易斷裂而造成物質分解。
故答案為:過氧鍵見光、受熱易斷裂而造成物質分解;
(2)“步驟2”中加入5滴1%MnSO4溶液的目的是作為Cr3+與(NH4)2S2O8反應的指示劑,判斷溶液中的Cr3+是否完全被氧化成Cr2O72-。
故答案為:判斷溶液中的Cr3+是否完全被氧化成Cr2O72-;
(3)②“氧化”過程中,如果繼續加熱煮沸時間不充足,溶液中過量的(NH4)2S2O8和生成的HMnO4不能完全分解除去,會消耗更多(NH4)2Fe(SO4)2標準溶液,導致計算得到結果偏大;
故答案為:偏大;
(4)根據氧化還原反應規律:亞鐵離子被氧化,離子方程式為:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,據此得到:6Fe2+~Cr2O72-,n(Cr2O72-)=![]() ×0.20000mol·L-1×19.50mL×10-3 mL·L-1=6.5×10-4 mol,鉻的質量分數=
×0.20000mol·L-1×19.50mL×10-3 mL·L-1=6.5×10-4 mol,鉻的質量分數=![]() ×100%=33.8%;
×100%=33.8%;
故答案為:33.8%。


科目:高中化學 來源: 題型:
【題目】某實驗小組對H2O2分解反應進行實驗探究:將質量相等狀態不同的MnO2分別加入盛有等體積等濃度的H2O2溶液的大試管中,并用帶火星的木條在試管口測試。有關記錄如下:
MnO2 | 觸摸試管 | 現象 | 反應時間/min |
粉末 | 發燙 | 反應劇烈,帶火星的木條迅速復燃 | t1 |
塊狀 | 微熱 | 反應較慢,火星紅亮但木條未復燃 | t2 |
(1)試管中化學反應方程式:____________。
(2)實驗結果證明了催化劑的催化效果與____________有關。
(3)表中t1____________t2(填寫“>”、“<”或“=”)
(4)控制該反應速率,除了改變催化劑因素,可行的方法還有____________。
(5)某同學用一定濃度的H2O2溶液10mL,加入適量MnO2在某溫度下反應,測量放出氣體的體積(標準狀況)與反應時間的關系如圖所示,則A、B、C三點所表示的即時反應速率最慢的是____________點。
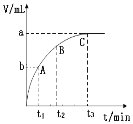
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】298K時,向20mL濃度均為0.1 mol·L-1的MOH和NH3·H2O混合液中滴加0.1mol·L-1的CH3COOH溶液,測得混合液的電阻率(表示電阻特性的物理量)與加入CH3COOH溶液的體積(V)的關系如圖所示。已知CH3COOH的Ka=1.8×10-5,NH3·H2O的Kb =1.8×10-5。下列說法正確的是
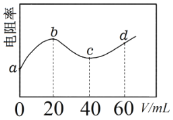
A.b→c過程發生的反應:MOH+CH3COOH=CH3COOM+H2O
B.c點溶液中:c(CH3COOH)+c(CH3COO–)=2c(NH4+)
C.d 點溶液中:c(CH3COO–)c(CH3COOH)>c(M+)>c(H+)>c(OH–)
D.a→c過程中水的電離程度一直在增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Y是合成藥物查爾酮類抑制劑的中間體,可由X在一定條件下反應制得。下列敘述正確的是( )
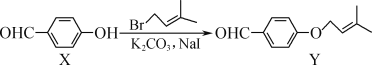
A.Y的分子式為C12H14O2
B.可用FeCl3溶液鑒別X和Y
C.Y能使酸性高錳酸鉀溶液褪色可證明其分子中含有碳碳雙鍵
D.1molX與4molH2完全加成所得產物分子中含2個手性碳原子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H5IO6(正高碘酸)是用于光度法測定苯肼的試劑。工業上用NaIO3制備H5IO6的流程如圖:
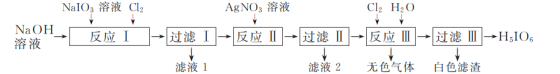
(1)“反應Ⅰ”可在如圖所示的裝置中進行。該反應生成不溶于水的Na2H3IO6的離子方程式為____。若要提高Cl2的利用率,可對裝置進行改進的措施為___。
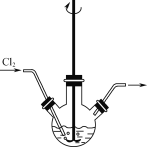
(2)反應Ⅱ生成不溶于水的黑色Ag5IO6,“濾液2”呈__(填“酸”“堿”或“中”)性。
(3)“無色氣體”為__(填化學式)。
(4)工業上為降低成本,減少對環境的污染,整個流程需要控制加入Cl2和AgNO3的物質的量之比為n(Cl2)∶n(AgNO3)=__。
(5)H5IO6具有強氧化性,可將FeSO4氧化為H2FeO4,自身被還原為HIO3,該反應的化學方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2S是石油化工行業廣泛存在的污染性氣體,但同時也是重要的氫源和硫源,工業上可以采取多種方式處理。
Ⅰ.干法脫硫
(1)已知:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l);ΔH1=akJ·mol-1
S(s)+O2(g)=SO2(g);ΔH2=bkJ·mol-1
則空氣氧化脫除H2S反應2H2S(g)+O2(g)=2S(s)+2H2O(l)的ΔH=___kJ·mol-1。
(2)常用脫硫劑的脫硫效果及反應條件如表,則最佳脫硫劑為___。
脫硫劑 | 出口硫/(mg·m-3) | 脫硫溫度/℃ | 操作壓力(MPa) | 再生條件 |
一氧化碳 | <1.33 | 300~400 | 0~3.0 | 蒸汽再生 |
活性碳 | <1.33 | 常溫 | 0~3.0 | 蒸汽再生 |
氧化鋅 | <1.33 | 350~400 | 0~5.0 | 不再生 |
鋅錳礦 | <3.99 | 400 | 0~2.0 | 不再生 |
Ⅱ.熱分解法脫硫
在密閉容器中,充入一定量的H2S氣體,發生如下熱分解反應:H2S(g)![]() H2(g)+
H2(g)+![]() S2(g)
S2(g)
控制不同的溫度和壓強進行實驗,結果如圖1所示。
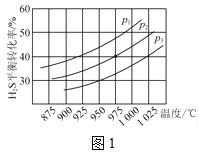
(1)p1、p2、p3由大到小的順序為___。
()保持壓強不變,能提高H2S的平衡轉化率的措施有__(寫一條)。
Ⅲ.間接電解法脫硫
間接電解法脫硫原理如圖2所示(吸收反應器中盛放FeCl3溶液,電解反應器的陰極、陽極均為惰性電極)。
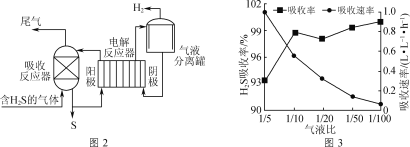
(1)吸收反應器中發生反應的離子方程式為___。
(2)反應器陰極生成H2的電極反應式為__。
(3)氣液比為氣體與液體的流速比,吸收反應器內液體流速固定。測定吸收器中相同時間內不同氣液比下H2S的吸收率和吸收速率,結果如圖3所示。隨著氣液比減小,H2S的吸收率呈上升趨勢的原因為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硝酸是一種重要的化工原料,用來制取一系列硝酸鹽類氮肥,如硝酸銨、硝酸鉀等;也用來制取含硝基的炸藥等。試回答下列問題:
(1)某同學對鐵與稀硝酸的反應進行探究,若HNO3只被還原成NO,則:
①寫出鐵與過量稀硝酸反應的離子方程式:__。
②寫出過量鐵與稀硝酸反應的離子方程式:__。
③若28g鐵與含1.6mol硝酸的稀硝酸恰好完全反應,則生成的Fe3+和Fe2+的物質的量之比為__。上述反應結束后,向反應后的溶液中加足量氫氧化鈉溶液,濾出沉淀洗滌后,在空氣中灼燒至質量不變,最終得到的固體質量為__g。
(2)飲用水中NO3-對人類健康會產生危害,為了降低飲用水中NO3-的濃度,某飲用水研究人員提出,可在堿性條件下用鋁粉將NO3-還原為N2。
①配平方程式:__Al+__NO3-+__OH-+__=__[Al(OH)4]-+__N2↑。
②上述反應中,還原劑與還原產物的物質的量之比是__,反應中轉移電子0.3mol,生成__mL(標準狀況下)N2。
【答案】Fe+NO3-+4H+=Fe3++NO↑+2H2O 3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O 2∶3 40 10 6 4 18H2O 10 3 10∶3 672
【解析】
(1)①鐵與過量稀硝酸反應生成硝酸鐵、NO和水,離子方程式為Fe+NO3-+4H+=Fe3++NO↑+2H2O;
②過量鐵與稀硝酸反應生成硝酸亞鐵、NO和水,離子方程式為3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O;
③28g鐵的物質的量為0.5mol,與含1.6mol硝酸的稀硝酸恰好完全反應,設生成的Fe3+和Fe2+的物質的量分別是xmol、ymol,即生成xmol硝酸鐵和ymol硝酸亞鐵,根據N原子守恒知,生成NO的物質的量為(1.6-3x-2y)mol,根據得失電子守恒有3x+2y=3(1.6-3x-2y),又有x+y=0.5,解得x=0.2,y=0.3,則生成的Fe3+和Fe2+的物質的量之比為2∶3;上述反應結束后,向反應后的溶液中加足量氫氧化鈉溶液,濾出沉淀洗滌后,在空氣中灼燒至質量不變,由于生成的氫氧化亞鐵在空氣中易被氧化為氫氧化鐵,氫氧化鐵受熱分解最終得到的固體是氧化鐵,故其物質的量為0.5mol×![]() =0.25mol,質量為40g;
=0.25mol,質量為40g;
(2)①根據得失電子守恒、原子守恒及電荷守恒,可知離子方程式為10Al+6NO3-+4OH-+18H2O=10[Al(OH)4]-+3N2↑;
②上述反應中,還原劑是Al,還原產物是N2,其物質的量之比為10∶3;由方程式可知,生成3molN2時轉移電子30mol,所以反應中轉移電子0.3mol,生成N2的體積(標準狀況下)為![]() ×22.4L·mol-1=0.672L=672mL。
×22.4L·mol-1=0.672L=672mL。
【點睛】
金屬與硝酸反應的計算一般常采用以下方法:①原子守恒法:HNO3與金屬反應時,一部分HNO3起酸的作用,以NO的形式存在于溶液中;一部分作為氧化劑轉化為還原產物,這兩部分中氮原子的總物質的量等于反應消耗的HNO3中氮原子的物質的量;②得失電子守恒法:HNO3與金屬的反應屬于氧化還原反應,HNO3中氮原子得到電子的物質的量等于金屬失電子的物質的量;③電荷守恒法:HNO3過量時反應后溶液中(不考慮OH-)有:c(NO3-)=c(H+)+nc(Mn+)(Mn+代表金屬離子);④離子方程式計算法:金屬與H2SO4、HNO3的混合酸反應時,由于溶液中NO3-在H2SO4提供H+的條件下能繼續與金屬反應,因此此類題目應用離子方程式來計算,先作過量判斷,然后根據完全反應的金屬或H+或NO3-進行相關計算,且溶液中要符合電荷守恒。
【題型】綜合題
【結束】
21
【題目】如圖是氮元素的幾種價態與物質類別的對應關系。請回答下列問題:

(1)寫出N2的一種用途:___。
(2)HNO3與圖中的物質C
(3)實驗室制取物質B的化學方程式為____。
(4)NO2與水反應生成物質A的化學方程式為____。
(5)濃硝酸與木炭在加熱條件下反應的化學方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作對應的現象不符合事實的是
|
|
|
|
A.用鉑絲蘸取NaCl溶液置于酒精燈火焰上灼燒,火焰呈黃色 | B.將少量銀氨溶液加入盛有淀粉和硫酸的試管中,加熱,產生光亮的銀鏡 | C.飽和食鹽水通電一段時間后,濕潤的KI-淀粉試紙遇b處氣體變藍色 | D.將膽礬晶體懸掛于盛有濃H2SO4的密閉試管中,藍色晶體逐漸變為白色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過氧化氫俗名雙氧水,醫療上利用它有殺菌消毒作用來清洗傷口.關于雙氧水,回答下列問題:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反應中,不屬于氧化還原反應的是__________(填代號,下同),H 2 O 2 僅體現還原性的反應是__________。
(2)上述反應說明H2O2 、Ag2O、K2CrO 4 氧化性由強到弱的順序是_________________
(3)某強酸反應體系中發生的一個氧化還原的離子反應,反應物和生成物共六種微粒:O2、MnO4— 、H2O、Mn2+ 、H2O2 、H+ 。已知該反應中H2O2 只發生了如下過程:H2O2 →O2。
①反應體系選擇的酸是:____________ A.鹽酸 B.硫酸 C醋酸
②該反應的離子方程式為________________________________________。
③如果上述反應中有2.24L(標準狀況)氣體生成,轉移的電子為 _______mol.
(4)H2O2 有時可作為礦業廢液消毒劑,有“綠色氧化劑”的美稱;如消除采礦業膠液中的氰化物(如KCN),經以下反應實驗:KCN+H2O2 +H2O=A+NH3↑,試指出生成物A的化學式為_____________.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com