
“氫能”是人類未來最理想的新能源之一。
(1)實驗測得,1 g氫氣燃燒生成液態水時放出142.9 kJ熱量,則表示氫氣燃燒熱的熱化學方程式為__________________________。
(2)利用核能把水分解制氫氣,是目前正研究的課題。如圖是其中的一種流程,流程中用了過量的碘(提示:反應②的產物是O2、SO2和H2O)。
完成下列反應的化學方程式:反應①________________;反應②________________。此法制取氫氣的最大優點是____________________。
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:填空題
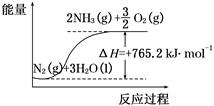
一種“人工固氮”的新方法是在常溫、常壓、光照條件下,N2在催化劑表面與水發生反應生成NH3:N2+3H2O 2NH3+O2
2NH3+O2
進一步研究NH3生成量與溫度的關系,部分實驗數據見下表(反應時間3 h):
| T/℃ | 30 | 40 | 50 |
| 生成NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
 2NH3(g) ΔH=-92.4 kJ·mol-1。在某壓強恒定的密閉容器中加入2 mol N2和4 mol H2,達到平衡時,N2的轉化率為50%,體積變為10 L。求:
2NH3(g) ΔH=-92.4 kJ·mol-1。在某壓強恒定的密閉容器中加入2 mol N2和4 mol H2,達到平衡時,N2的轉化率為50%,體積變為10 L。求:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(16分)碳、氮、硫、氯是四種重要的非金屬元素。
(1)CH4(g)在O2(g)中燃燒生成CO(g)和H2O(g)的△H難以直接測量,原因是 。
已知:a.2CO(g)+O2(g)=2CO2(g) △H =-566.0 kJ·mol-1
b.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H =-890.0 kJ·mol-1
則CH4(g)在O2(g)中燃燒生成CO(g)和H2O(g)的熱化學方程式為 。
(2)工業上合成氨氣的反應為:N2(g)+3H2(g)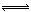 2NH3(g) △H<0。現將10 mol N2和26 mol H2置于容積可變的密閉容器中,N2的平衡轉化率(
2NH3(g) △H<0。現將10 mol N2和26 mol H2置于容積可變的密閉容器中,N2的平衡轉化率(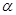 )與體系總壓強(P)、溫度(T)的關系如圖所示。回答下列問題:
)與體系總壓強(P)、溫度(T)的關系如圖所示。回答下列問題:
①反應達到平衡狀態B時,容器的容積10 L,則T1時,合成氨反應的平衡常數K= L2·mol-1。
②平衡狀態由A變到C時,對應的平衡常數K(A) K(C)(填“>”、“<”或“=”)。
(3)在25℃時,HSCN、HClO、H2CO3的電離常數如下表:
| HClO | HSCN | H2CO3 |
| K=3.210-8 | K=0.13 | Kl=4.210-7 K2=5.610-11 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
用Cl2生產某些含氯有機物時會產生副產物HCl。利用反應A,可實現氯的循環利用。
反應A:4HCl+O2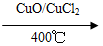 2Cl2+2H2O
2Cl2+2H2O
(1)已知:ⅰ.反應A中,4 molHCl被氧化,放出115.6 kJ的熱量。
ⅱ.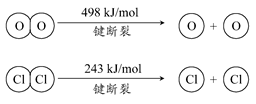
①H2O的電子式是________。
②反應A的熱化學方程式是______________________________________。
③斷開1 mol H—O鍵與斷開1 mol H—Cl鍵所需能量相差約為________kJ,H2O中H—O鍵比HCl中H—Cl鍵(填“強”或“弱”)________。
(2)對于反應A,下圖是在4種投料比[n(HCl):n(O2),分別為1:1、2:1、4:1、6:1]下,反應溫度對HCl平衡轉化率影響的曲線。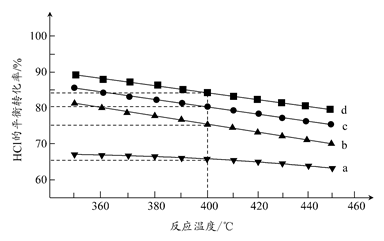
①曲線b對應的投料比是________。
②當曲線b、c、d對應的投料比達到相同的HCl平衡轉化率時,對應的反應溫度與投料比的關系是______________________________。
③投料比為2:1、溫度為400℃時,平衡混合氣中Cl2的物質的量分數是________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2012年11月16日,5名男孩被發現死于貴州省畢節市七星關區街頭垃圾箱內,經當地公安部門初步調查,5名男孩是因在垃圾箱內生火取暖導致CO中毒而死亡。
(1)CO中毒是由于CO與血液中血紅蛋白的血紅素部分反應生成碳氧血紅蛋白,反應的化學方程式可表示為CO+HbO2 O2+HbCO,實驗表明,c(HbCO)即使只有c(HbO2)的
O2+HbCO,實驗表明,c(HbCO)即使只有c(HbO2)的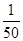 ,也可造成人的智力損傷。已知t ℃時上述反應的平衡常數K=200,吸入肺部O2的濃度約為1.0×10-2 mol·L-1,若使c(HbCO)小于c(HbO2)的
,也可造成人的智力損傷。已知t ℃時上述反應的平衡常數K=200,吸入肺部O2的濃度約為1.0×10-2 mol·L-1,若使c(HbCO)小于c(HbO2)的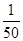 ,則吸入肺部CO的濃度不能超過______mol·L-1。
,則吸入肺部CO的濃度不能超過______mol·L-1。
(2)有如下三個與CO相關的反應:
Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=Q1,平衡常數K1
FeO(s)+CO(g) ΔH=Q1,平衡常數K1
Fe(s)+H2O(g) FeO(s)+H2(g) ΔH=Q2,平衡常數為K2
FeO(s)+H2(g) ΔH=Q2,平衡常數為K2
H2(g)+CO2(g) CO(g)+H2O(g) ΔH=Q3,平衡常數為K3
CO(g)+H2O(g) ΔH=Q3,平衡常數為K3
在不同的溫度下K1、K2、K3的數值如下:
| T/℃ | K1 | K2 | K3 |
| 700 | 1.47 | 2.38 | 0.62 |
| 900 | 2.15 | 1.67 | |
 CO(g)+H2O(g)為________(填“放”或“吸”)熱反應,Q3________0(填“>”、“<”或“=”)。③改變條件使可逆反應H2(g)+CO2(g)
CO(g)+H2O(g)為________(填“放”或“吸”)熱反應,Q3________0(填“>”、“<”或“=”)。③改變條件使可逆反應H2(g)+CO2(g) CO(g)+H2O(g)已經建立的平衡逆向移動,可采取的措施有________。
CO(g)+H2O(g)已經建立的平衡逆向移動,可采取的措施有________。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫的化合物在生產和科研中發揮著重要作用。
(1)SO2Cl2常用于制造醫藥品、染料、表面活性劑等。已知:SO2Cl2(g) SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某溫度時向體積為1 L的恒容密閉容器中充入0. 20mol SO2Cl2,達到平衡時,容器中含0.18mol SO2,則此過程反應吸收的熱量為_____kJ,該溫度時反應的平衡常數為_____。將上述所得混合氣體溶于足量BaCl2溶液中,最終生成沉淀的質量為_______。
SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某溫度時向體積為1 L的恒容密閉容器中充入0. 20mol SO2Cl2,達到平衡時,容器中含0.18mol SO2,則此過程反應吸收的熱量為_____kJ,該溫度時反應的平衡常數為_____。將上述所得混合氣體溶于足量BaCl2溶液中,最終生成沉淀的質量為_______。
(2)工業上制備硫酸的過程中存在反應:2SO2(g)+O2(g) 2SO3(g) △H=-198kJ·mol-1400℃,1.01×105Pa,向容積為2L的恒容密閉容器中充入一定量 SO2和O2,n(SO3)和n(O2)隨時間的變化曲線如圖所示。
2SO3(g) △H=-198kJ·mol-1400℃,1.01×105Pa,向容積為2L的恒容密閉容器中充入一定量 SO2和O2,n(SO3)和n(O2)隨時間的變化曲線如圖所示。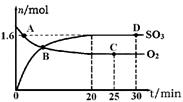
①0~20min反應的平均速率υ(O2)=___________。
②下列敘述正確的是 。
a.A點υ正(SO2)>υ逆(SO2)
b.B點處于平衡狀態
c.C點和D點n(SO2)相同
d.其它條件不變,500℃時反應達平衡,n(SO3)比圖中D點的值大
(3)工業上用Na2SO3溶液吸收煙氣中的SO2。將煙氣通入1.0 mol·L-1的Na2SO3溶液,當溶液pH約為6時,Na2SO3溶液吸收SO2的能力顯著下降,應更換吸收劑。此時溶液中c (SO32-)的濃度是0.2 mol·L-1,則溶液中c(HSO3-)是_________mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
煤制備CH4是一種有發展前景的新技術。
I. 煤炭氣化并制備CH4包括以下反應:
C(s)+H2O(g)=CO(g)+H2 (g) ΔH 1 = +131 kJ/mol
CO(g) + H2O(g)=CO2 (g)+ H2(g) ΔH 2 = ?41 kJ/mol
CO(g) + 3H2 (g)=CH4 (g)+ H2O(g) ΔH 3 = ?206 kJ/mol
(1)寫出煤和氣態水制備CH4(產物還有CO2)的熱化學方程式 。
(2)煤轉化為水煤氣(CO和H2)作為燃料和煤直接作為燃料相比,主要的優點有 。
(3)寫出甲烷—空氣燃料電池(電解質溶液為KOH溶液)中負極的電極反應式 。
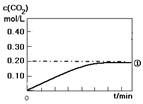
II. 對以上反應CO(g) + H2O(g)  CO2 (g)+ H2(g) ΔH 2 = ?41 kJ/mol,起始時在密閉容器中充入1.00 molCO和1.00 molH2O,分別進行以下實驗,探究影響平衡的因素(其它條件相同且不考慮任何副反應的影響)。實驗條件如下表:
CO2 (g)+ H2(g) ΔH 2 = ?41 kJ/mol,起始時在密閉容器中充入1.00 molCO和1.00 molH2O,分別進行以下實驗,探究影響平衡的因素(其它條件相同且不考慮任何副反應的影響)。實驗條件如下表:
| 實驗編號 | 容器體積/L | 溫度/°C |
| ① | 2.0 | 1200 |
| ② | 2.0 | 1300 |
| ③ | 1.0 | 1200 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
請參考題中圖表,已知E1=134 kJ·mol-1、E2=368 kJ·mol-1,根據要求回答問題: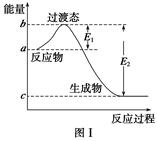
(1)圖Ⅰ是1 mol NO2(g)和1 mol CO(g)反應生成CO2和NO過程中的能量變化示意圖,若在反應體系中加入催化劑,反應速率增大,E1的變化是________(填“增大”、“減小”或“不變”,下同),ΔH的變化是________。請寫出NO2和CO反應的熱化學方程式:________________________________。
(2)甲醇質子交換膜燃料電池中將甲醇蒸汽轉化為氫氣的兩種反應的熱化學方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1
②CH3OH(g)+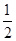 O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1,則甲醇蒸汽燃燒為液態水的熱化學方程式為______________________。
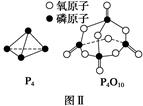
(3)如表所示是部分化學鍵的鍵能參數:
| 化學鍵 | P—P | P—O | O=O | P=O |
| 鍵能/kJ·mol-1 | a | b | c | x |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
碳及其化合物有廣泛的用途。
(1)將水蒸氣通過紅熱的碳即可產生水煤氣。反應為
C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,
以上反應達到平衡后,在體積不變的條件下,以下措施有利于提高H2O的平衡轉化率的是________。(填序號)
| A.升高溫度 | B.增加碳的用量 | C.加入催化劑 | D.用CO吸收劑除去CO |
 2CO(g) ΔH=+172.5 kJ·mol-1,則CO(g)+H2O(g)
2CO(g) ΔH=+172.5 kJ·mol-1,則CO(g)+H2O(g) CO2(g)+H2(g)的焓變ΔH=________。
CO2(g)+H2(g)的焓變ΔH=________。 CH3OH(g)。甲醇是一種燃料,可利用甲醇設計一個燃料電池,用稀硫酸作電解質溶液,多孔石墨作電極,該電池負極反應式為__________________________________。
CH3OH(g)。甲醇是一種燃料,可利用甲醇設計一個燃料電池,用稀硫酸作電解質溶液,多孔石墨作電極,該電池負極反應式為__________________________________。 CO2(g)+H2(g)。得到如下數據:
CO2(g)+H2(g)。得到如下數據:| 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| H2O | CO | H2 | CO | | |
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
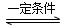 2NH3(g) ΔH=-92.4 kJ·mol-1。實驗室模擬化工生產,分別在不同實驗條件下反應,N2濃度隨時間變化如圖甲所示。
2NH3(g) ΔH=-92.4 kJ·mol-1。實驗室模擬化工生產,分別在不同實驗條件下反應,N2濃度隨時間變化如圖甲所示。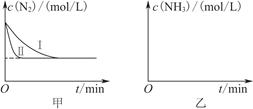
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com