
【題目】X、Y、Z、Q、R是五種短周期元素,原了序數依次增大。X、Y兩元素最高正價與最低負價之和均為0;Q與X同主族;Z、R分別是地殼中含量最高的非金屬元素和金屬元素。請回答下列問題:
(1)五種元素原子半徑由大到小的順序是(寫元素符號)______________。
(2)X與Z能形成多種化合物,其中相對分了質量是34的分子的結構式為___________。
(3)由以上某些元素組成的化合物A、B、C、D有如下轉化關系:![]() (在水溶液中進行)。其中,C是溶于水顯酸性的氣體;D是淡黃色固體。寫出D的電子式_______。
(在水溶液中進行)。其中,C是溶于水顯酸性的氣體;D是淡黃色固體。寫出D的電子式_______。
①如果A、B均由三種元素組成,B為兩性不溶物,由A轉化為B的離子方程式為______。
②如果A由三種元素組成,B由四種元素組成,A、B溶液均顯堿性,由A轉化為B的離子方程式為_________________。
【答案】 Na>Cl>C>O>H H-O-O-H ![]() CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-(或CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-) CO2+H2O+CO32-=2HCO3-
CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-(或CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-) CO2+H2O+CO32-=2HCO3-
【解析】X、Y、Z、Q、R是五種短周期元素,原子序數依次增大,Z、R分別是地殼中含量最高的非金屬元素和金屬元素,則Z為O元素、R為Al;X、Y兩元素最高正價與最低負價代數和均為0,原子序數均小于O元素,為ⅠA族元素、ⅣA族元素,故X為H元素、Y為C元素;Q與X同主族,結合原子序數可知,Q為Na元素,據此分析解答。
根據以上分析可知X、Y、Z、Q、R分別是H、C、O、Na、Al。則
(1)同周期自左而右,原子半徑逐漸減小,電子層越多,原子半徑越大,故原子半徑由大到小的順序是:Na>Al>C>O>H;
(2)O和H能形成多種化合物,其中相對分子質量是34的分子為雙氧水,含有氫氧單鍵和氧氧單鍵,結構式為H-O-O-H;
(3)由以上某些元素組成的化合物A、B、C、D有如下轉化關系:![]() (在水溶液中進行),其中C是溶于水顯酸性的氣體,D是淡黃色固體,則D是Na2O2,C是CO2,過氧化鈉是離子化合物,電子式為
(在水溶液中進行),其中C是溶于水顯酸性的氣體,D是淡黃色固體,則D是Na2O2,C是CO2,過氧化鈉是離子化合物,電子式為![]() ;
;
①如果A、B均由三種元素組成,B為兩性不溶物,則B是Al(OH)3,D是過氧化鈉、C是二氧化碳,A是偏鋁酸鈉,偏鋁酸鈉和二氧化碳反應生成氫氧化鋁和碳酸根離子或碳酸氫根離子,離子反應方程式為:AlO2-+2H2O+CO2=Al(OH)3+HCO3-或2AlO2-+3H2O+CO2=2Al(OH)3+CO32-;
②如果A由三種元素組成,B由四種元素組成,A、B溶液均顯堿性,則A為Na2CO3、B為NaHCO3,碳酸鈉轉化為碳酸氫鈉的離子方程式為CO32-+H2O+CO2=2HCO3-。


 藍天教育暑假優化學習系列答案
藍天教育暑假優化學習系列答案科目:高中化學 來源: 題型:
【題目】某新型電池,以NaBH4(B的化合價為+3價)和H2O2作原料,負極材料采用Pt,正極材料采用MnO2(既作電極材料又對該極的電極反應具有催化作用),該電池可用作衛星、深水勘探等無空氣環境電源,其工作原理如圖所示。下列說法不正確的是

A. 每消耗3mol H2O2,轉移6mol e﹣
B. 電池工作時Na+從b極區移向a極區
C. a極上的電極反應式為:BH4﹣+8OH﹣﹣8e﹣═BO2﹣+6H2O
D. b極材料是MnO2,該電池總反應方程式:NaBH4 + 4H2O2===NaBO2 + 6H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業焊接鋼管常用55137Cs進行“無損探傷”.下列有關說法正確的是( )
A.137表示質量數
B.137表示質子數
C.該原子質子數大于中子數
D.55表示中子數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,對于可逆反應X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始濃度分別為c1、c2、c3(均不為零),達到平衡時,X、Y、Z的濃度分別為0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,則下列判斷正確的是( )
2Z(g),若X、Y、Z的起始濃度分別為c1、c2、c3(均不為零),達到平衡時,X、Y、Z的濃度分別為0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,則下列判斷正確的是( )
A. c1∶c2=3∶1 B. 平衡時,Y和Z的生成速率之比為2∶3
C. X、Y的轉化率不相等 D. c1的取值范圍為0<c1<0.14 mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖表示不同溫度下水溶液中c(H+)與c(OH﹣)的關系,下列判斷正確的是( )
A.兩條曲線上任意點均有c(H+)×c (OH﹣)=Kw
B.T<25
C.b點和c點pH均為6,溶液呈酸性
D.只采用升溫的方式,可由a點變成d點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)為了驗證Fe3+與Cu2+氧化性強弱,下列裝置能達到實驗目的的是_______。

(2)將CH4設計成燃料電池,其利用率更高,裝置如圖所示(A、B為多孔碳棒)。
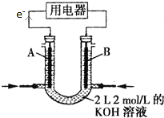
A處其電極反應式為___________;
(3)某元素的同位素![]() ,它的氯化物XCl21.11g溶于水配成溶液后,加入1mo1/L的AgNO3溶液20mL,恰好完全反應。若這種同位素的原子核內有20個中子,Z的值為_____,A的值為______。
,它的氯化物XCl21.11g溶于水配成溶液后,加入1mo1/L的AgNO3溶液20mL,恰好完全反應。若這種同位素的原子核內有20個中子,Z的值為_____,A的值為______。
(4)將固體NH4Br置于密閉容器中,在某溫度下,發生下列反應:
NH4Br(s)![]() NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g)![]() Br2(g)+H2(g)
Br2(g)+H2(g)
2min后,測知c(H2)=0.5mo/L,c(HBr)=4mol/L。若上述反應速率用v(NH3)表示,則v(NH3)=_____
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的數值,下列說法不正確的是
A. 1mol甲基(-CH3)中含有的電子數為9NA
B. 標準狀況下,22.4LCH2=CH2中含C-H數為4NA
C. 1mol分子式為C2H6O的物質,含O-H數一定是NA
D. 0.1mol由乙烯與乙醇組成的混合物完全燃燒所消托的氧氣分子數為0.3NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某公司設計的用于驅動潛艇的液氨﹣液氧燃料電池示意圖如下,有關說法正確的是( )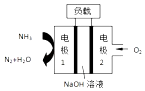
A.電池總反應為:4NH3+3O2=2N2+6H2O
B.電池工作時,OH﹣向正極移動
C.電極 2 發生的電極反應為:O2+4H++4e﹣=2H2O
D.電流由電極 1 經外電路流向電極2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com