
【題目】電解飽和食鹽水,2NaCl+2H2O ![]() H2↑+Cl2↑+2NaOH 生成4mol 的NaOH,(a為飽和食鹽水),下列說法正確的是
H2↑+Cl2↑+2NaOH 生成4mol 的NaOH,(a為飽和食鹽水),下列說法正確的是

A. 在X極生成2mol Cl2 B. 在X極生成2molH2
C. 在Y極生成4mol Cl2 D. NaOH在Y極生成
科目:高中化學 來源: 題型:
【題目】金屬及其相關化合物在化工、醫藥、材料等領域有著廣泛的應用。回答下列問題:
(1)下列關于金屬及金屬鍵的說法不正確的是______。(填字母代號)
a.金屬鍵沒有方向性與飽和性
b.金屬鍵是金屬原子與自由電子間的相互作用
c.金屬熔沸點不同的原因可以用金屬鍵強弱解釋
d.電子氣理論可解釋金屬材料的延展性,不能解釋金屬有良好的導電性
(2)釩廣泛用于催化及鋼鐵工業,基態釩原子的價層電子排布圖為_________________。
(3)二茂鐵又叫雙環戊二烯基鐵[Fe(C5H5)2],熔點是172.5~173 ℃,100 ℃以上升華,二茂鐵屬于_____晶體。已知分子中的大π鍵可用符號![]() 表示,其中m代表參與形成大π鍵的原子數,n代表參與形成大π鍵的電子數(如苯分子中的大π鍵可表示為
表示,其中m代表參與形成大π鍵的原子數,n代表參與形成大π鍵的電子數(如苯分子中的大π鍵可表示為![]() )。已知二茂鐵的每個茂環帶有一個單位負電荷,則每個環中的大π鍵應表示為________________。
)。已知二茂鐵的每個茂環帶有一個單位負電荷,則每個環中的大π鍵應表示為________________。
(4)銅可以形成一種離子化合物[Cu(NH3)4(H2O)2]SO4,若要確定[Cu(NH3)4(H2O)2]SO4是晶體還是非晶體,最科學的方法是對其進行______實驗,其中陰離子的空間構型是_____,該化合物加熱時首先失去的組分是H2O,原因是_______________________。
(5)最近發現,只含鎂、鎳和碳三種元素的晶體也具有超導性,該物質形成的晶體的立方晶胞結構如圖所示。
①與Mg緊鄰的Ni有________個。
②原子坐標參數可表示晶胞內部各原子的相對位置。該晶胞中原子的坐標參數為a為(0,0,0);b為(1/2,1/2,0);d為(1,1,1)。則c原子的坐標參數為_______。
③若晶胞中Ni、Mg之間的最短距離為a pm,阿伏加德羅常數的值為NA,則晶體的密度ρ=______g·cm-3(用含a、NA的代數式表示)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】請按要求填空:
(1)Mg是第3周期元素,該周期部分元素氟化物的熔點見下表:
氟化物 | NaF | MgF2 | SiF4 |
熔點/K | 1266 | 1534 | 183 |
①解釋表中氟化物熔點差異的原因:
a._________________________________________________。
b.__________________________________。
②硅在一定條件下可以與Cl2反應生成SiCl4,試判斷SiCl4的沸點比CCl4的________(填“高”或“低”),理由__________________________________。
(2)下列物質變化,只與范德華力有關的是_________
a.干冰熔化 b.乙酸汽化
c.石英熔融 d.HCONHCH3CH3溶于水
e.碘溶于四氯化碳
(3)C,N元素形成的新材料具有如下圖所示結構, 該晶體的化學式為:_______________。該晶體硬度將超過目前世界上最硬的金剛石,其原因是________________________。

(4)FeCl3常溫下為固體,熔點282 ℃,沸點315 ℃,在300 ℃以上升華。易溶于水,也易溶于乙醚、丙酮等有機溶劑。據此判斷FeCl3的晶體類型為_________________。
(5)氮化碳和氮化硅晶體結構相似,是新型的非金屬高溫陶瓷材料,它們的硬度大,熔點高、化學性質穩定。
①氮化硅的硬度________(“大于”或“小于”)氮化碳的硬度,原因是________________。
②下列物質熔化時所克服的微粒間的作用力與氮化硅熔化時所克服的微粒間的作用力相同的是_________。
a.單質I2和晶體硅 b.冰和干冰
c.碳化硅和二氧化硅 d.石墨和氧化鎂
③已知氮化硅的晶體結構中,原子間都以單鍵相連,且氮原子與氮原子不直接相連、硅原子與硅原子不直接相連,同時每個原子都滿足8電子穩定結構,請寫出氮化硅的化學式________。
(6)第ⅢA,ⅤA元素組成的化合物GaN、GaP、GaAs等是人工合成的新型半導體材料,其晶體結構與單晶硅相似。在GaN晶體中,每個Ga原子與______個N原子相連,與同一個Ga原子相連的N原子構成的空間構型為________。在四大晶體類型中,GaN屬于_______晶體。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮和氮的相關化合物在很多領域有著廣泛的應用。請回答:
I.搭載“神舟十一號”的長征-2F火箭使用的推進劑燃料由N、H兩種元素組成,且原子個數N:H=1:2,其水溶液顯堿性。
(1)該物質中N原子的雜化方式為________,溶于水呈堿性的原因為___________(用離子方程式表示)。
(2)氮元素的第一電離能比相鄰的氧元素大,其原因為________________。
II.笑氣(N2O)曾被用作麻醉劑,但過度吸食會導致身體機能紊亂。
(3)預測N2O的結構式為________________。
(4)在短周期元素組成的物質中,寫出與NO2-互為等電子體的分子_________。(寫兩個,填分子式)
III.氮化鈦為金黃色晶體,有仿金效果,越來越多地成為黃金的代替品。
(5)Ti金屬晶體的堆積模型為________,配位數為_______,基態Ti3+中未成對電子數有______個。
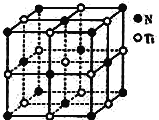
(6)氮化鈦晶體的晶胞與NaCl晶胞相似(如圖所示),該氮化鈦的密度為ρg·cm-3,則該晶胞中N、Ti之間的最近距離為______nm(NA為阿伏加德羅常數的值,只列計算式)。該晶體中與氮原子距離相等且最近的鈦原子圍成的空間幾何體為____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】五氧化二釩及其他釩的化合物廣泛應用于鋼鐵、有色合金、化工、煉油、玻璃及陶瓷等工業部門。可從含釩石煤灰渣中提釩,該試驗工藝流程如下圖:

表1 灰渣主要化學成分分析/%
V2O3 | SiO2 | Fe2O3 | Al2O3 | MgO | K2O | CaO | 燒失量 |
1.26 | 55.71 | 6.34 | 7.54 | 1.26 | 3.19 | 1.41 | 20.55 |
表2中間鹽主要成分分析/%(以氧化物形式表示其含量)
V2O3 | Al2O3 | Fe2O3 | MgO | K2O |
5.92 | 1.70 | 18.63 | 2.11 | 3.38 |
已知:
①石煤灰渣的化學成分分析見表1,中間鹽的主要成分分析見表2。
②礦物焙燒過程中,若溫度過高,易發生燒結,溫度越高,燒結現象越嚴重。
③萃取反應可以表示為:VO2++(HR2)PO4(o)→VO[R2PO4]R(o)+H+,(o)表示有機相
④有機萃取劑(HR2)PO4萃取VO2+的能力比萃取V02+要強。
請回答:
(1)提高浸取率的方法有____________,殘渣的主要成分為______________________,
(2)經幾級萃取后,有時候要適當加酸調整pH值,結合萃取反應方程式,說明原因_____________。反萃取操作應加入_____________試劑。
(3)中間鹽溶解過程中,加鐵粉的主要目的是_____________________。
(4)石煤中的釩以V(Ⅲ)為主,有部分V(Ⅳ),很少見V(Ⅴ)。如圖1和如圖2分別為焙燒溫度和焙燒時間對釩浸出率的影響,由如圖2可得最佳焙燒時間為______________h,由如圖1可得最佳焙燒溫度為800-850℃之間,焙燒溫度在850℃以下時,釩浸出率隨焙燒溫度的上升幾乎直線上升的原因是_________________________,當焙燒溫度高超過850℃以后,再提高溫度,浸出率反而下降的可能原因是:_________________________。

(5)反萃取液中的VO2+,加入氯酸鈉后被氧化為VO2+,請寫出該反應的離子方程式______________。然后用氨水調節pH到1.9~2.2沉釩,得多釩酸銨沉淀(化學式為(NH4)2V12O31·nH2O),再經固液分離、干燥、焙燒得五氧化二釩產品,請寫出此步反應的化學方程式____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】最近我國科學家在液流電池研究方面取得新進展。一種硫/碘體系(KI/K2S2)的液流電池工作原理如圖所示。下列說法正確的是( )

A. 放電時電池右側為負極,發生氧化反應
B. 放電時電池左側的電極反應為S22-+2e-==2S2-
C. 充電時電解質溶液中K經交換膜向右側移動
D. 充電時電池的總反應為3I-+S22-=I3-+2S2-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化氯(ClO2)是國際上公認的安全、無毒的綠色消毒劑。常溫下二氧化氯為黃綠色氣體,其熔點為-59.5℃,沸點為11.0℃,極易溶于水,不與水反應。若溫度過高,二氧化氯的水溶液可能會發生爆炸。某研究性學習小組擬用如下圖所示裝置制取并收集ClO2(加熱和夾持裝置均省略)。

(1)在圓底燒瓶中先放入一定量的KClO3和草酸H2C2O4),然后再加入足量的稀硫酸,在60~80℃之間反應生成ClO2、CO2和一種硫酸鹽,該反應的化學方程式為________。
(2)裝置A中使用溫度計的目的是____。反應開始后,可以觀察到圓底燒瓶內的現象是_____。
(3)裝置B的作用是________。
(4)實驗過程中裝置D中的溶液里除生成Na2CO3外,還生成物質的量之比為1︰1的另外兩種鹽,一種為NaClO3,另一種為_______。
(5)ClO2很不穩定,需隨用隨制,產物用水吸收得到ClO2溶液。為測定所得溶液中ClO2的含量,進行了下列實驗:
步驟1:量取ClO2溶液20mL,稀釋成100mL試樣,量取V1mL試樣加入到錐形瓶中;
步驟2:調節試樣的pH≤2.0,加入足量的KI晶體,振蕩后,靜置片刻;
步驟3:加入指示劑X,用 cmol·L-1Na2S2O3標準溶液滴定至終點,消耗Na2S2O3溶液V2mL。
已知:2ClO2+8H++10I-==5I2+2C1-+4H2O 2Na2S2O3+I2=Na2S4O6+2NaI
請回答:
①配制100mL步驟3中所需的Na2S2O3標準溶液時,用到的玻璃儀器除燒杯、量筒、玻璃棒、膠頭滴管外,還需要_______。(填儀器名稱)
②步驟3中滴定終點的現象為_______。
③原ClO2溶液的濃度為_______g·L-1(用含字母的代數式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分析下列硫燃燒時的能量變化圖,判斷有關熱化學方程式和說法正確的是( )

A. S(s,單斜)+O2(g)===SO2(g) ΔH=+297.16 kJ·mol-1
B. S(s,正交)===S(s,單斜) ΔH=-0.33 kJ·mol-1
C. S(s,正交)+O2(g)===SO2(g) ΔH=-296.83 kJ·mol-1
D. 單斜硫的穩定性大于正交硫的穩定性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法與鹽類水解有關且正確的是: ( )
A. AlCl3溶液和NaAlO2溶液加熱、蒸發、濃縮、結晶、灼燒,所得固體的成分相同
B. 配制FeCl3溶液時,將FeCl3固體溶解在硫酸中,然后再用水稀釋到所需的濃度
C. 用加熱的方法可除去KCl溶液中混有的Fe3+
D. 食醋可以溶解水垢
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com