





 Ո�ش����І��}��
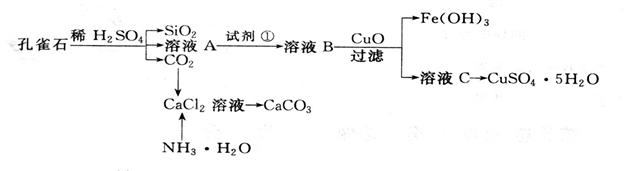
Ո�ش����І��}�� ��1����ҺA�Ľ����x����__________���z���ҺA��Fe3+�����ԇ���� ��
��1����ҺA�Ľ����x����__________���z���ҺA��Fe3+�����ԇ���� ��  A��KMnO4�� ���� B��(NH4) 2S C��H2O2 D��KSCN
A��KMnO4�� ���� B��(NH4) 2S C��H2O2 D��KSCN  ��2������ҺC�@��CuSO4��5H2O����Ҫ���^�ӟ����l(f��)������ �������^�V�Ȳ�����
��2������ҺC�@��CuSO4��5H2O����Ҫ���^�ӟ����l(f��)������ �������^�V�Ȳ����� ��3���Ƃ�CaCO3�r������CaCl2��Һ���ȼ���NH3.H2O,Ȼ��ͨ��CO2�������ķ���ʽ��__________________________________________________________________��
��3���Ƃ�CaCO3�r������CaCl2��Һ���ȼ���NH3.H2O,Ȼ��ͨ��CO2�������ķ���ʽ��__________________________________________________________________��


 ��4�����y����ҺA��Fe2+�ĝ�ȣ���Ҫ������ƿ����ij�˜���Һ����KMnO4�˜���Һ�ζ��r���x���� �� �����ζ��ܣ����ʽ���Aʽ������
��4�����y����ҺA��Fe2+�ĝ�ȣ���Ҫ������ƿ����ij�˜���Һ����KMnO4�˜���Һ�ζ��r���x���� �� �����ζ��ܣ����ʽ���Aʽ������ ��x��܇ϵ�д�
��x��܇ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ����Ԕ �}�ͣ�����}
| ���| | FeSO4 | H2SO4 | Ag2SO4 | Al2(SO4)2 | ���� |
| �|���֔��������� | 15.0 | 7.0 | 0.40 | 0.34 | 5.0 |
| �ض�/�� | 0 | 10 | 20 | 30 | 40 | 50 |
| FeSO4��Һ�ȣ�g�� | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 |
| Al2(SO4)3�ܽ�ȣ�g�� | 31.2 | 33.5 | 36.4 | 40.4 | 45.7 | 52.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ����Ԕ �}�ͣ�����}
 ij�����W��С�M��ͬ�W�M�C�����е���Ч�ɷֲ��y���������ȵĺ������Ø�Ʒ���ᷴ���a���������ȵ��|���c��Ʒ�|���ı�ֵ����������Ո�ش����І��}��
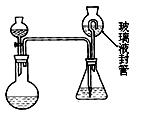
ij�����W��С�M��ͬ�W�M�C�����е���Ч�ɷֲ��y���������ȵĺ������Ø�Ʒ���ᷴ���a���������ȵ��|���c��Ʒ�|���ı�ֵ����������Ո�ش����І��}�� ��1�����C������(w��n)���Զ���������Һ���к����c�x�ӣ������_�IJ������E�ǣ� ��
��1�����C������(w��n)���Զ���������Һ���к����c�x�ӣ������_�IJ������E�ǣ� �� ��2����y������(w��n)���Զ���������Һ���ж������ȵĺ������F�M�����²�������ȡmg��2g���ң�
��2����y������(w��n)���Զ���������Һ���ж������ȵĺ������F�M�����²�������ȡmg��2g���ң� ԇ�ӣ����ڟ�ƿ�У����Һ©���м���10mL�}����Һ�������F��ƿ�м���4g�⻯⛣���100mLˮ�ܽ���ټ�3mL������Һ�����ڲ���Һ����м���ˮ���܌���Һ©���е��}����Һ�����ƿ�У��P�]�����������ӟ��ƿ��ʹ�a���Ķ������Ț��wȫ��ͨ�^�������F��ƿ�б����գ�������Һ����е�ˮ��Һ�����F��ƿ�У�����ε�����Һ����cmol/L��������c�˜���Һ�ζ����{ɫ��ʧ(I2+2S2O32-=2I- +S4O62-)������ȥVmL��������c��Һ��
ԇ�ӣ����ڟ�ƿ�У����Һ©���м���10mL�}����Һ�������F��ƿ�м���4g�⻯⛣���100mLˮ�ܽ���ټ�3mL������Һ�����ڲ���Һ����м���ˮ���܌���Һ©���е��}����Һ�����ƿ�У��P�]�����������ӟ��ƿ��ʹ�a���Ķ������Ț��wȫ��ͨ�^�������F��ƿ�б����գ�������Һ����е�ˮ��Һ�����F��ƿ�У�����ε�����Һ����cmol/L��������c�˜���Һ�ζ����{ɫ��ʧ(I2+2S2O32-=2I- +S4O62-)������ȥVmL��������c��Һ�� ����ʽ�飺
����ʽ�飺 �������ȱ�߀ԭ�����x�ӣ�ԓ�������x�ӷ���ʽ�飺 ��
�������ȱ�߀ԭ�����x�ӣ�ԓ�������x�ӷ���ʽ�飺 �� �����b���в���Һ��ܵ������ǣ� ����δ_����ƿ��
�����b���в���Һ��ܵ������ǣ� ����δ_����ƿ�� �Ķ�������ȫ�����F��ƿ�е�Һ�w���� ��
�Ķ�������ȫ�����F��ƿ�е�Һ�w���� �� ������(w��n)���Զ���������Һ���У�ClO2���|���֔���
������(w��n)���Զ���������Һ���У�ClO2���|���֔���  ����m��c��V��ʾ����
����m��c��V��ʾ�����鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ����Ԕ �}�ͣ�����}
| A���������cϡ��Һ | B��̼���cϡ��Һ |
| C�������y��Һ | D�����Ȼ�̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ����Ԕ �}�ͣ�����}
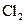 ��
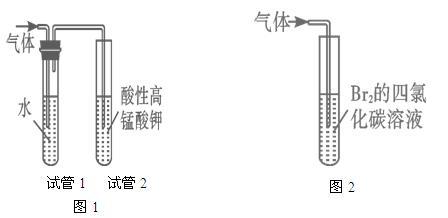
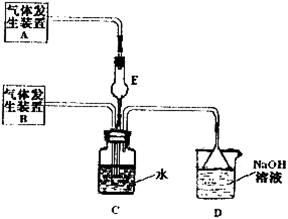
��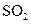 ���w���F����Na2SO3�c70%�ĝ������ԭ����ȡSO2������MnO2�͝��}���ԭ����ȡC12���ڴˌ���У�E�x����������__________���l(f��)���b��B���x���������N�b���е�___________������̖����
���w���F����Na2SO3�c70%�ĝ������ԭ����ȡSO2������MnO2�͝��}���ԭ����ȡC12���ڴˌ���У�E�x����������__________���l(f��)���b��B���x���������N�b���е�___________������̖����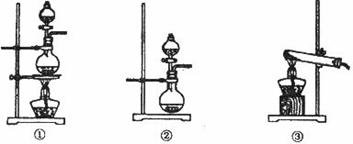
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ����Ԕ �}�ͣ�����}
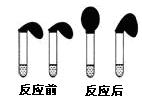
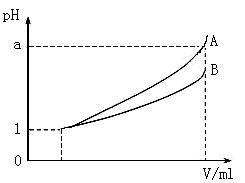
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ����Ԕ �}�ͣ�����}
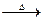 CH3COOH+Cu2O��+2H2O��������|�ɣ����M������̽����
CH3COOH+Cu2O��+2H2O��������|�ɣ����M������̽����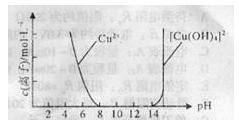
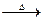 CH3COOH+Cu2O��+2H2O���|�ɵ����ɣ�
CH3COOH+Cu2O��+2H2O���|�ɵ����ɣ��鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ����Ԕ �}�ͣ�����}
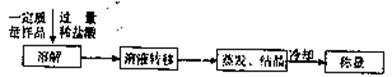
 |
| | 50mLϡ���� | 50mLϡ���� | 50mLϡ���� |
| m������ | 9��2g | 15��7g | 27��6g |
| V��CO2�����˛r�� | 2��24L | 3��36L | 3��36L |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ����Ԕ �}�ͣ����x�}
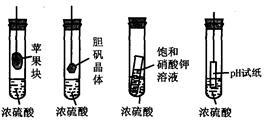
| A���O���K���ɰT | B��đ�\���w�����С��װߡ� |
| C��Сԇ�܃��о��w���� | D��pHԇ��׃�t |
�鿴�𰸺ͽ���>>
���H�WУ��(y��u)�x - �������б� - ԇ�}�б�
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com