
如圖中,A、B、C、D、E是單質,F、G、H、I是B、C、D、E分別和A形成的化合物。已知:①G、H的化學式為“X2Y3”形式,F的化學式為“XY”形式;②I是一種常見的氣體,能使澄清石灰水變渾濁,固態I用于人工降雨, E可以在I中燃燒,發生置換反應;③F中的A元素的質量分數為40%。回答問題:

(1)I和E反應的化學方程式為: 。(2分)
(2)C既能與鹽酸反應,又能與氫氧化鈉溶液反應。C和A形成的化合物H與氫氧化鈉溶液反應的離子方程式為: 。(2分)電解H可以制取C, 反應的化學方程式為: 。(2分)
(3)G是一種紅棕色粉末,向一定量的G中加入足量硫酸,反應的化學方程式為: 。(2分)向反應后的溶液中加入足量鐵粉,反應的離子方程式為: 。(2分)
(4)G與鹽酸反應的離子方程式為: 。(2分)得到的溶液中加入銅粉,反應的離子方程式為: 。(2分)1.6g G 溶于鹽酸,得到的溶液與銅粉完全反應,至少需銅粉 g(3分)。
(1)2Mg+CO2 2MgO+C(2分)(2)Al2O3+2OH-=2AlO2-+H2O(2分)
2MgO+C(2分)(2)Al2O3+2OH-=2AlO2-+H2O(2分)
2Al2O3 4Al+3O2↑(2分)
4Al+3O2↑(2分)
(3)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O(2分)2Fe3++Fe=3Fe2+(2分)
(4)Fe2O3+6H+=2Fe3++3H2O(2分) Cu+2Fe3+=Cu2++2Fe2+(2分) 0.64g(1分)
解析試題分析:I是一種常見的氣體,能使澄清石灰水變渾濁,固態I用于人工降雨,這說明I是二氧化碳。E可以在I中燃燒,發生置換反應2E+I=2F+D,推斷E為金屬單質Mg,發生的反應為,2Mg+CO2 2MgO+C,F為MgO,D為單質C;MgO中的氧元素的質量分數為40%,證明推斷正確.因此E是鎂,則A是氧氣,D是碳,F是氧化鎂。
2MgO+C,F為MgO,D為單質C;MgO中的氧元素的質量分數為40%,證明推斷正確.因此E是鎂,則A是氧氣,D是碳,F是氧化鎂。
(1)I和E反應的化學方程式為2Mg+CO2 2MgO+C。
2MgO+C。
(2)C既能與鹽酸反應,又能與氫氧化鈉溶液反應,說明C是金屬鋁。C和A形成的化合物H是氧化鋁,屬于兩性氧化物與氫氧化鈉溶液反應的離子方程式為Al2O3+2OH-=2AlO2-+H2O;電解氧化鋁可以制取鋁, 反應的化學方程式為2Al2O3 4Al+3O2↑。
4Al+3O2↑。
(3)G是一種紅棕色粉末,則G是氧化鐵。向一定量的G中加入足量硫酸,反應的化學方程式為Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;鐵離子能氧化單質鐵,因此向反應后的溶液中加入足量鐵粉,反應的離子方程式為2Fe3++Fe=3Fe2+。
(4)氧化鐵與鹽酸反應的離子方程式為Fe2O3+6H+=2Fe3++3H2O;鐵離子能氧化單質銅,因此得到的溶液中加入銅粉,反應的離子方程式為Cu+2Fe3+=Cu2++2Fe2+;1.6g 氧化鐵的物質的量是1.6g÷160g/mol=0.01mol,根據方程式Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=Cu2++2Fe2+可知 Fe2O3~Cu,則需要銅的物質的量是0.01mol,銅粉的質量是0.64g。
考點:考查無機物推斷


科目:高中化學 來源: 題型:單選題
A~G各物質間的關系如下圖所示,其中B、D為氣體單質。則下列說法錯誤的是
A.若反應①在常溫下進行,則1 mol A在反應中能轉移1 mol電子
B.反應②的離子方程式為MnO2+4H++2Cl- Mn2++2H2O+Cl2↑
Mn2++2H2O+Cl2↑
C.新配制的F溶液一般需要加入鐵屑和稀鹽酸,前者用于防止Fe2+被空氣氧化成Fe3+,后者可抑制Fe2+的水解
D.已知C的濃溶液在催化劑存在的條件下加熱,能與B反應生成D,由此可以推斷B的氧化性比MnO2強
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(13分).巳知 A、B、D為中學常見的單質,甲、乙、丙、丁、戊為短周期元素組成的化合物。其中,丙是一種能使濕潤的紅色石蕊試紙變藍的無色氣體;丁是一種高能燃料,其組成元素與丙相同,1 mol 丁分子中不同原子的數目比為1 :2,且含有18 mol電子;戊是一種難溶于水的白色膠狀物質,既能與強酸反應,也能與強堿反應,具有凈水作用。各物質間的轉化關系如下圖所示(某些條件巳略去)。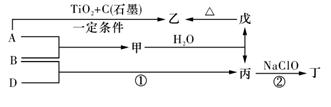
請回答:(1)單質B的組成元素在周期表中的位置是_________。
(2)戊的化學式為________。戊與強堿反應的離子方程式:________________
(3)丙中所包含的化學鍵類型有________ (填字母序號)。
a.離子鍵 b.極性共價鍵 c.非極性共價鍵
(4)反應①的化學方程式為________________________。
(5)反應②中,0.5mol NaClO參加反應時,轉移1 mol電子,其化學方程式為_________
(6)—定條件下,A與TiO2、C(石墨)反應只生成乙和碳化鈦(TiC),二者均為某些高溫結構陶瓷的主要成分。巳知,該反應生成1 mol乙時放出536 kJ熱量,其熱化學方程式為_______________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
中學化學中的一些常見物質有下圖轉化關系(部分產物未給出)。其中A的焰色呈黃色,D常溫下為黃綠色氣體,反應③為侯氏制堿法反應原理之一,E是常見的金屬。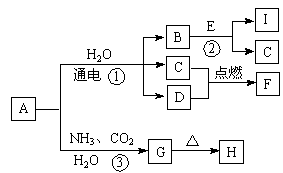
回答下列問題。
(1)F的電子式為 。
(2)G的化學式為 。
(3)寫出反應①的化學方程式 。
(4)寫出反應②的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A~H均為短周期元素,A~F在元素周期表中的相對位置如圖1所示,G與其它七種元素
| 圖1 | |||
| A | B | C | |
| D | | E | F |
| 圖2 | |||
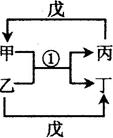 | |||
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在下圖轉化關系中,固體甲的焰色反應呈黃色,M為常見的液體物質,I為一常見金屬,酸G是重要的化工產品和化工原料;固體H能夠溶解在A溶液和酸G中,且H為良好的耐火材料(圖中部分產物沒有列出)。
(1)固體甲與液體M反應的方程式為______。A溶液與固體H反應的離子方程式為______。
(2)固體乙的化學式為_______。液體M的電子式為_______。
(3)反應①~⑦中屬于氧化還原反應的為_______(填寫反應序號)。
(4)若I與C的稀溶液不反應,只能與G的濃溶液在加熱條件下反應,則反應⑦的化學方程式為_______。
(5)若由黃鐵礦(FeS2)與氣體B反應來生產氣體E,且每生成1 mol E放出426.5 kJ的熱量,該反應的熱化學方程式為_______ 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下圖是無機物A~M在一定條件下的轉化關系(部分產物及反應條件未列出)。其中,I是由第三周期元素組成的單質中熔點最高的金屬,K是一種紅棕色氣體。
提示:4FeS2+11O2高溫,2Fe2O3+8SO2
請填寫下列空白:
(1)在周期表中,組成單質G的元素位于第________周期________族。
(2)在反應⑦中氧化劑與還原劑的物質的量之比為________。
(3)在②、③、⑥、⑨中既屬于化合反應又屬于非氧化還原反應的是________(填序號)。
(4)反應④的離子方程式是_____________________________________。
(5)將化合物D與KNO3、KOH共熔,可制得一種“綠色”環保高效凈水劑K2FeO4(高鐵酸鉀),同時還生成KNO2和H2O。該反應的化學方程式是________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在下圖所示的物質轉化關系中,A是海水中含量最豐富的鹽,B是常見的無色液體,G的水溶液是一種常用的漂白劑,F是地殼中含量最多的金屬元素。(反應中生成的水和部分反應條件未列出)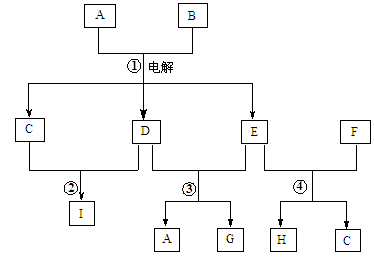
(1)畫出A中陰離子的結構示意圖 。
(2)反應②在點燃條件下的現象是 。
(3)H轉化為F的氫氧化物最好選擇的試劑是 。
(4)反應③的離子方程式為 。
(5)反應④的離子方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
X、Y、Z、W是原子序數依次增大的四種短周期元素,A、B、C、D、F都是由其中的兩種或三種元素組成的化合物,E是由Z元素形成的單質,0.1 mol·L-1 D溶液的pH為13(25 ℃)。它們滿足如圖轉化關系,則下列說法正確的是( )。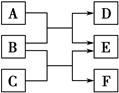
A.原子半徑W>Z>Y>X
B.0.1 mol·L-1 F溶液中陰離子總的物質的量大于0.1 mol·L-1 D溶液中陰離子總的物質的量
C.0.1 mol B與足量C完全反應共轉移電子數0.1NA
D.Z元素的最高正價為+6
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com