
科學家一直致力于“人工固氨”的新方法研究。目前合成氨技術原理為:N2(g) +3H2(g)  2NH3(g)+92.4 kJ/mol673K,30MPa下,上述合成氨反應中n(NH3)和n(H2)隨時間變化的關系如右圖所示。
2NH3(g)+92.4 kJ/mol673K,30MPa下,上述合成氨反應中n(NH3)和n(H2)隨時間變化的關系如右圖所示。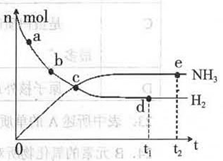
(1)下列敘述正確的是
A.點a的正反應速率比點b的大
B.點c處反應達到平衡
C.點d和點e處的n (N2)相同
D.773K,30MPa 下,反應至t2時刻達到平衡,則n(NH3)比圖中e點的值大
(2)在容積為2.0 L恒容得密閉容器中充入0.80 mol N2(g)和1.60 mol H2(g),673K、30MPa下達到平衡時,NH3的體積分數為20%。該條件下,N2(g)+3H2(g)  2NH3(g)的平衡常數值為:___。
2NH3(g)的平衡常數值為:___。
(3)K值越大,表明反應達到平衡時( )。
A. H2的轉化率一定越高 B.NH3的產量一定越大
C.正反應進行得越完全 D.化學反應速率越大
(4)1998年希臘亞里斯多德大學的兩位科學家采用高質子導電性的SCY陶瓷(能傳遞H+),實現了高溫、常壓下高轉化率的電解合成氨。其實驗裝置如圖。陽極的電極反應為:H2-2e→2H+,則陰極的電極反應為:_____________。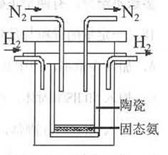
(本題共8分)(1)AC(2分)(2)K=16/15(或1.07或1.1)(2分)
(3)C(2分) (4)N2+6H+ +6e→2NH3(2分)
解析試題分析:(1)A、a點反應物的濃度大于b點,濃度越大反應速率越快,故a點反應速率更大,A正確;B、點c之后氫氣的物質的量繼續減小,可逆反應未達到平衡狀態,反應向正反應方向進行,故B錯誤;C、d、e對應氫氣、氨氣的物質的量不變,可逆反應處于平衡狀態,點d和點e處的n(N2)相同,故C正確;D、該反應正反應是放熱反應,溫度升高平衡向逆反應方向移動,氨氣的物質的量減小,故D錯誤,答案選AC。
(2)令平衡時轉化的氮氣的物質的量濃度為x,則:
N2(g)+ 3H2(g) 2NH3(g)
2NH3(g)
起始濃度(mol/L) 0.4 0.8 0
轉化濃度mol/L) x 3x 2x
平衡濃度mol/L) 0.4-x 0.8-3x 2x
所以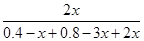 =20%
=20%
解得x=0.1
因此該溫度下平衡常數K=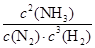 =
=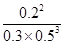 =1.07
=1.07
(3)A、氫氣的轉化率與氮氣、氫氣的投入量等有關,K值大,氫氣轉化率不一定高,故A錯誤;B、氨氣的產率與與氮氣、氫氣的投入量等有關,K值大,氨氣的產量不一定大,故B錯誤;C、K值越大,表示反應正向進行的程度大,即正反應進行得越完全,故C正確;D、K值越大,表示反應正向進行的程度大,但該溫度下不一定反應發生,反應速率不一定大,故D錯誤,答案選C。
(4)電解池的陰極發生得電子的還原反應,在合成氨反應中,氮氣得電子,所以陰極電極反應為N2+6H+ +6e-→2NH3。
考點:考查外界條件對反應速率、平衡狀態的影響;平衡常數的計算以及應用;圖像識別以及電極反應式的書寫等


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:填空題
I.設反應①Fe(s)+CO2(g) FeO(s)+CO(g)的平衡常數為K1。反應 ②Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常數為K1。反應 ②Fe(s)+H2O(g)  FeO(s)+H2(g)的平衡常數為K2,在不同溫度下,K1、K2的值如下:
FeO(s)+H2(g)的平衡常數為K2,在不同溫度下,K1、K2的值如下:
| T(K) | K1 | K2 |
| 973 | 1.47 | 2.36 |
| 1173 | 2.15 | 1.67 |
 CO(g)+H2O(g),這是一個 (填“吸”或“放”)熱反應,要使平衡③向右移動,可采取的措施有 (填序號)。
CO(g)+H2O(g),這是一個 (填“吸”或“放”)熱反應,要使平衡③向右移動,可采取的措施有 (填序號)。 FeO(s)+CO(g)在溫度T1下進行;Fe(s)+H2O(g)
FeO(s)+CO(g)在溫度T1下進行;Fe(s)+H2O(g)  FeO(s)+H2(g)在溫度T2下進行,已知T1>T2,且c(CO2)>c(H2O)(其他條件均相同),則兩者的反應速率 (填序號)。
FeO(s)+H2(g)在溫度T2下進行,已知T1>T2,且c(CO2)>c(H2O)(其他條件均相同),則兩者的反應速率 (填序號)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Cl2合成有機物時會產生副產物HC1。4HCl+O2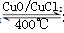 2Cl2+2H2O,可實現氯的循環利用。
2Cl2+2H2O,可實現氯的循環利用。
完成下列填空:
(1)該反應平衡常數的表達式K= ;若反應容器的容積為2L,8min后達到平衡,測得容器內物質由2.5mol減少至2.25mol,則HCl的平均反應速率為 mol/L? min。
(2)若該反應在體積不變的密閉容器中發生,當反應達平衡時,下列敘述正確的是 。
a.v (HCl)="2" v(Cl2)
b.4v正(HCl)= v逆(O2)
c.又加入1mol O2,達新平衡時,HCl的轉化率增大
d.分離出H2O,達新平衡時,v正(HCl)增大
(3)下圖是該反應兩種投料比[n (HCl):n (O2)分別為4:1和2:1 ] 下,反應溫度對HCl平衡轉化率影響的曲線。下列敘述正確的是 。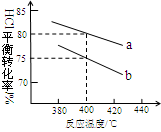
a.該反應的正反應是放熱反應
b.其他條件不變,升高溫度,平衡常數K值增大
c.若平衡常數K值變大,達新平衡前v逆始終減小
d.若平衡常數K值變大,則平衡向正反應方向移動
(4)投料比為4:1、溫度為400℃時,平衡混合物中Cl2的物質的量分數是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(甲醇是重要的化學工業基礎原料和清潔液體燃料,它廣泛用于有機合成、醫藥、農藥、涂料、染料、汽車和國防等工業中。工業上一般在恒容密閉容器中采用下列反應合成甲醇:
CO(g) 2H2(g)
2H2(g)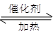 CH3OH(g)
CH3OH(g) Q
Q
下表所列數據是反應在不同溫度下的化學平衡常數(K)。
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
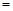 ”或“<”),要提高CO轉化率,可采取的措施
”或“<”),要提高CO轉化率,可采取的措施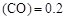 mol/L,則以CH3OH表示的反應速率v
mol/L,則以CH3OH表示的反應速率v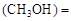 mol /(L·min),
mol /(L·min), CO2(g)
CO2(g)  2CO(g) 平衡常數K1
2CO(g) 平衡常數K1 H2O(g)
H2O(g)  CO(g)
CO(g) H2(g) 平衡常數K2
H2(g) 平衡常數K2 H2O(g)
H2O(g)  H2(g)
H2(g) CO2(g) 平衡常數K3
CO2(g) 平衡常數K3查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鉛及其化合物工業生產及日常生活具有非常廣泛的用途。
(1)瓦紐科夫法熔煉鉛,其相關反應的熱化學方程式如下:
2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) ΔH=" a" kJ/mol
PbS(s)+2PbO(s)=3Pb(s)+SO2(g) ΔH=" b" kJ·mol-1
PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) ΔH=" c" kJ·mol-1
反應3PbS(s) + 6O2(g) = 3PbSO4(s) ΔH="kJ" ·mol-1(用含a,b ,c的代數式表示)。
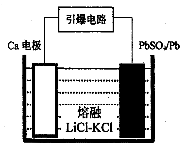
(2)還原法煉鉛,包含反應PbO(s)+CO(g)  Pb(s) + CO2(g) ΔH,該反應的平衡常數的對數值與溫度的關系如下表
Pb(s) + CO2(g) ΔH,該反應的平衡常數的對數值與溫度的關系如下表
| 溫度 | 300 | 727 | 1227 |
| lgK | 6.17 | 2.87 | 1.24 |



查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(Ⅰ)銅鐵及其化合物在日常生活中應用廣泛,某研究性學習小組用粗銅(含雜質Fe)與過量氯氣反應得固體A,用稀鹽酸溶解A,然后加試劑調節溶液的pH后得溶液B,溶液B經系列操作可得氯化銅晶體,請回答:
(1)固體A用稀鹽酸溶解的原因是 ;
(2)檢驗溶液B中是否存在Fe3+的方法是 ;
(3)已知元素在高價態時常表現氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加熱,生成CuCl沉淀,則生成CuCl的離子方程式是 ;
(Ⅱ)(1) 常溫下,某同學將稀鹽酸與氨水等體積混合,兩種溶液的濃度和混合后所得溶液的pH如下表:
| 實驗編號 | 氨水物質的量濃度 (mol·L-1) | 鹽酸物質的量濃度 (mol·L-1) | 混合溶液 pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | C | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH>7 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一個固定體積的密閉容器中,向容器中充入2 mol A 和1 mol B,發生如下反應:2A(g) + B(g)  3C(g) + D(s),反應達到平衡時C的濃度為1.2 mol/L.
3C(g) + D(s),反應達到平衡時C的濃度為1.2 mol/L.
(1)若使容器溫度升高,平衡時混合氣體的平均相對摩爾質量減小,則正反應為________(填“吸熱”或“放熱”)反應.
(2)若維持容器體積和溫度不變,按下列方法加入起始物質,達到平衡時C的濃度仍為1.2 mol/L的是______(用序號填空).
①4 mol A+2 mol B ②3 mol C+1 mol D+l mol B
③3 mol C+2 mol D ④1.6 mol A+0.8 mol B+0.6 mol C
(3)某溫度下,向容器中加入3 mol C和0.8 mol D,反應達到平衡時C的濃度仍為1.2 mol/L,則容器的容積V應大于________L,小于________L.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com