
【題目】用無水 Na2SO3固體配制 250 mL 0.1000 mol·L-1 溶液的步驟如下圖,請回答:
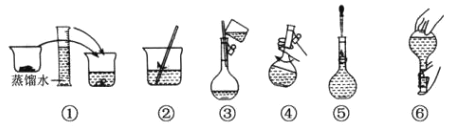
(1)在配制過程中必要的儀器有:燒杯、玻璃棒、膠頭滴管、 250ml 容量瓶和____________;檢驗容量瓶是否漏水的操作方法是____________________________________。
(2)下列操作不會對所配的Na2SO3溶液濃度產生誤差的是__________。
A.容量瓶剛用蒸餾水洗凈,沒有烘干
B.圖③沒有用蒸餾水洗燒杯 2-3 次,并轉移洗液
C.圖⑤時仰視容量瓶的刻度線
D.圖⑥后,發現液面略低于刻度線,再滴加少量水使液面凹面與刻度線相切
(3)已知亞硫酸鈉在空氣中能被氧氣氧化生成硫酸鈉,請設計實驗檢驗配制的 Na2SO3 溶液是否發生變質_______________________。
【答案】 電子天平 在容量瓶中注入水,蓋好瓶塞,右手托住瓶底倒立, 觀察瓶塞是否漏水; 如不漏,將塞旋轉 180 度,再重復檢漏 A 取少量 Na2SO3 溶液,加入鹽酸酸化、 滴加 BaCl2 溶液,若有白色沉淀,則有溶液已變質產生硫酸鈉
【解析】(1)在配制過程中必要的儀器有:燒杯、玻璃棒、膠頭滴管、 250ml 容量瓶和電子天平;檢驗容量瓶是否漏水的操作方法是在容量瓶中注入水,蓋好瓶塞,右手托住瓶底倒立, 觀察瓶塞是否漏水; 如不漏,將塞旋轉 180 度,再重復檢漏。
(2)下列操作A.容量瓶剛用蒸餾水洗凈,沒有烘干,無影響;B.圖③沒有用蒸餾水洗燒杯 2-3 次,并轉移洗液,則溶質減少,所以配得的Na2SO3溶液濃度偏低;C.圖⑤時仰視容量瓶的刻度線,則溶液體積偏大,配得的Na2SO3溶液濃度偏低;D.圖⑥后,發現液面略低于刻度線,再滴加少量水使液面凹面與刻度線相切,則溶液體積偏大,配得的Na2SO3溶液濃度偏低。綜上所述,不會對所配的Na2SO3溶液的濃度產生誤差的是A。
(3)亞硫酸鈉在空氣中能被氧氣氧化生成硫酸鈉,要檢驗配制的 Na2SO3 溶液是否發生變質,可以檢驗硫酸根離子,方法是:取少量 Na2SO3 溶液,加入鹽酸酸化、 滴加 BaCl2 溶液,若有白色沉淀,則有溶液已變質產生硫酸鈉。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】硼酸( H3BO3) 為一元弱酸,H3BO3可以通過電解的方法制備。其工作原理如右圖所示( 陽膜和陰膜分別只允許陽離子、陰離子通過)。下列說法錯誤的是
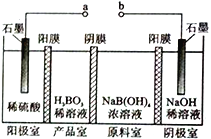
A. a 與電源的正極相連接
B. 陽極的電極反應式為:2H2O-4e-=O2↑+4H+
C. [B(OH)4]-穿過陰膜進入產品室,Na+穿過陽膜進入陰極室
D. 當電路中通過3mol 電子時,可得到1molH3BO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將 NaCl 溶液滴在一塊光亮清潔的鐵板表面上,一段時間后發現液滴覆蓋的圓周中心區(a)已被腐蝕而變暗,在液滴外沿棕色鐵銹環(b),如圖所示。下列說法不正確的是
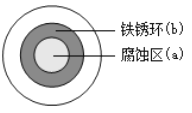
A. 鐵片腐蝕過程發生的總化學方程式為:4Fe+6H2O+3O2 ==4 Fe(OH)3
B. 液滴之下氧氣含量少, 鐵片作負極,發生的氧化反應為: Fe-3e-=Fe3+
C. 液滴邊緣是正極區,發生的電極反應為: O2+2H2O+4e-=4OH-
D. 鐵片腐蝕最嚴重區域不是生銹最多的區域
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關共價鍵鍵參數的的比較中,不正確的是( )
A. 鍵能:C—N < C=N < C≡N
B. 鍵長:I—I > Br—Br > Cl—Cl
C. 分子中的鍵角:H2O > NH3
D. 乙烯分子中碳碳鍵的鍵能:σ鍵 > π鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表列出了某短周期元素R的各級電離能數據(單位為kJ·mol-1)。下列關于元素R的判斷中一定正確的是( )
I1 | I2 | I3 | I4 | …… | |
R | 577.5 | 1816.7 | 2744.8 | 11577 |
①R的主要化合價中最高正價為+3價 ②R元素位于元素周期表中第ⅡA族
③R元素第一電離能小于同周期相鄰元素 ④R元素基態原子的電子排布式為1s22s22p1
A. ①② B. ②③ C. ③④ D. ①③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組數據中,前者剛好是后者兩倍的是 ( )
A. 2 mol H2O的摩爾質量和1 mol H2O的摩爾質量
B. 200 mL 1 mol·L-1氯化鈣溶液中c(Cl-)和100 mL 2 mol·L-1氯化鉀溶液中c(Cl-)
C. 64 g二氧化硫中氧原子數和標準狀況下22.4 L一氧化碳中氧原子數
D. 20% NaOH溶液中NaOH的物質的量濃度和10% NaOH溶液中NaOH的物質的量濃度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表列出了①~⑨九種元素在周期表中的位置。

請按要求回答下列問題:
(1)元素⑦的原子結構示意圖______________________。①、④按原子個數比為1:1組成的分子的電子式____________________;由②、④兩種元素組成的一種化合物的結構式________________;
(2)⑤⑥兩種元素的原子半徑由大到小的順序是____________(填元素符號)。
(3)⑧和⑨兩種元素的最高價氧化物對應的水化物中酸性較弱的是________(填化學式)。
(4)元素③的氣態氫化物和元素⑧的氣態氫化物易于制備的是___________(填化學式)。
(5)元素⑤的最高價氧化物對應的水化物與元素⑦的最高價氧化物對應水化物反應,其離子方程式為_________________________________________。
(6)元素①、④、⑤兩兩之間可以形成兩種類型的化合物,寫出一種共價化合物的化學式__________________ ;一種離子化合物的化學式_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某工廠的工業廢水中含有大量的“FeSO4”、較多的Cu2+和少量的Na+。為了減少污染變廢為寶,工廠計劃從該廢水中回收硫酸亞鐵和銅。根據流程圖,完成回收硫酸亞鐵和銅的簡單實驗方案。回答下列問題:

(1)加入原料①為____________;操作②的名稱為___________,該操作所用到的玻璃儀器主要有______。
(2)固體A為____________;
(3)寫出加入原料①和②有關反應的離子方程式__________________、________________________。
(4)操作③獲得FeSO4·7H2O,需要經過_____、_____、過濾等操作。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com