
25℃時,下列有關溶液中微粒的物質的量濃度關系正確的是
| A.0.1mol/LCH3COONa與0.1mol/LHCl溶液等體積混合:c(Na+)=c(Cl-)>cCH3COO-)>c(OH-) |
| B.0.1mol/LNH4Cl與0.1mol/L氨水等體積混合(pH>7):c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-) |
C.0.1mol/LNa2CO3與0.1mol/L NaHCO3溶液等體積混合: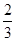 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D.0.1mol/LNa2C2O4與0.1mol/LHCl溶液等體積混合(H2C2O4為二元弱酸): |
AC
解析試題分析:A、0.1mol/LCH3COONa與0.1mol/LHCl溶液等體積恰好反應混合生成醋酸和氯化鈉,醋酸電離溶液顯酸性,則c(Na+)=c(Cl-)>cCH3COO-)>c(OH-),A正確;B、0.1mol/LNH4Cl與0.1mol/L氨水等體積混合(pH>7),這說明溶液顯堿性,因此氨水的電離程度大于銨根的水解程度,則c(NH4+)>c(Cl-)>c(NH3·H2O)>c(OH-),B不正確;C、0.1mol/LNa2CO3與0.1mol/L NaHCO3溶液等體積混合,則根據物料守恒可知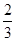 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),C正確;D、0.1mol/LNa2C2O4與0.1mol/LHCl溶液等體積混合(H2C2O4為二元弱酸),二者恰好反應生成草酸酸氫鈉和氯化鈉,則根據電荷守恒可知溶液中2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),D不正確,答案選AC。
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),C正確;D、0.1mol/LNa2C2O4與0.1mol/LHCl溶液等體積混合(H2C2O4為二元弱酸),二者恰好反應生成草酸酸氫鈉和氯化鈉,則根據電荷守恒可知溶液中2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),D不正確,答案選AC。
考點:考查溶液中離子濃度大小比較


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:單選題
已知同溫度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或電離出S2-的能力而言,FeS>H2S>CuS,則下列離子方程式錯誤的是
| A.Mg2+ + 2HCO3- + 2Ca2+ + 4OH-= Mg(OH)2↓+ 2CaCO3↓+ 2H2O |
| B.Cu2+ + H2S = CuS↓+ 2H+ |
| C.Zn2+ + S2- + 2H2O = Zn(OH)2↓+ H2S↑ |
| D.FeS + 2H+= Fe2+ + H2S↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
海洋中有豐富的食品、礦產、能源、藥物和水產資源,下圖為海水利用的部分過程。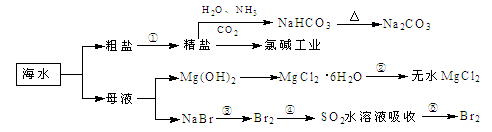
下列有關說法正確的是
| A.過程①中除去粗鹽中的SO、Ca2+、Mg2+、Fe3+等雜質,加入的藥品順序為:Na2CO3溶液→NaOH溶液→BaCl2溶液→過濾后加鹽酸 |
| B.用澄清的石灰水可鑒別NaHCO3和Na2CO3 |
| C.過程②中結晶出的MgCl2·6H2O要在HCl氛圍中加熱脫水制得無水MgCl2 |
| D.工業上通過電解飽和MgCl2溶液制取金屬鎂 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
溴酸銀(AgBrO3)溶解度隨溫度變化曲線如圖所示,下列說法錯誤的是( )
| A.溴酸銀的溶解時放熱過程 |
| B.溫度升高時溴酸銀溶解速度加快 |
| C.60 ℃時溴酸銀的Ksp約等于6×10-4 |
| D.若硝酸鉀中含有少量溴酸銀,可用重結晶方法提純 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
室溫下,下列溶液中粒子濃度大小關系正確的是
| A.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) |
| B.Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) |
| C.Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-) |
| D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
室溫下,對于醋酸及其鹽的下列判斷正確的是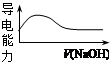
| A.稀醋酸溶解石灰石的離子方程式為 CaCO3+2H+=Ca2++H2O+CO2↑ |
| B.稀醋酸加水稀釋后,溶液中c(CH3COO-)/c(CH3COOH)變大 |
| C.向稀醋酸中加入等濃度的NaOH溶液,導電能力變化如右圖 |
| D.CH3COONH4溶液和K2SO4溶液均顯中性,兩溶液中水的電離程度相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
25℃時,下列各溶液中有關微粒的物質的量濃度關系正確的是
| A.在0.1 mol·L-1Na2S溶液中:2c(Na+) =c(S2-)+c(HS-) +c(H2S) |
| B.pH=2的醋酸溶液與pH=12的NaOH溶液等體積混合:c(Na+)+ c(H+)= c(OH-)+c(CH3COO-) |
| C.向0.1 mol·L-1鹽酸與0.1 mol·L-1K2CO3溶液等體積混合: c(K+) >c(Cl-)>c(HCO3-)>c(OH-)>c(H+) |
| D.向0.1 mol·L-1NH4HSO4溶液中滴加NaOH至溶液恰好呈中性: |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,下列說法不正確的是
A.等體積、等物質的量濃度的NaCl(aq) 離子總數大于NaClO(aq)中離子總數
B.pH=3的硫酸溶液中水的電離程度等于pH=11的氨水溶液中水的電離程度
C.0.1 mol/L的NaHA溶液pH=5,則溶液:c(HA-)>c(H+)>c(A2-)>c(H2A)
D.向NH4Cl溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(Cl-)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
25℃時,向20.00mLNaOH溶液中逐滴加入0.20mo1·L-l的CH3COOH溶液得到如圖曲線。下列說法正確的是
| A.水電離出的氫離子濃度:a>b |
| B.c點時恰好中和 |
| C.在d~e之間存在如下關系:C(Na十)>c(CH3COO-)>c(H十)>c(OH一) |
| D.e點時溶液中溶質是CH3COONa和CH3COOH |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com