
某化工廠的含鎳廢催化劑主要含Ni,還含有Al、Al2O3、Fe、FeO、Fe2O3及其他不溶雜質(其他不溶雜質不與酸堿反應)。某校化學研究性學習小組設計了如下圖所示的方法,以該含鎳廢催化劑為原料來制備NiSO4·7H2O。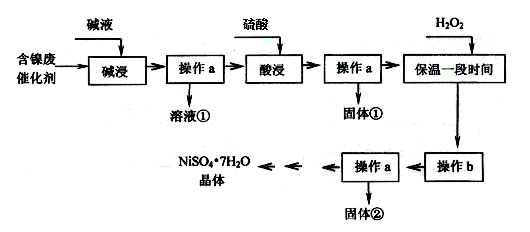
【查閱資料】
①Ni能與非氧化性酸反應生成Ni2+,不與堿液反應。
②部分陽離子以氫氧化物形式沉淀時pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 開始沉淀的pH | 4.1 | 1.7 | 7.6 | 7.0 |
| 完全沉淀的pH | 5.2 | 3.2 | 9.5 | 9.2 |
 2Ni(OH)2,寫出該反應放電時正極反應式 。
2Ni(OH)2,寫出該反應放電時正極反應式 。 。
。 (1)過濾 (2分) (2)Al、Al2O3(2分) (3)3.2≤pH<7.0 (2分)
(4)①2Ni2++ClO-+4OH-=2NiOOH+Cl-+H2O(3分) ②NiOOH + H2O + e- = Ni(OH)2 + OH- (3分)
(5)1.0×10-14 mol3·L-3(2分)
解析試題分析:(1)捏Ni、Fe、FeO、Fe2O3及其他不溶雜質均不與堿反應,所以堿液浸后金屬鋁、氧化鋁溶解,其它物質不溶,過濾即可除去,所以操作a是過濾。
(2)“堿浸”的目的是除去含鎳廢催化劑Al、Al2O3。
(3)由于前面加入了氧化劑雙氧水,所以溶液中的亞鐵離子被氧化生成了鐵離子。根據表中數據可知,鐵離子完全沉淀時的pH值是3.2,而Ni2+開始沉淀時的pH值是7.0,因此操作b應該控制溶液的pH值為3.2≤pH<7.0。
(4)①NiSO4在強堿溶液中用次氯酸鈉氧化,可以制得堿性鎳氫電池電極材料NiOOH,在反應中氯元素的化合價從+1價降低到-1價,得到2個電子。而Ni元素的化合價從+2價升高到+3價失去1個電子,所以還原劑硫酸鎳與氧化劑次氯酸鈉的物質的量之比是2:1,因此反應的離子方程式為2Ni2++ClO-+4OH-=2NiOOH+Cl-+H2O。
②原電池中負極失去電子,發生氧化反應。電子經導線傳遞到正極,所以正極得到電子,發生還原反應。根據方程式可知放電時氫氣是還原劑失去電子,NiOOH是氧化劑得到電子,做正極,因此正極電極反應式為NiOOH + H2O + e- = Ni(OH)2 + OH-。
③根據表中數據可知,氫氧化亞鐵完全沉淀時的pH值是9.5,根據氫氧化亞鐵的溶度積常數表達式Ksp=c(Fe2+)·c2(OH-),氫氧化亞鐵的溶度積常數Ksp=1.0×10-5 mol·L-1×(10-4.5mol/L)2=1.0×10-14 mol3·L-3。
考點:考查物質制備工藝流程的有關判斷、溶度積常數的有關計算與應用、氧化還原反應方程式的書寫以及電極反應式的書寫等


科目:高中化學 來源: 題型:填空題
(1)在0.10 mol·L-1硫酸銅溶液中加入氫氧化鈉稀溶液充分攪拌有淺藍色氫氧化銅沉淀生成,當溶液的pH=8時,c(Cu2+)=
mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。
(2)若在0.1 mol·L-1硫酸銅溶液中通入過量H2S氣體,使Cu2+完全沉淀為CuS,此時溶液中的H+濃度是 mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有A、B、C、D、E五種可溶強電解質,它們在水中可電離產生下列離子(各種離子不重復)。
| 陽離子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 陰離子 | OH-、Cl-、CO32-、NO3-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有pH=2的醋酸溶液甲和pH=2的鹽酸乙,請根據下列操作完成問題:
(1)取10 mL的甲溶液,加入等體積的水,醋酸的電離平衡________(填“向左”、“向右”或“不”)移動;另取10 mL的甲溶液,加入少量無水醋酸鈉固體(假設加入固體前后,溶液體積保持不變),待固體溶完后,溶液中[H+]/[CH3COOH]的比值將________(填“增大”、“減小”或“無法確定”)。
(2)相同條件下,取等體積的甲、乙兩溶液,各稀釋100倍。稀釋后的溶液,其pH大小關系為:pH(甲)________pH(乙)。(填“大于”、“小于”或“等于”,下同)
(3)各取25 mL的甲、乙兩溶液,分別用等濃度的NaOH稀溶液中和至pH=7,則消耗的NaOH溶液的體積大小關系為:V(甲)________V(乙)。
(4)取25 mL的甲溶液,加入等體積pH=12的NaOH溶液,反應后溶液中c(Na+)、c(CH3COO-)的大小關系為:c(Na+)________c(CH3COO-)。
(5)取25 mL的乙溶液,加入等體積pH=12的氨水,反應后溶液中的溶質為_________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
科學家利用淡水與海水之間含鹽量的差別發明了一種新型電池——水電池。
(1)用二氧化錳納米棒作電池正極可提高發電效率,這是利用納米材料的 特性,使之能與鈉離子充分接觸。
(2)水電池總反應可表示為:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,該電池的負極反應式為 。水電池工作時,Na+不斷向 極方向移動。
(3)水電池生成1 mol Na2Mn5O10轉移電子的物質的量為 。
(4)某溫度下,Fe(OH)3(s)、Mg(OH)2(s)分別在溶液中達到沉淀溶解平衡后,溶液中金屬陽離子的濃度與溶液pH的關系如右圖。請據右圖分析: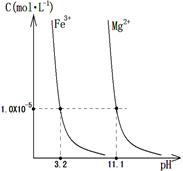
①該溫度下,溶度積常數的關系為:KSP[Fe(OH)3] KSP[Mg(OH)2](填“>”、“=”或“<”);
②如果在新生成的Mg(OH)2濁液中滴入足量的FeCl3溶液,振蕩后,白色沉淀會全部轉化為紅褐色沉淀,原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知:在室溫時H2O H++OH- KW=10-14 CH3COOH
H++OH- KW=10-14 CH3COOH  H++ CH3COO- Ka=1.8×10-5
H++ CH3COO- Ka=1.8×10-5
(1)取適量醋酸溶液,加入少量醋酸鈉固體,此時溶液中C(H+)與C(CH3COOH)的比值 (填“增大”或“減小”或“不變”)
(2)醋酸鈉水解的離子方程式為 。當升高溫度時,C(OH—)將 (填“增大”“減小”“不變”);
(3)0.5mol·L-1醋酸鈉溶液pH為m,其水解的程度(已水解的醋酸鈉與原有醋酸鈉的比值)為a;1mol·L-1醋酸鈉溶液pH為n,水解的程度為b,則m與n的關系為 ,a與b的關系為 (填“大于”“小于”“等于”);
(4)將等體積等濃度的醋酸和氫氧化鈉溶液混合后,所得溶液中離子濃度由大到小的順序是 。
(5)若醋酸和氫氧化鈉溶液混合后pH<7,則c(Na+)_______________ c(CH3COO-)(填“大于”、“小于”或“等于”),
(6)室溫時,若由pH=3的HA溶液V1mL與pH=11的NaOH溶液V2 mL混合,則下列說法不正確的是____________。
| A.若反應后溶液呈中性,則c(H+)+c(OH-)=2×10-7mol·L-1 |
| B.若V1=V2,反應后溶液pH一定等于7 |
| C.若反應后溶液呈酸性,則V1一定大于V2 |
| D.若反應后溶液呈堿性,則V1一定小于V2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
25℃時,將0.01molCH3COONa和0.002molHCl溶于水,形成1L混合溶液。
(1)該溶液中存在著三個平衡體系,用電離方程式或離子方程式表示:
A___________________________________________________;
B____________________________________________________;
C___________________________________________________。
(2)溶液中共有______________種不同的粒子。
(3)在這些粒子中,濃度為0.01mol/L的是 ;濃度為0.002mol/L的是 。
(4) 和 兩種粒子物質的量之和等于0.01mol。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
亞磷酸(H3PO3)是二元酸,H3PO3溶液存在電離平衡:H3PO3  H+ + H2PO3-。亞磷酸與足量NaOH溶液反應,生成Na2HPO3。
H+ + H2PO3-。亞磷酸與足量NaOH溶液反應,生成Na2HPO3。
(1)①寫出亞磷酸與少量NaOH溶液反應的離子方程式____________________________。
②某溫度下,0.1000 mol·L-1的H3PO3溶液pH的讀數為1.6,即此時溶液中c (H+) = 2.5×10-2 mol·L-1,除OH-之外其他離子的濃度由小到大的順序是 ,該溫度下H3PO3電離平衡的平衡常數K= 。(H3PO3第二步電離忽略不計,結果保留兩位有效數字)
③向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中
c(Na+)_______ c(H2PO3-)+ 2c(HPO32-)(填“>”、 “<” 或“=”)。
(2)亞磷酸具有強還原性,可使碘水褪色,該反應的化學方程式_______________________。
(3)電解Na2HPO3溶液也可得到亞磷酸,裝置示意圖如下: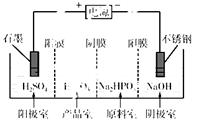
說明:陽膜只允許陽離子通過,陰膜只允許陰離子通過。
①陰極的電極反應式為________________________。
②產品室中反應的離子方程式為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
常溫下,如果取0.1 mol/L HA溶液與0.1 mol/L NaOH溶液等體積混合(忽略混合后
溶液體積的變化),測得混合溶液的pH=8,試回答以下問題:
(1)混合溶液的pH=8的原因: (用離子方程式表示)。
(2)混合溶液中由水電離出的c(H+) (填“>”“<”或“=”)0.1 mol/L NaOH
溶液中由水電離出的c(H+)。
(3)求出混合液中下列算式的精確計算結果(填具體數字):
c(Na+)-c(A-)= mol/L,
c(OH-)-c(HA) = mol/L。
(4)已知NH4A溶液為中性,又知HA溶液加到Na2CO3溶液中有氣體放出,試推斷(NH4)2CO3
溶液的pH (填“大于”“小于”或“等于”)7;將同溫度下等濃度的四
種鹽溶液:
A.NH4HCO3 B.NH4A C.(NH4)2SO4 D.NH4Cl
按pH由大到小的順序排列是 (填序號)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com