
【題目】下列敘述中,正確的是( )
A.氧化還原反應的本質是元素化合價發生了變化
B.所含元素化合價升高的反應物被氧化
C.得到電子的物質被氧化
D.氧化還原反應中,氧化劑和還原劑一定是兩種物質
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】實驗室中需要配制2mol/L的NaCl溶液950mL,配制時應選用的容量瓶的規格和稱取的NaCl質量分別是( )
A.950 mL,111.2 g
B.500 mL,117 g
C.1 000 mL,117 g
D.任意規格,111.2 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式如圖所示,下列有關該有機物的說法中正確的是

A. 能和碳酸鈉溶液反應的官能團有2種
B. 1mol該有機物最多能與2molH2發生加成
C. 與![]() 互為同分異構體
互為同分異構體
D. 既可以發生取代反應又可以發生氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用下列實驗裝置完成對應的實驗,能達到實驗目的的是
A. 制取并收集少量氨氣 
B. 比較NaHCO3和Na2CO3的熱穩定性
C. 制取并檢驗乙烯
D. 比較鹽酸、碳酸、硅酸的酸性強弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,水的電離達到平衡: H2O![]() H++ OH-ΔH > 0 ,下列敘述正確的是
H++ OH-ΔH > 0 ,下列敘述正確的是
A. 將水加熱,Kw增大,pH不變
B. 向水中加入少量鹽酸,c(H+)增大,Kw不變
C. 向水中加入NaOH固體,平衡逆向移動,c(OH-) 降低
D. 向水中加入AlCl3固體,平衡逆向移動,c(OH-) 增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D為原子序數依次增大的短周期元素,A元素氣態氫化物的水溶液呈堿性,B為最活潑的非金屬元素,C元素原子的電子層數是最外層電子數的3倍,D元素最高化合價為+6價。
(1)A元素氣態氫化物的電子式為______;B在元素周期表中的位置為________。
(2)DBn做制冷劑替代氟利昂,對臭氧層完全沒有破壞作用,是一種很有發展潛力的制冷劑。該物質的摩爾質量為146 g·mol-1,則該物質的化學式為_____。已知DBn在溫度高于45℃時為氣態,DBn屬于____晶體。該物質被稱為人造惰性氣體,目前廣泛應用于電器工業,在空氣中不能燃燒,請從氧化還原角度分析不能燃燒的理由_________。
(3)C與氫元素組成1∶1的化合物,與水發生劇烈反應生成堿和一種氣體,寫出該反應的化學反應方程式____________,生成1mol氣體轉移的電子的數目為______個。
(4)A和C兩元素可形成離子化合物甲。取13.0g化合物甲,加熱使其完全分解,生成A的單質和C的單質,生成的A單質氣體折合成標準狀況下的體積為6.72L。化合物甲分解的化學方程式為______________________________。
(5)D元素的+4價含氧酸鈉鹽在空氣中容易變質,設計實驗方案證明該鹽已經變質____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用鋅粒和稀硫酸反應制取氫氣,下列措施不能使反應速率加快的是
A. 鋅粉代替鋅粒 B. 滴加少量硫酸銅溶液
C. 滴加少量98%的濃硫酸 D. 降低反應溫度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是2SO3(g)![]() 2SO2(g)+O2(g)的能量變化圖,據圖得出的相關敘述正確的是( )
2SO2(g)+O2(g)的能量變化圖,據圖得出的相關敘述正確的是( )
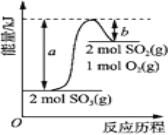
A. 該化學反應過程中既有能量的吸收又有能量的釋放
B. 2SO3(g)![]() 2SO2(g)+O2(g) △H=-(a-b) kJ/mol
2SO2(g)+O2(g) △H=-(a-b) kJ/mol
C. 1 mol SO2的能量比1 mol SO3的能量高
D. 若某容器內有2 mol SO3充分反應,吸收(a-b) kJ熱量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 3.0L0.1mol·L-1NaOH溶液中緩慢通入CO2至溶液增重8.8g時。溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
B. 常溫下,將CH3COONa溶液和鹽酸混合至溶液pH=7:c(Na+)>c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)=c(OH-)
C. 常溫下,pH=6的NaHSO3溶液中:c(SO32-)- c(H2SO3)=9.9×10-7mol·L-1
D. Ksp (Fe(OH)3)=1.0×10-38,Ksp (Mg(OH)2)=1.0×10-11,則濃度均為0.1 mol·L-1氯化鐵、氯化鎂混合溶液,若除去溶液中的Fe3+,應將pH調至3~11。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com