
下列生產或實驗事實引出的相應結論不正確的是( )
| | 事實 | 結論 |
| A | 其他條件相同,Na2S2O3溶液和H2SO4溶液反應,升高溶液的溫度,析出硫沉淀所需時間縮短 | 當其他條件不變時,升高反應溫度,化學反應速率加快 |
| B | 工業制硫酸中,在SO3的吸收階段,吸收塔里要裝填瓷環 | 增大氣液接觸面積,使SO3的吸收速率增大 |
| C |  在容積可變的密閉容器中發生反應:2NH3(g)??N2H4(l)+H2(g),把容積的體積縮小一半 在容積可變的密閉容器中發生反應:2NH3(g)??N2H4(l)+H2(g),把容積的體積縮小一半 | 正反應速率加快,逆反應速率減慢 |
| D | A、B兩支試管中分別加入等體積5%的H2O2溶液,在B試管中加入2~3滴FeCl3溶液,B試管中產生氣泡快 | 當其他條件不變時,催化劑可以改變化學反應速率 |
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:單選題
下列有關說法正確的是
| A.鐵表面鍍銅時,銅與電源的正極相連,鐵與電源的負極相連 |
| B.用pH均為2的鹽酸和醋酸分別中和等物質的量的NaOH,消耗醋酸的體積更大 |
| C.一定溫度下,反應2Mg(s)+CO2(g)=2MgO(s)+C(s)能自發進行,則該反應△H<0 |
| D.常溫下,向飽和Na2CO3溶液中加少量BaSO4粉末,過濾,向洗凈的沉淀中加稀鹽酸有氣泡產生,說明常溫下Ksp(BaCO3)<Ksp(BaSO4) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在某密閉容器中,可逆反應:A(g)+B(g) xC(g)符合圖像(Ⅰ)所示關系。由此推斷,對圖像(Ⅱ)的不正確的說法是( )
xC(g)符合圖像(Ⅰ)所示關系。由此推斷,對圖像(Ⅱ)的不正確的說法是( )
| A.p3>p4,y軸表示A的轉化率 |
| B.p3>p4,y軸表示B的質量分數 |
| C.p3>p4,y軸表示C的質量分數 |
| D.p3>p4,y軸表示混合氣體的平均相對分子質量 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
為了探究外界條件對反應aX(g)+bY(g)  cZ(g)的影響,以X和Y物質的量之比為a∶
cZ(g)的影響,以X和Y物質的量之比為a∶
b開始反應,通過實驗得到不同條件下達到平衡時Z的體積分數,實驗結果如下圖所示。以下判斷正確的是( )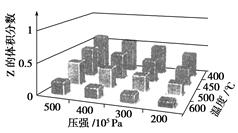
| A.ΔH>0,a+b>c | B.ΔH>0,a+b<c |
| C.ΔH<0,a+b>c | D.ΔH<0,a+b<c |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在25 ℃、1.01×105 Pa下,反應2N2O5(g) 4NO2(g)+O2(g) ΔH="+56.7" kJ·mol-1能自發進行的合理解釋是( )
4NO2(g)+O2(g) ΔH="+56.7" kJ·mol-1能自發進行的合理解釋是( )
| A.該反應是分解反應 |
| B.該反應的熵增效應大于焓變效應 |
| C.該反應是熵減反應 |
| D.該反應是放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在密閉容器中進行反應:H2(g)+Br2(g) 2HBr(g) ΔH<0,達到平衡后,欲使顏色加深,應采取的措施是( )
2HBr(g) ΔH<0,達到平衡后,欲使顏色加深,應采取的措施是( )
| A.升高溫度 | B.降低溫度 |
| C.增大H2濃度 | D.減小壓強 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
碳酸銨[(NH4)2CO3]室溫下能自發地分解產生氨氣,對其說法正確的是( )
| A.碳酸銨分解是因為生成了易揮發的氣體,使體系的熵增大 |
| B.碳酸銨分解是因為外界給予了能量 |
| C.該反應的ΔH-TΔS>0 |
| D.碳酸鹽都不穩定,都能自發分解 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
納米是長度單位,1納米等于1×10-9 m,物質的顆粒達到納米級時,具有特殊的性質。例如將單質銅制成“納米銅”時,具有非常強的化學活性,在空氣中可以燃燒。下列對“納米銅”的有關敘述正確的是( )
| A.常溫下“納米銅”比銅片的金屬性強,反應時反應速率快 |
| B.常溫下“納米銅”比銅片更易失電子,反應時反應速率快 |
| C.常溫下“納米銅”的還原性大于銅片的還原性 |
| D.“納米銅”顆粒更細小,化學反應時接觸面大,所以反應速率快 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在2NO2(紅棕色) N2O4(無色)的可逆反應中,下列狀態一定屬于平衡狀態的是( )。
N2O4(無色)的可逆反應中,下列狀態一定屬于平衡狀態的是( )。
| A.N2O4和NO2的分子數比為1∶2 |
| B.N2O4和NO2的濃度相等 |
| C.平衡體系的顏色不再改變 |
| D.單位時間內有1 mol N2O4變為NO2的同時,有1 mol NO2變為N2O4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com