
【題目】用惰性電極電解一定濃度的硫酸銅溶液,通電一段時間后,向所得的溶液中加入0.1molCu2(OH)2CO3后恰好恢復到電解前的濃度和pH(不考慮CO2的溶解)。則電解過程中共轉移電子的物質的量為( )
A. 0.4mol B. 0.5mol C. 0.6mol D. 0.8mol
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】研究CO2的利用對促進低碳社會的構建具有重要意義。
(1)將CO2與焦炭作用生成CO,CO可用于煉鐵等。
已知:
Fe2O3(s)+3CO(s,石墨)═2Fe(s)+3CO2(g)△H1=+489.0kJmol﹣1
C(s,石墨)+CO2(g)═2CO(g)△H2=+172.5kJmol﹣1
則CO還原Fe2O3(s)的熱化學方程式為_____。
(2)二氧化碳合成甲醇是碳減排的新方向,將CO2轉化為甲醇的熱化學方程式為:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H
①取一定體積CO2和H2的混合氣體(物質的量之比為1:3),加入恒容密閉容器中,發生上述反應反應過程中測得甲醇的體積分數φ(CH3OH)與反應溫度T的關系如圖1所示,則該反應的△H____0(填“>”、“<”或“=”,下同)。
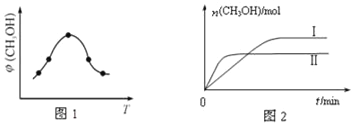
②在兩種不同條件下發生反應,測得CH3OH的物質的量隨時間變化如圖2所示,曲線I、Ⅱ對應的平衡常數關系為KⅠ_____KⅡ。
(3)以CO2為原料還可以合成多種物質。
①工業上尿素[CO(NH2)2]由CO2和NH3在一定條件下合成.開始以氨碳比![]() =3進行反應,達平衡時CO2的轉化率為60%,則NH3的平衡轉化率為_____。
=3進行反應,達平衡時CO2的轉化率為60%,則NH3的平衡轉化率為_____。
②將足量CO2通入飽和氨水中可得氮肥NH4HCO3,已知常溫下一水合氨Kb=1.8×10﹣5,碳酸一級電離常數Ka=4.3×10﹣7,則NH4HCO3溶液呈_____(填“酸性”、“中性”或“堿性”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,將1.000mol·L-1鹽酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和溫度隨加入鹽酸體積變化曲線如下圖所示。下列有關說法正確的是( )
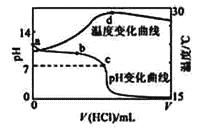
A. a點由水電離出的c(H+)=1.0×10-14mol/L
B. b點:c(NH4+)+c(NH3·H2O) > c(Cl-)
C. c點:反應消耗的HCl 和NH3·H2O 的關系為:n(HCl)= n(NH3·H2O)
D. d點后,溶液溫度略下降的主要原因是NH3·H2O電離吸熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】《本草衍義》中對精制砒霜過程有如下敘述:“取砒之法,將生砒就置火上,以器覆之,令砒煙上飛著覆器,遂凝結累然下垂如乳,尖長者為勝,平短者次之.”文中涉及的操作方法是( )
A.蒸餾
B.升華
C.干餾
D.萃取
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關化學與生活的說法錯誤的是( )
A.鐵粉、生石灰均可作食品抗氧化劑
B.明礬、氯化鐵均可作凈水劑
C.牛奶、雞蛋清均可用于重金屬中毒解毒
D.碘酒、雙氧水均可用于傷口消毒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸是一種重要的含氧酸.實驗室用濃硫酸與乙二酸(H2C2O4)晶體加熱,可獲得CO與CO2的混合氣體,再將混合氣體進一步通過(填一種試劑的名稱)即可得純凈干燥的CO.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知有機物A~I之間的轉化關系如圖所示:
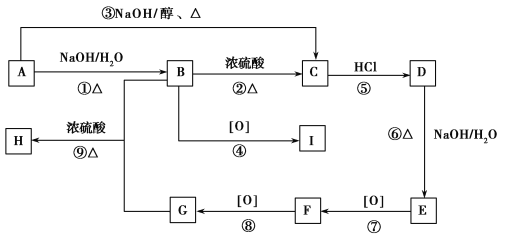
①A與D、B與E、I與F互為同分異構體;
②C的最簡式與乙炔相同,且相對分子質量為104;
③A~I均為芳香族化合物。
根據以上信息,回答下列問題:
(1)G中含有的官能團名稱為________________。
(2)H的結構簡式________________。
(3)I與F互為同分異構體,下列能夠鑒別兩者的方法或試劑是________。
A.李比希法 B.質譜法 C.紅外光譜法 D.核磁共振氫譜法 E.銀氨溶液
(4)寫出反應⑥的化學方程式:_______________________________。
(5)寫出E→F反應的化學方程式:____________________________。
(6)苯環上含有兩個取代基且能與NaOH溶液反應,但不與FeCl3溶液發生顯色反應的G的同分異構體有________種。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列變化過程中,ΔS<0的是
A. 氯化鈉溶于水中 B. NH3(g)與HCl(g)反應生成NH4Cl(s)
C. 汽油的燃燒 D. 煅燒石灰石得到生石灰和二氧化碳
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅單質及其化合物在很多領域中都有重要的用途。請回答以下問題:
(1)超細銅粉可用作導電材料、催化劑等,其制備方法如下:
![]()
![]()
![]()
![]()
![]()
①NH4CuSO3中金屬陽離子的核外電子排布式為__________________。N、O、S三種元素的第一電離能大小順序為____________________(填元素符號)。
②向CuSO4溶液中加入過量氨水,可生成[Cu(NH3)4]SO4,下列說法正確的是________。
A.氨氣極易溶于水,原因之一是NH3分子和H2O分子之間形成氫鍵的緣故
B.NH3分子和H2O分子,分子空間構型不同,氨氣分子的鍵角小于水分子的鍵角
C.[Cu(NH3)4]SO4溶液中加入乙醇,會析出深藍色的晶體
D.已知3.4 g氨氣在氧氣中完全燃燒生成無污染的氣體,并放出a kJ熱量,則NH3的燃燒熱的熱化學方程式為:NH3(g)+3/4O2(g)===1/2N2(g)+3/2H2O(g) ΔH=-5a kJ·mol-1
(2)銅錳氧化物(CuMn2O4)能在常溫下催化氧化空氣中的氧氣變為臭氧(與SO2互為等電子體)。根據等電子體原理,O3分子的空間構型為________。
(3)氯和鉀與不同價態的銅可生成兩種化合物,其陰離子均為無限長鏈結構(如圖所示),a位置上Cl原子(含有一個配位鍵)的雜化軌道類型為_______________________。
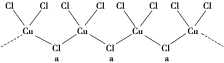
(4)如圖是金屬Ca和D所形成的某種合金的晶胞結構示意圖,已知鑭鎳合金與上述Ca-D合金都具有相同類型的晶胞結構XYn,它們有很強的儲氫能力。已知鑭鎳合金LaNin晶胞體積為9.0×10-23 cm3,儲氫后形成LaNinH4.5合金(氫進入晶胞空隙,體積不變),則LaNin中n=________(填數值);氫在合金中的密度為________(保留兩位有效數字)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com