
【題目】室溫時,CaCO3在水中的溶解平街曲線如陽所示。已知25℃其濃度積為2.8×10-9mol2/L2,下列說法不正的是( )
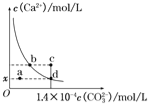
A. x數值為2×10-5 B. c點時有碳酸鈣沉淀生成
C. 加入蒸餾水可使溶液由d 點變到a點 D. b點與d對應的的溶度積相等
科目:高中化學 來源: 題型:
【題目】已知甲為恒壓容器、乙為恒容容器。相同條件下充入等物質的量NO2氣體,且起始時體積相同。發生反應:2NO2(g)![]() N2O4(g) △H<0。一段時間后均達到平衡狀態。下列說法中正確的是
N2O4(g) △H<0。一段時間后均達到平衡狀態。下列說法中正確的是
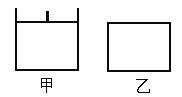
A. 平衡時NO2體積分數:甲<乙
B. 達到平衡所需時間,甲與乙相等
C. 該反應的平衡常數表達式K=c(N2O4)/c(NO2)
D. 若兩容器內氣體的壓強保持不變,均說明反應已達到平衡狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下到有關電解質溶液的說法不正確的是( )
A. 向Na2CO3溶液中通入NH3, 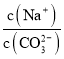 減小
減小
B. 將0.1mol·L-1的K2C2O4溶液從25℃升溫至35℃,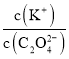 增大
增大
C. 向0.1mol·L-1的HF溶液中滴加NaOH溶液至中性, 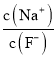 =1
=1
D. 向0.1mol·L-1的CH3COONa溶液中加入少量水, 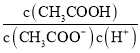 增大
增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖中的實驗,能達到實驗目的的是( )
A.  證明穩定性:Na2CO3>NaHCO3
證明穩定性:Na2CO3>NaHCO3
B.  證明非金屬性:Cl>Br>I
證明非金屬性:Cl>Br>I
C.  驗證鎂和鹽酸反應的熱效應
驗證鎂和鹽酸反應的熱效應
D. 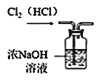 除去 Cl2 中的雜質氣體 HCl
除去 Cl2 中的雜質氣體 HCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定質量的鎂、鋁合金與硝酸恰好完全反應,得到硝酸鹽溶液和NO2、N2O4、NO的混合氣體,將這些氣體與標準狀況下3.36 L O2混合后通入水中,所有氣體恰好完全被水吸收生成硝酸。若向所得硝酸鹽溶液中加入2 mol/L NaOH溶液至沉淀最多時停止加入,將沉淀濾出,向濾液中加水稀釋至500 mL,此時所得溶液的物質的量濃度為( )
A. 0.5 mol/LB. 1 mol/L
C. 1.2 mol/LD. 2 mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組同學進行如下實驗,以檢驗化學反應中的能量變化。
(1)實驗中發現,反應后①中的溫度升高;②中的溫度降低.由此判斷鋁條與鹽酸的反應是______熱反應, Ba(OH)28H2O與NH4Cl反應時,需要將固體研細其目的是________________.反應過程______ (填“①”或“②”)的能量變化可用圖表示。

(2)為了驗證Fe3+與Cu2+氧化性強弱,下列裝置能達到實驗目的是_________(填序號)。

(3)將CH4設計成燃料電池,其利用率更高,裝置如圖所示(a、b為多孔碳棒)其中____(填A或B)處電極入口通甲烷,其電極反應式為_____________________ 。當消耗標況下甲烷33.6L時,假設能量轉化率為90%,則導線中轉移電子的物質的量為_________mol。

(4)如圖是某化學興趣小組探究不同條件下化學能轉變為電能的裝置.請回答下列問題:

①當電極c為Al、電極d為Cu、電解質溶液為稀硫酸時,寫出該原電池正極的電極反應式為_______________。
②當電極c為Al、電極d為Mg、電解質溶液為氫氧化鈉溶液時,該原電池的正極為_______;該原電池的負極反應式為_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】資料顯示不同濃度的硫酸與鋅反應時,硫酸可以被還原為SO2,也可被還原為氫氣。為了驗證這一事實,某同學擬用下圖裝置進行實驗(實驗時壓強為10lkPa,溫度為0℃)。
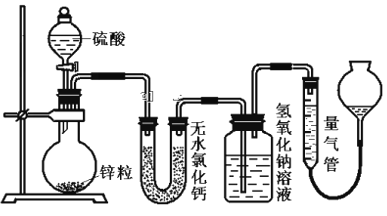
(1)若在燒瓶中放入1.30g鋅粒,與c mol/L H2SO4反應,為保證實驗結論的可靠,量氣管的適宜規格是_____________ (選填:200,400,500) mL 。
(2)若1.30g鋅粒完全溶解,氫氧化鈉洗氣瓶增重l.28g ,則圓底燒瓶中發生反應的化學方程式為:_______________________
(3)若燒瓶中投入a g鋅且完全反應,氫氧化鈉洗氣瓶增重b g.量氣瓶中收集到V mL氣體,則有: ![]() =
=![]() +
+![]() ,依據的原理是____________________________。
,依據的原理是____________________________。
(4)若在燒瓶中投入d g鋅,加入一定量的c mol/L 濃硫酸V L,充分反應后鋅有剩余,測得氫氧化鈉洗氣瓶增重m g,則整個實驗過程產生的氣體中,![]() =_______________(用含字母的代數式表示)。
=_______________(用含字母的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“低碳經濟”已成為全世界科學家研究的重要課題,其綜合利用具有重要意義。回答下列問題:
(1)CO2與CH4經催化重整,制得合成氣:CH4(g)+ CO2(g)![]() 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
①已知上述反應中相關的化學鍵鍵能數據如下:
化學鍵 | C—H | C=O | H—H | C |
鍵能/kJ·mol1 | 413 | 745 | 436 | 1075 |
則該反應的ΔH=_________。有利于提高CH4平衡轉化率的條件是____(填標號)。
A.高溫低壓 B.低溫高壓 C.高溫高壓 D.低溫低壓
②某溫度下,在體積為2 L的容器中加入2 mol CH4、1 mol CO2以及催化劑進行重整反應,達到平衡時CO2的轉化率是50%,其平衡常數為_______mol2·L-2。
(2)CO2可以被NaOH溶液捕獲。若所得溶液c(HCO3)∶c(CO32 -)=2∶1,溶液pH=____。(室溫下,H2CO3的K1=4×10-7;K2=5×10-11),0.1mol·L-1 NaHCO3溶液中陰離子的濃度由大到小的順序為______________
(3)研究證實,CO2也可在酸性水溶液中通過電解生成甲醇,則生成甲醇的反應發生在_______極,該電極反應式是___________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】開發和利用礦物資源有重要的意義。某廠用無機礦物資源生產部分材料,其產品流程示意圖如下,下列有關說法不正確的是( )

A. 制取粗硅時生成的氣體產物為CO
B. 生產鋁、銅、高純硅及玻璃的過程中都涉及氧化還原反應
C. 黃銅礦冶煉銅時,產生的SO2可用于生產硫酸,產生的FeO可用作冶煉鐵的原料
D. 粗硅制高純硅時,提純四氯化硅可用多次分餾的方法
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com