


 浙江之星課時優化作業系列答案
浙江之星課時優化作業系列答案 激活思維優加課堂系列答案
激活思維優加課堂系列答案科目:初中化學 來源: 題型:閱讀理解
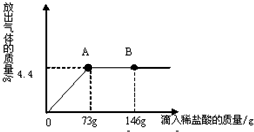
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
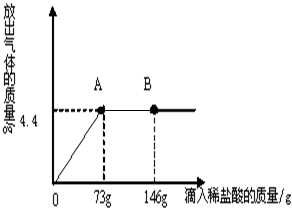 小剛在化學實驗室發現,盛放NaOH溶液的試劑瓶瓶口和橡皮塞上出現了白色粉末.小剛叫來小軍和小紅,共同探究這種白色粉末的成分.
小剛在化學實驗室發現,盛放NaOH溶液的試劑瓶瓶口和橡皮塞上出現了白色粉末.小剛叫來小軍和小紅,共同探究這種白色粉末的成分.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com